Содержание
- 2. «Возьмите первый слог названия «лунного элемента» и прибавьте к нему первый слог радиоактивного металла, открытого супругами
- 3. СЕРА
- 4. План урока: дать общую характеристику серы рассмотреть аллотропные модификации серы Физические и химические свойства нахождение в
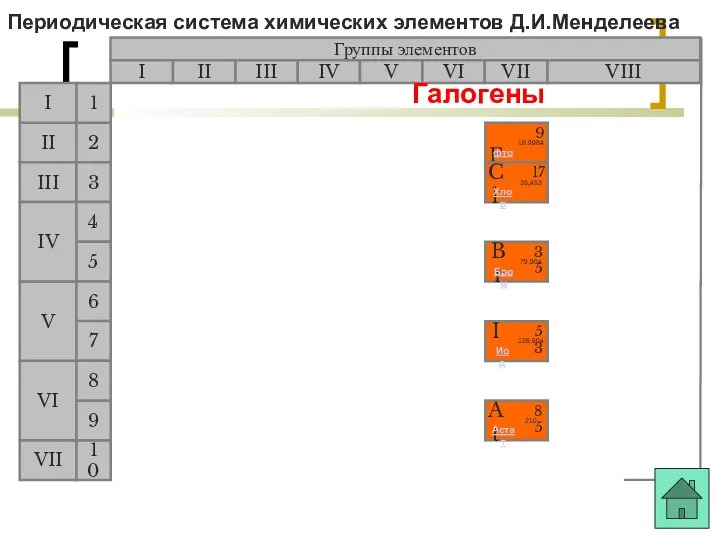
- 5. Периодическая система химических элементов Д.И.Менделеева Группы элементов I III II VIII IV V VI VII II
- 6. 1.Сера, как химический элемент 1)III малый период; VI(A) группаZ=16; e=16; р=16; Аr=32; n=16 2)S 2)8 )
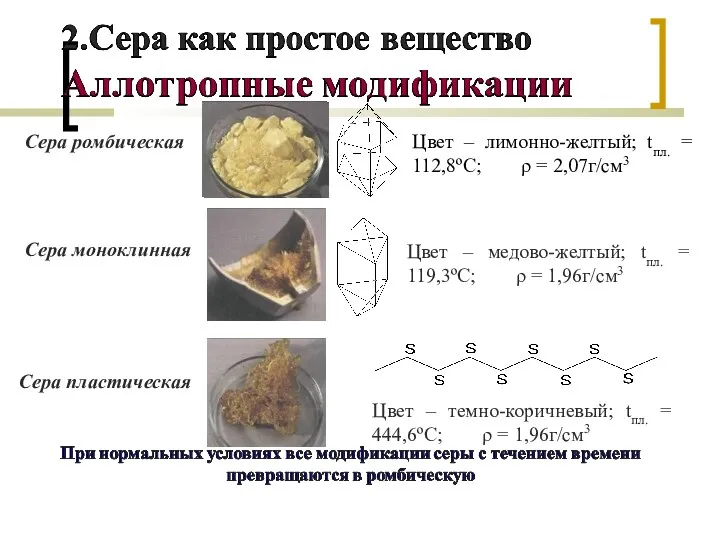
- 7. Сера ромбическая Сера пластическая Сера моноклинная Цвет – лимонно-желтый; tпл. = 112,8ºС; ρ = 2,07г/см3 Цвет
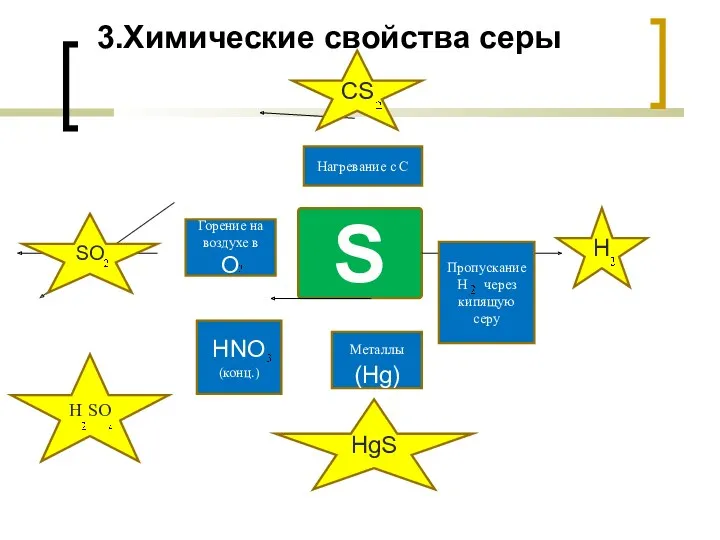
- 8. 3.Химические свойства серы S Пропускание Н через кипящую серу Металлы (Hg) HNO (конц.) Нагревание с С
- 9. Микропауза ДЛЯ УЛУЧШЕНИЯ МОЗГОВОГО КРОВООБРАЩЕНИЯ Крепко зажмурьте глаза на 3-5 секунд, а затем откройте их на
- 10. Сера - окислитель 1. 2S + C = CS 2 4 S S в-ся; ок-ль 1
- 11. 3.S + Hg = Hg S демеркуризация 12 S S в-ся; ок-ль 12 Hg Hg ок-ся;
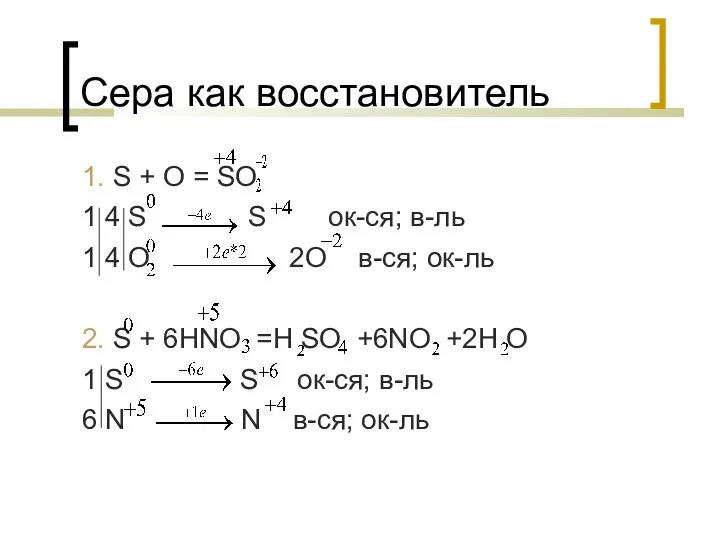
- 12. Сера как восстановитель 1. S + O = SO 1 4 S S ок-ся; в-ль 1
- 13. Закрепление Тест на взаимопроверку. 1. Строение атома серы: а) +15)2)8)5; б) +17)2)8)7; в) +16)2)8)6; г) +18)2)8)8
- 14. Ответы: 1.- в; 2.- а; 3 – б; 4 – б; 5 – г.
- 16. Скачать презентацию









 Выбор и проектирование заготовок. Лекция 4. Проектирование литых заготовок
Выбор и проектирование заготовок. Лекция 4. Проектирование литых заготовок Конспект совместной образовательной деятельности воспитателей и детей старшего дошкольного возраста Экскурсия на почтовое отделение(с презентацией)
Конспект совместной образовательной деятельности воспитателей и детей старшего дошкольного возраста Экскурсия на почтовое отделение(с презентацией) ПроектКомпетентность родителей как условие содействия нравственному и эмоциональному благополучию ребенка
ПроектКомпетентность родителей как условие содействия нравственному и эмоциональному благополучию ребенка презентация добро и зло
презентация добро и зло Транспорт и мировое хозяйство. 10 класс
Транспорт и мировое хозяйство. 10 класс Покорители космоса. 4 класс
Покорители космоса. 4 класс Мерез
Мерез Презентация проф 2024
Презентация проф 2024 Проектная деятельность учащихся
Проектная деятельность учащихся Игра Тропинки здоровья
Игра Тропинки здоровья Аймақтандыру және компартиментализация
Аймақтандыру және компартиментализация Свойства функции (9 класс)
Свойства функции (9 класс) The political system in the kingdom of Far Far Away
The political system in the kingdom of Far Far Away Судебная медицина. Введение в специальность
Судебная медицина. Введение в специальность Пневматический привод. Особенности пневматического привода
Пневматический привод. Особенности пневматического привода Перспектива модернизации самолета Ту-154
Перспектива модернизации самолета Ту-154 Виды и типы культурно-досуговой деятельности
Виды и типы культурно-досуговой деятельности З 8 березням!
З 8 березням! Отделка шерстяных тканей
Отделка шерстяных тканей Знакомство с Arduino. Lesson 1
Знакомство с Arduino. Lesson 1 С новым годом
С новым годом Презентация Стихи Агнии Барто
Презентация Стихи Агнии Барто Игры с использованием нестандартного самодельного оборудования для детей
Игры с использованием нестандартного самодельного оборудования для детей Опасность сигарет
Опасность сигарет Презентация по теме Азбука профессий
Презентация по теме Азбука профессий Праздник Казанской иконы Божией Матери
Праздник Казанской иконы Божией Матери Назови одним словом
Назови одним словом Прогрессивные и офисные очковые линзы
Прогрессивные и офисные очковые линзы