Содержание
- 2. Э А=Е Н=Л , О=И ,,, Я Ё=Е
- 3. Электролит
- 4. Цель урока Изучить процесс электролитической диссоциации, объяснить причины электролитической диссоциации.
- 5. Что такое электрический ток? Как называются вещества, которые проводят электрический ток? Приведите примеры. Почему металлы проводят
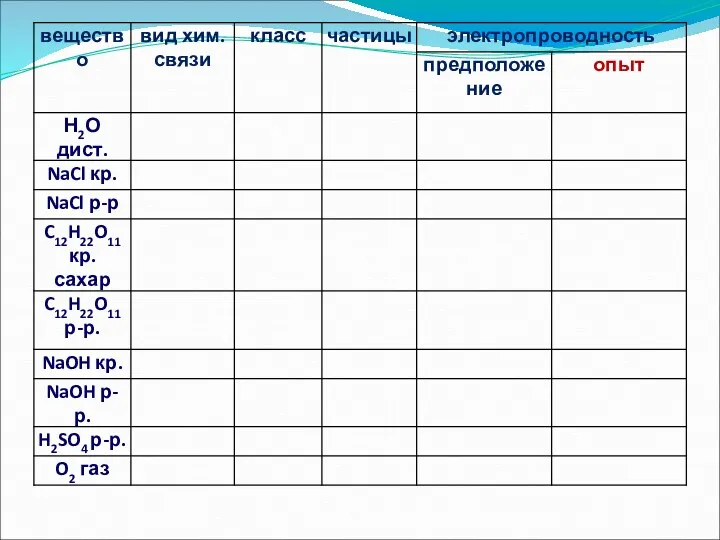
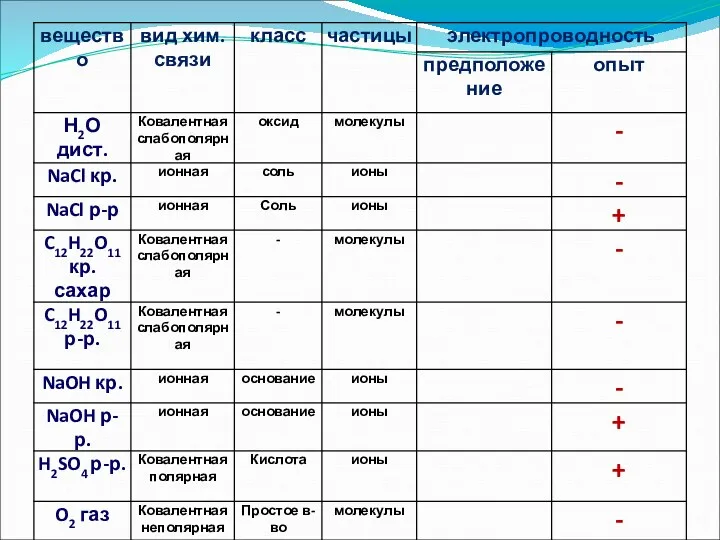
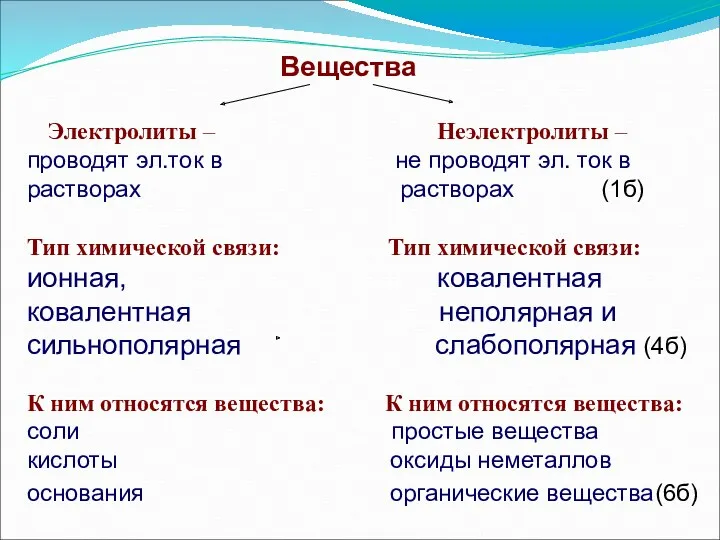
- 8. Вещества Электролиты – Неэлектролиты – проводят эл.ток в не проводят эл. ток в растворах растворах (1б)
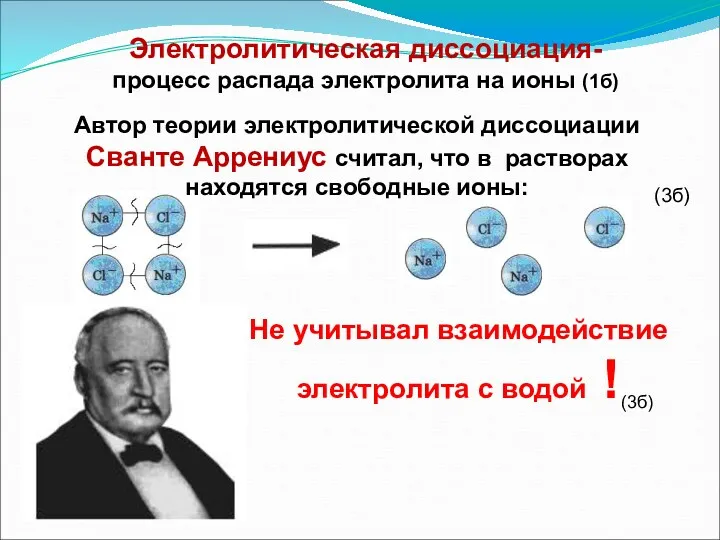
- 9. Автор теории электролитической диссоциации Сванте Аррениус считал, что в растворах находятся свободные ионы: Электролитическая диссоциация- процесс
- 10. Причину диссоциации объяснили И.А. Каблуков, В.А. Кистяковский ─ при растворении электролита происходит химическое взаимодействие растворенного вещества
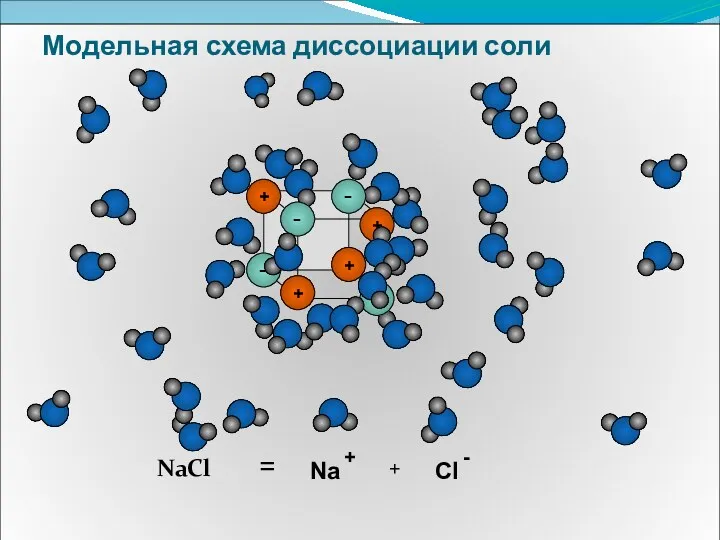
- 11. Модельная схема диссоциации соли NaCl = + Na +
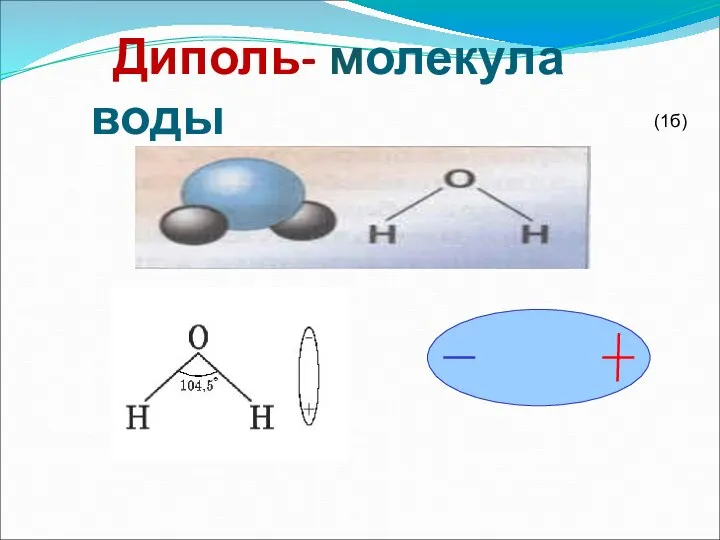
- 12. Диполь- молекула воды (1б)
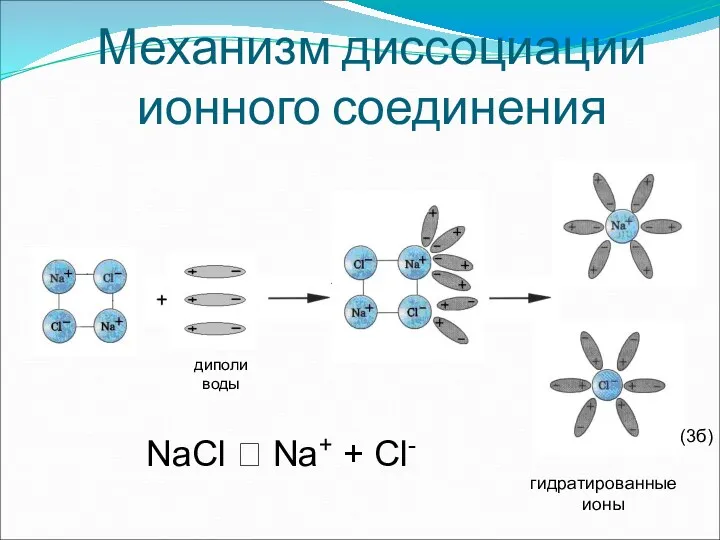
- 13. Механизм диссоциации ионного соединения NaCl ⮀ Na+ + Cl- гидратированные ионы диполи воды (3б)
- 14. Последовательность процессов, происходящих при диссоциации веществ с ионной связью: 1)ориентация молекул; 2)гидратация(взаимодействие); 3)диссоциация(распад) кристалла
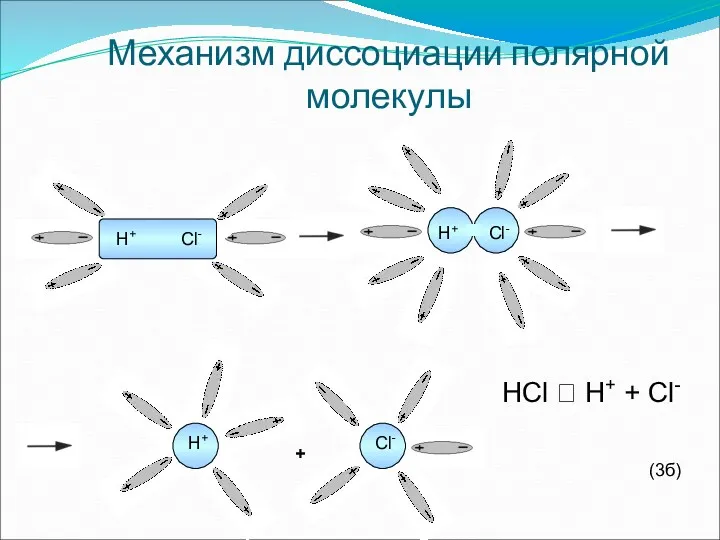
- 15. Механизм диссоциации полярной молекулы H+ Cl- H+ Cl- H+ Cl- + HCl ⮀ H+ + Cl-
- 16. Последовательность процессов, происходящих при диссоциации веществ с ковалентной полярной связью: 1)ориентация молекул; 2)гидратация(взаимодействие) молекул; 3)ионизация молекул(превращение
- 17. Степень диссоциации (α) (1б)
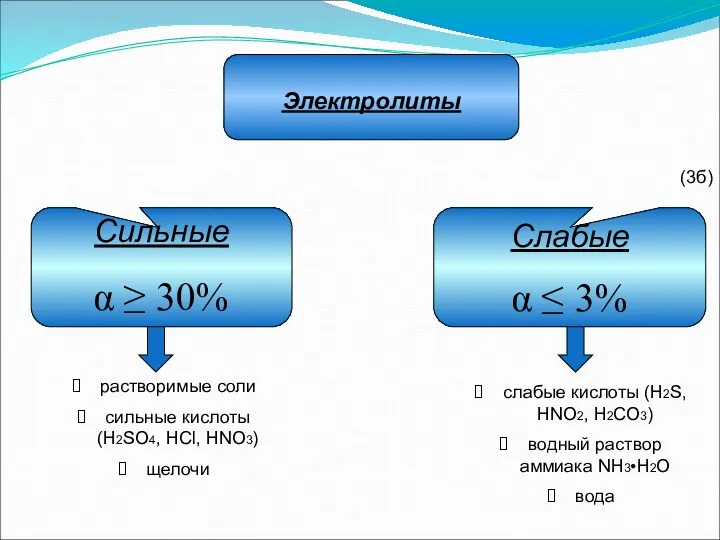
- 18. Сильные α ≥ 30% Слабые α ≤ 3% Электролиты растворимые соли сильные кислоты (H2SO4, HCl, HNO3)
- 21. Установите связь между электролитической диссоциацией и проблемами эксплуатации автомобиля Гололёд - Реагент - Коррозия
- 22. Объясните процесс приготовления пищи с точки зрения электролитической диссоциации
- 23. Задание для группы №1: Впишите недостающие слова: Все вещества по их способности проводить электрический ток в
- 24. Задание для группы №2;3: (2б за каждый правильный) всего12б Покажите выигрышный путь, состоящий из названий веществ
- 25. Задание для группы №4: Соотнесите: 1. (2б за каждый правильный) всего10б А) Электролиты 1) Кислоты Б)
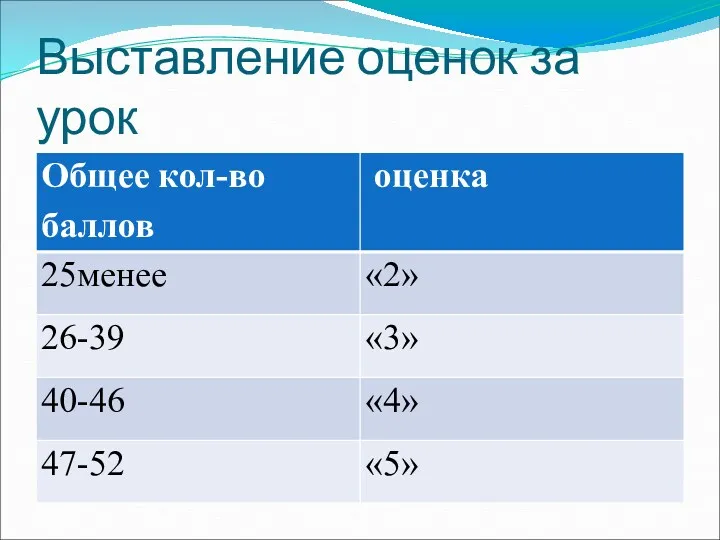
- 26. Выставление оценок за урок
- 27. РЕФЛЕКСИЯ Сегодня я узнал….. Было интересно…… Теперь я могу……… Я приобрел…… Я научился………
- 28. Домашнее задание: Читать Стр.193-197 до слов « В растворах электролитов..» упр.1,5 - «3»; упр.1,5,4 - «4»;
- 30. Скачать презентацию















 Управление социальными системами. Организационно-хозяйственный механизм. (Раздел 2)
Управление социальными системами. Организационно-хозяйственный механизм. (Раздел 2) Афферентті иннервацияға әсер ететін дәрілер
Афферентті иннервацияға әсер ететін дәрілер Обогащение познавательной сферы воспитанников в активных видах деятельности
Обогащение познавательной сферы воспитанников в активных видах деятельности Вычитание вида 52-24
Вычитание вида 52-24 Мы - Будущее
Мы - Будущее Комплекс упражнений для разминки баскетболиста
Комплекс упражнений для разминки баскетболиста LEGO Mindstorms EV3
LEGO Mindstorms EV3 Полезный задачник по химии. 9 класс
Полезный задачник по химии. 9 класс Технологические основы буровых работ
Технологические основы буровых работ Формирование толерантности дошкольников
Формирование толерантности дошкольников X19-11-10A SDJ-85/200 双螺杆双阶机组
X19-11-10A SDJ-85/200 双螺杆双阶机组 Измерение напряжений и уровней сигналов
Измерение напряжений и уровней сигналов Наука и научное исследование. Методология научных исследований
Наука и научное исследование. Методология научных исследований Правовая система. Семья
Правовая система. Семья Как составить исковое заявление в суд, при несогласии с отказом в признании лица инвалидом, при первичном освидетельствовании
Как составить исковое заявление в суд, при несогласии с отказом в признании лица инвалидом, при первичном освидетельствовании Grand Import офіційний ексклюзивний імпортер NAUJOJI RINGUVA в Україні
Grand Import офіційний ексклюзивний імпортер NAUJOJI RINGUVA в Україні Культура епохи Відродження
Культура епохи Відродження American history
American history Понятие, признаки,структура нормы права
Понятие, признаки,структура нормы права Англия. Соединенное Королевство Великобритании и Северной Ирландии
Англия. Соединенное Королевство Великобритании и Северной Ирландии Отношение к природе в буддизме
Отношение к природе в буддизме Оценка и усовершенствование клинических рекомендаций для национального распространения
Оценка и усовершенствование клинических рекомендаций для национального распространения Сахарный диабет (СД). Эпидемиология сахарного диабета
Сахарный диабет (СД). Эпидемиология сахарного диабета Колебания и волны. Геометрическая и волновая оптика
Колебания и волны. Геометрическая и волновая оптика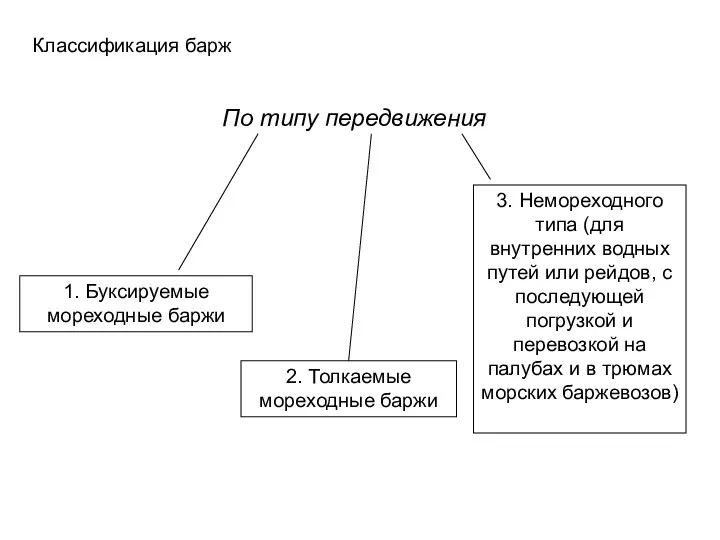 Классификация барж по типу передвижения
Классификация барж по типу передвижения Смешарики война 13 эпизод
Смешарики война 13 эпизод Радиобиология человека
Радиобиология человека Теория брендинга. Модели бренд-образования
Теория брендинга. Модели бренд-образования