Регулирование свойств тампонажных материалов для цементирования скважин в осложненных условиях презентация
Содержание
- 2. Литература Агзамов Ф.А., Измухамбетов Б.С.,Токунова Э.Ф. Химия тампонажных и буровых растворов. С-ПБ, Недра, 2011, 268 с
- 3. Лекция 1 Требования к тампонажным материалам. Портландцемент. Физико-химические основы твердение портландцемента. Физико-химические основы регулирования процесса твердения
- 4. ПОРТЛАНДЦЕМЕНТ Портландцемент = (Клинкер + Добавка + Гипс) → Помол → Затаривание Клинкер = (Известняк +
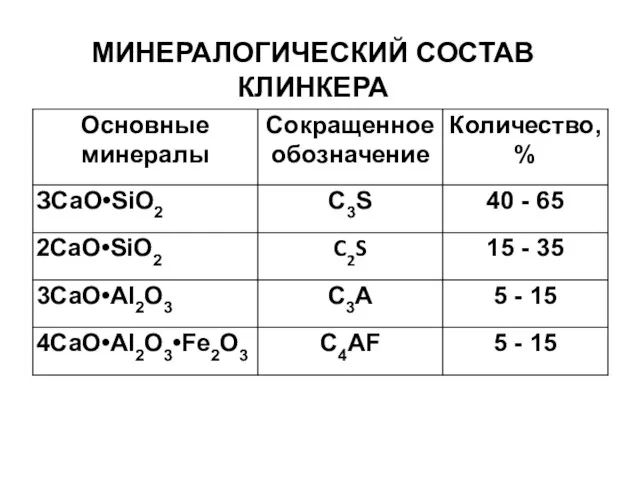
- 5. МИНЕРАЛОГИЧЕСКИЙ СОСТАВ КЛИНКЕРА
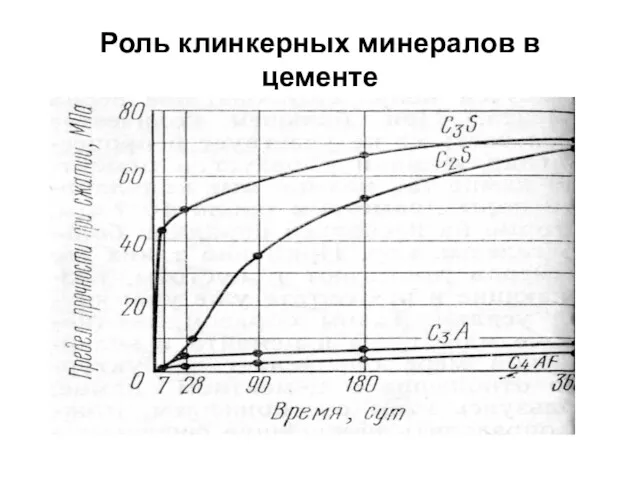
- 6. Роль клинкерных минералов в цементе
- 7. Гидратация и твердение цементов
- 8. РЕАКЦИИ ГИДРАТАЦИИ ДЛЯ МИНЕРАЛОВ ЦЕМЕНТА 2(ЗСаО•SiO2) + 6Н2О → ЗСаО•2SiO2•3H2О + 3Са(ОН)2 + 502 Дж/г 2(2CaO•SiО2)+
- 9. Схема гидратации цемента
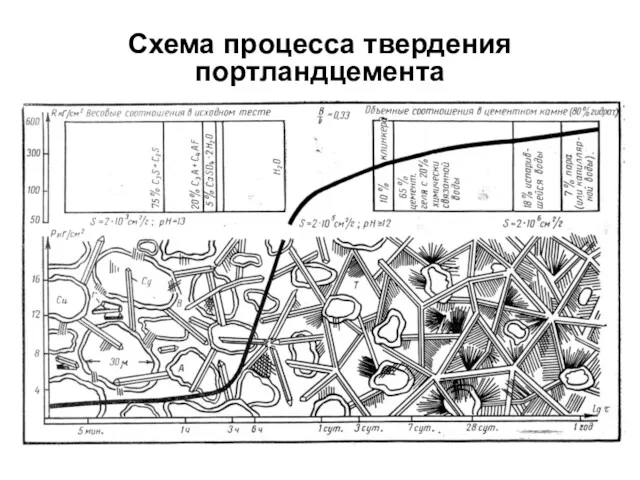
- 10. Схема процесса твердения портландцемента
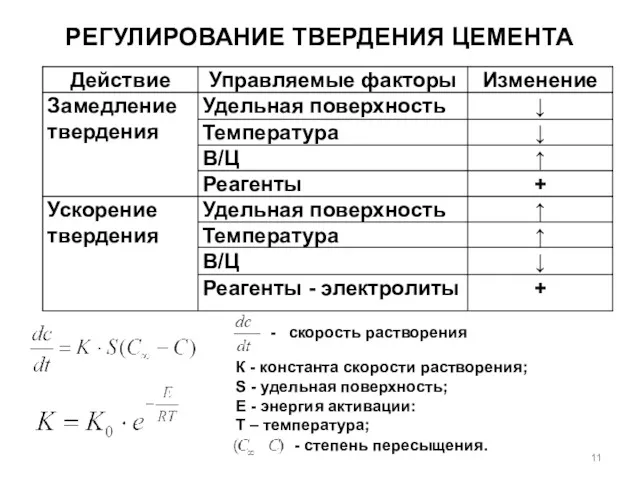
- 11. РЕГУЛИРОВАНИЕ ТВЕРДЕНИЯ ЦЕМЕНТА - скорость растворения К - константа скорости растворения; S - удельная поверхность; Е
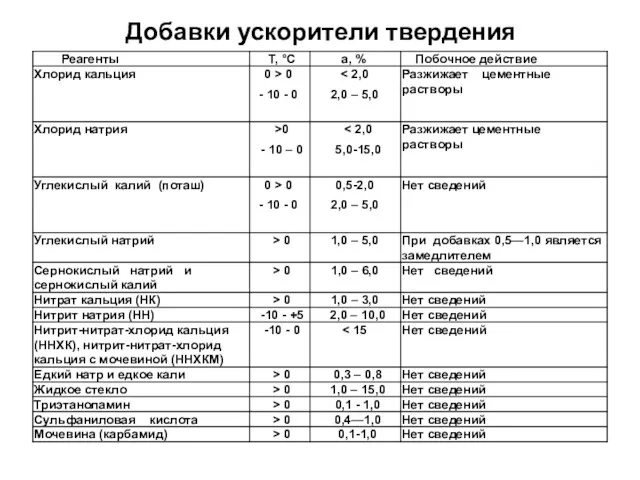
- 12. Добавки ускорители твердения
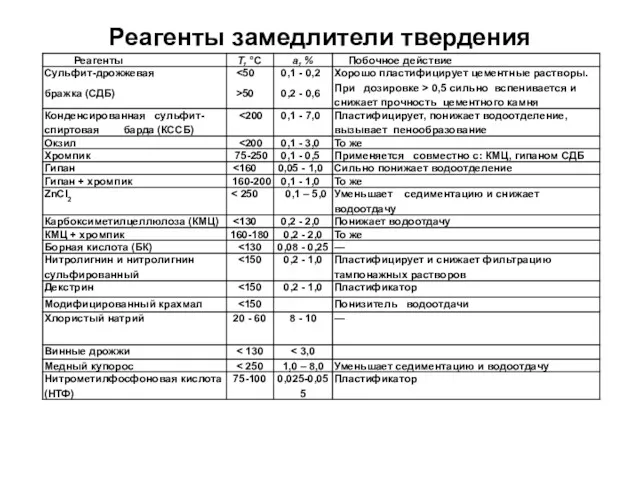
- 13. Реагенты замедлители твердения
- 14. Лекция 2 Свойства цемента, цементного раствора, приборы для контроля свойств Физико-химические основы и средства регулирования свойствами
- 15. Свойства цемента Гранулометрический состав; Удельная поверхность; Плотность; Насыпная плотность.
- 16. Свойства цементного раствора Водоцементное отношение (В/Ц) Растекаемость Прокачиваемость Сроки схватывания Реологические свойства Плотность Водоотдача Водоотделение
- 17. Контроль свойств цементного раствора Конус АзНИИ для определения растекаемости Игла Вика для определения сроков схватывания Атмосферный
- 18. Вискозиметр для определения реологических свойств тампонажных растворов
- 19. РЕГУЛИРОВАНИЕ ПЛОТНОСТИ ТАМПОНАЖНЫХ РАСТВОРОВ Рычажные весы для определения плотности
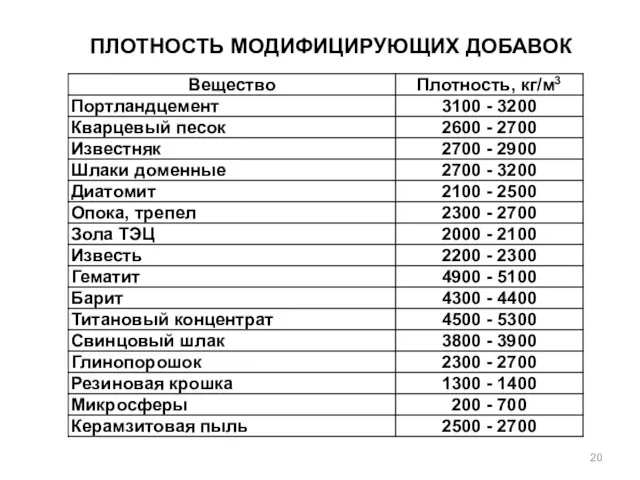
- 20. ПЛОТНОСТЬ МОДИФИЦИРУЮЩИХ ДОБАВОК
- 21. СНИЖЕНИЕ ВОДООТДАЧИ ТАМПОНАЖНЫХ РАСТВОРОВ
- 22. Лекция 3 Свойства цементного камня и методы управления ими. Стандарт на тампонажные цементы
- 23. Свойства цементного камня Пористость Предел прочности Проницаемость Объемные изменения Удароустойчивость Коррозионная стойкость.
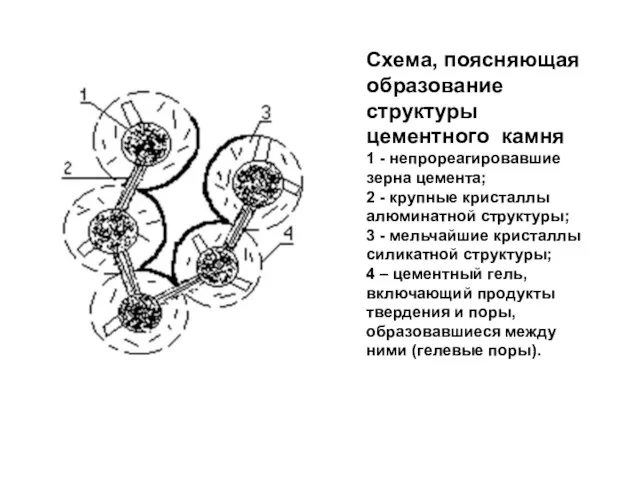
- 24. Схема, поясняющая образование структуры цементного камня 1 - непрореагировавшие зерна цемента; 2 - крупные кристаллы алюминатной
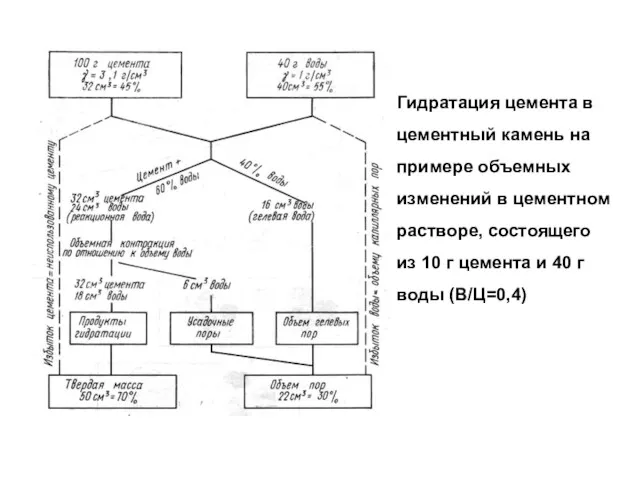
- 25. Гидратация цемента в цементный камень на примере объемных изменений в цементном растворе, состоящего из 10 г
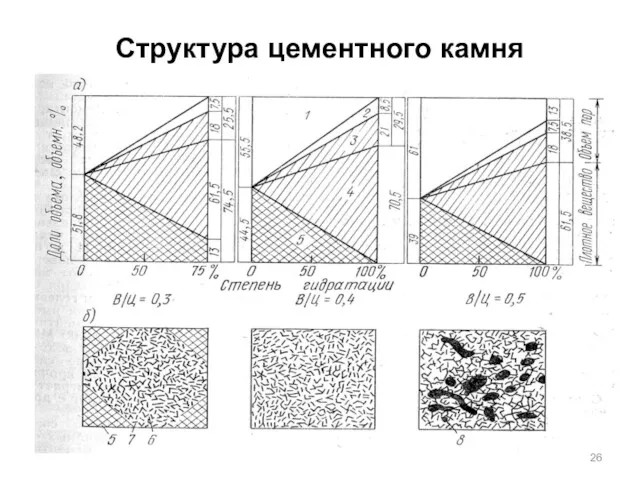
- 26. Структура цементного камня
- 27. Пресс для определения предела прочности цементного камня Формы для получения образцов-балочек и балочка для определения предела
- 28. Требования к кинетике расширения цементов основная часть расширения должна происходить после продавки цементного раствора в затрубное
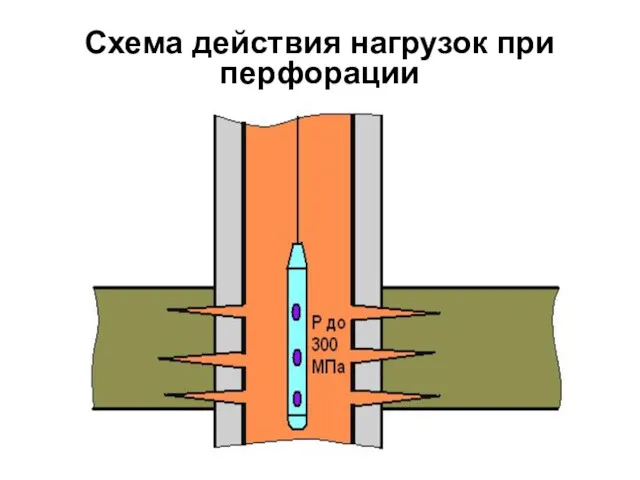
- 29. Схема действия нагрузок при перфорации
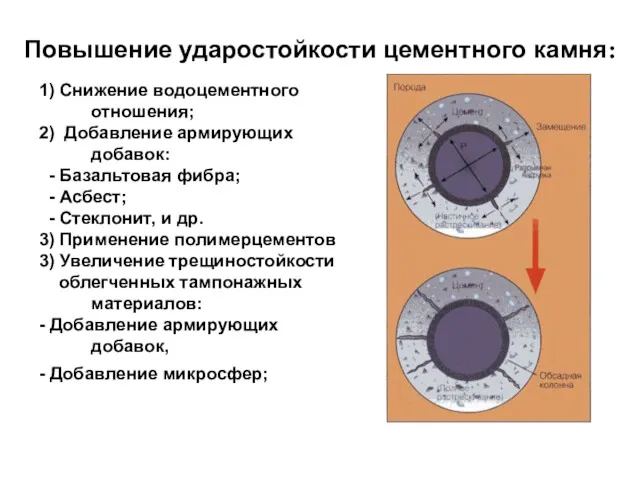
- 30. Повышение ударостойкости цементного камня: 1) Снижение водоцементного отношения; 2) Добавление армирующих добавок: - Базальтовая фибра; -
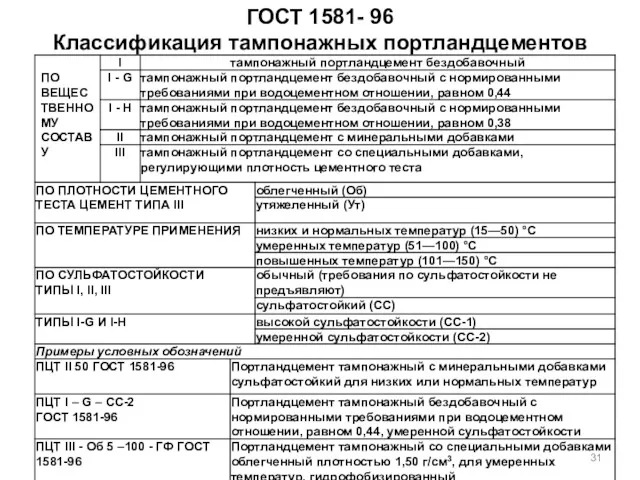
- 31. ГОСТ 1581- 96 Классификация тампонажных портландцементов
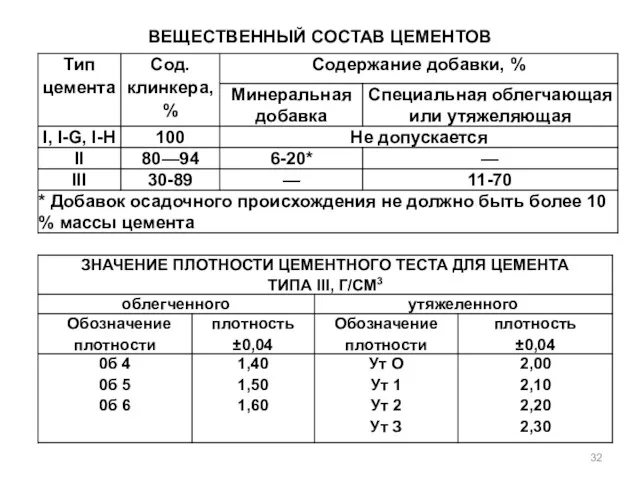
- 32. ВЕЩЕСТВЕННЫЙ СОСТАВ ЦЕМЕНТОВ
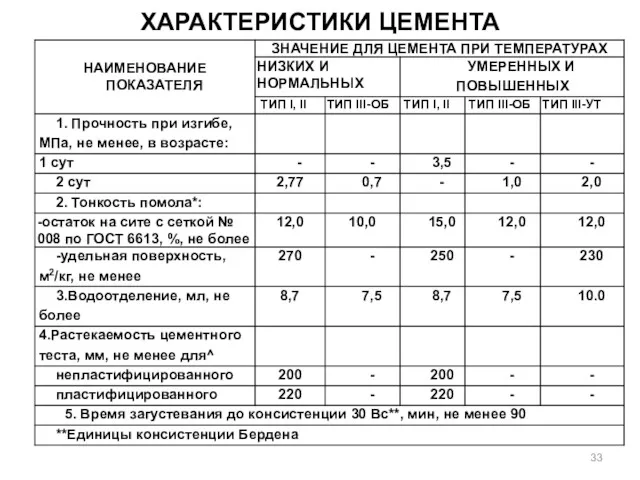
- 33. ХАРАКТЕРИСТИКИ ЦЕМЕНТА
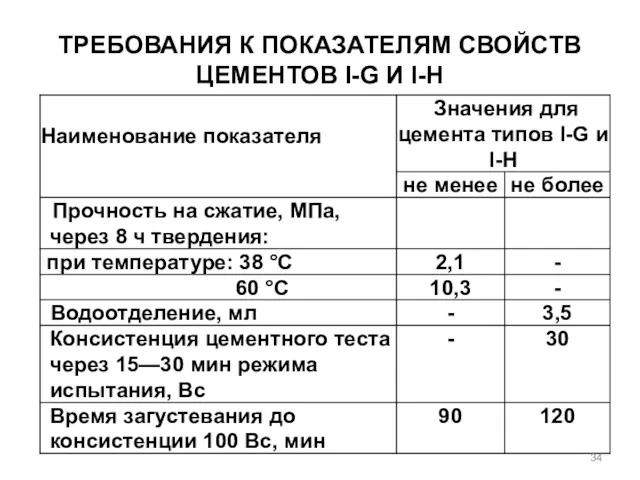
- 34. ТРЕБОВАНИЯ К ПОКАЗАТЕЛЯМ СВОЙСТВ ЦЕМЕНТОВ I-G И I-H
- 35. Лекция 4 Управление долговечностью тампонажных материалов.
- 36. Состав пластовых флюидов
- 37. Коррозия цементного камня. Определения Химические и физико-химические процессы, при которых цементный камень разрушается под действием окружающей
- 38. Классификация видов коррозии цементного камня 1. Физическая коррозия: Разрушение цементного камня при действии знакопеременных температур; Разрушение
- 39. Физическая коррозия цементного камня Разрушение цементного камня при действии знакопеременных температур Механизм; Факторы, определяющие процесс; Пути
- 40. Механизм При действии отрицательных температур вода, находящаяся в крупных порах, способна замерзать и переходить в твердое
- 41. Факторы, определяющие процесс На долговечность камня при действии знакопеременных температур влияют: степень гидратации цемента; водоцементное отношение;
- 42. Коррозия выщелачивания, примеры
- 43. Механизм Фазовый состав затвердевшего цементного камня представлен группой гидросиликатов кальция различной основности, гидроалюминатами и гидроферритами кальция,
- 44. Факторы, определяющие процесс Состав цемента; Пористость; Характер воздействия воды; Химический состав вод; Наличие негидратированного цемента
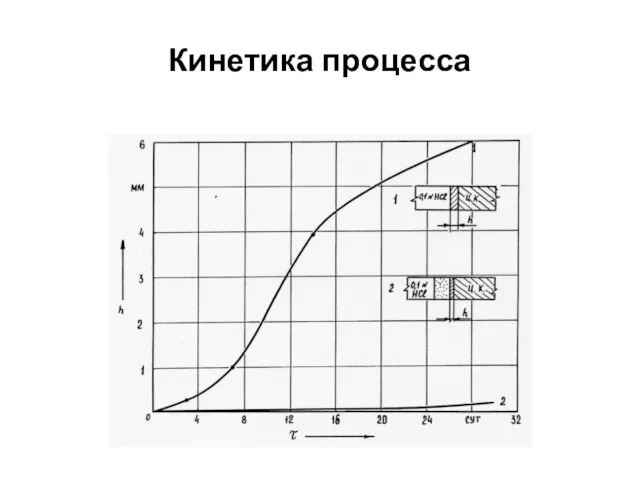
- 45. Кинетика процесса 1. Растворение и гидролиз продуктов твердения 2. Диффузный продуктов гидролиза в окружающую среду
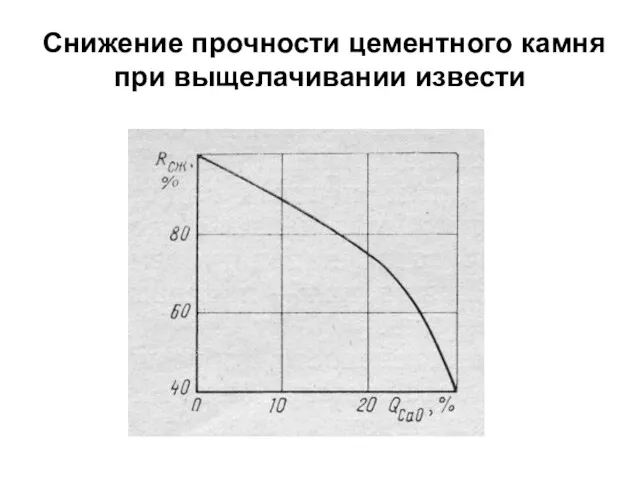
- 46. Снижение прочности цементного камня при выщелачивании извести
- 47. Кислотная коррозия цементного камня Химия процесса При контакте цементного камня с кислой средой происходит мгновенная нейтрализация
- 49. Кислотная коррозия цементного камня (пример)
- 50. Факторы, определяющие процесс Состав цемента; Пористость; Реакционная емкость; Добавки ингибиторы коррозии; Концентрация кислоты на границе с
- 51. Кинетика процесса
- 52. Сульфатная коррозия цементного камня Химия; Механизм; Управление; Принципы получения сульфатостойких цементов; Проблемы;
- 53. Сульфатная коррозия цементного камня (химия) Na2SO4 + Ca(OH)2 = CaSO4 + 2NaOH Когда концентрация CaSO4 превышает
- 54. Чаще всего сульфатная коррозия связывается с образованием гидросульфоалюмината кальция (эттрингита), образующегося за счет взаимодействия иона SО42-
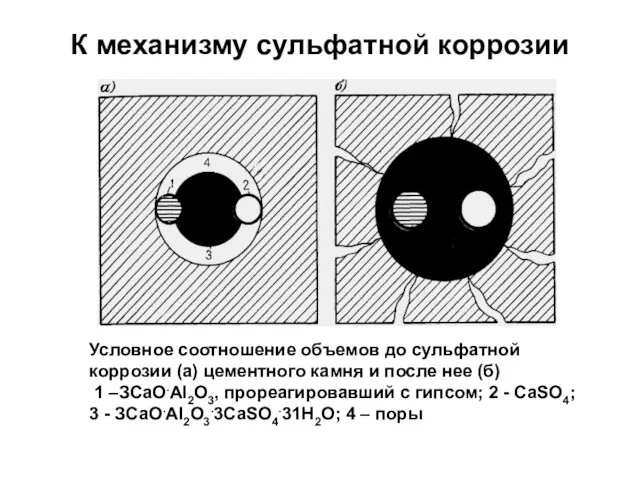
- 55. К механизму сульфатной коррозии Условное соотношение объемов до сульфатной коррозии (а) цементного камня и после нее
- 56. Необходимыми условия для протекания сульфатной коррозии наличие сульфат ионов, проникших внутрь цементного камня; наличие в составе
- 57. Анализ условий Ограничение скорости поступления ионов SО42- внутрь цементного камня. Уменьшение пористости камня за счет снижения
- 58. Анализ условий 2. Снижение содержания алюминий содержащих фаз в цементе. Используется на заводах при получении сульфатостойких
- 59. Анализ условий 3. Снижение pH цементного камня. Ввод кремнеземистых добавок в цемент для снижения основности продуктов
- 60. Магнезиальная коррозия цементного камня Химия процесса : MgSO4 + Са(ОН)2 = Mg (ОН)2 + CaSO4 MgCl2
- 61. Возможный механизм коррозии 1. Кислотный, поскольку одним продуктом реакции является хлорид кальция, который гидролизуясь, дает кислую
- 62. Возможный механизм коррозии 2. Осмотический. Выпадающий в осадок Mg (ОН)2 образует полупроницаемую перегородку на поверхности цементного
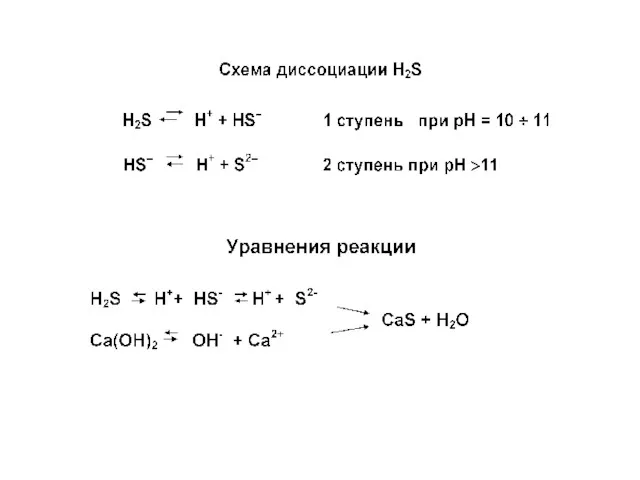
- 63. Сероводородная коррозия цементного камня Сероводород (H2S) является коррозионноактивным кислым газом, оказывающим интенсивное разрушающее действие не только
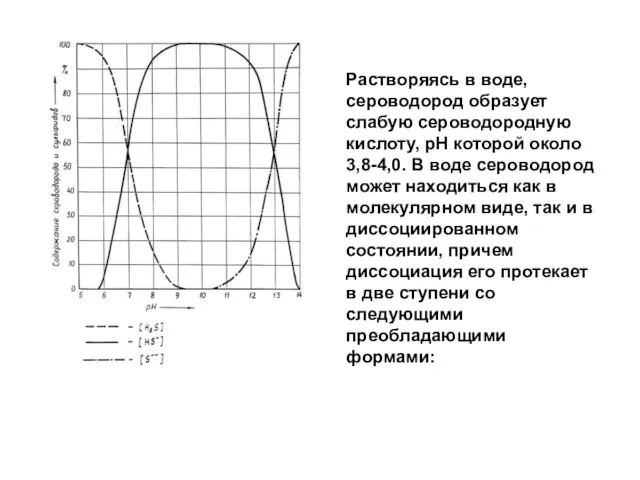
- 65. Растворяясь в воде, сероводород образует слабую сероводородную кислоту, рН которой около 3,8-4,0. В воде сероводород может
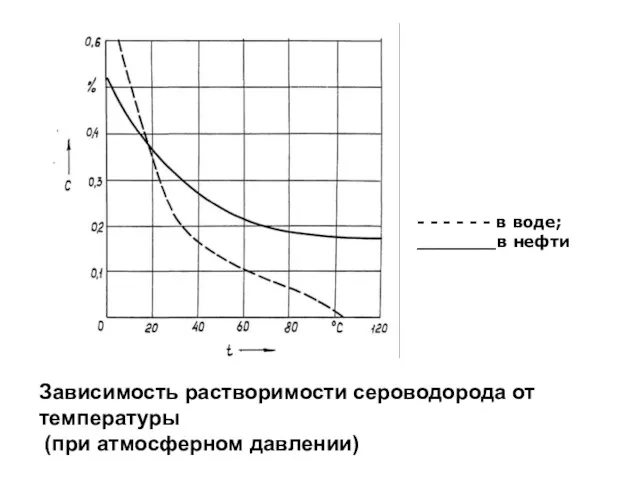
- 66. Зависимость растворимости сероводорода от температуры (при атмосферном давлении) - - - - - - в воде;
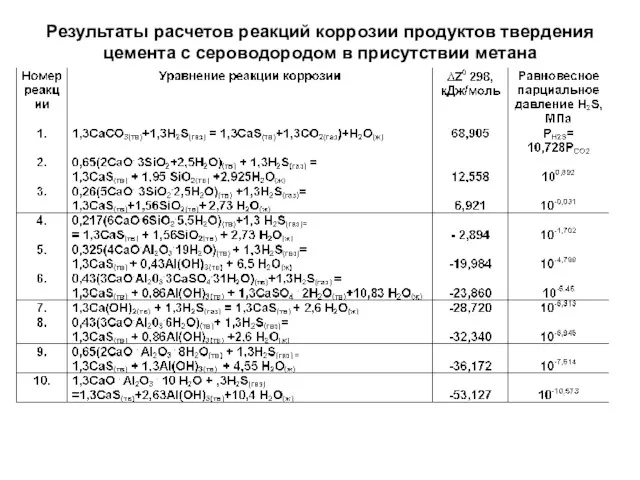
- 67. Результаты расчетов реакций коррозии продуктов твердения цемента с сероводородом в присутствии метана
- 69. Наиболее уязвимы к сероводороду высокоосновные гидросиликаты кальция, Са(ОН)2, гидроалюминаты кальция, соединения, содержащие оксиды железа. Наличие кислорода
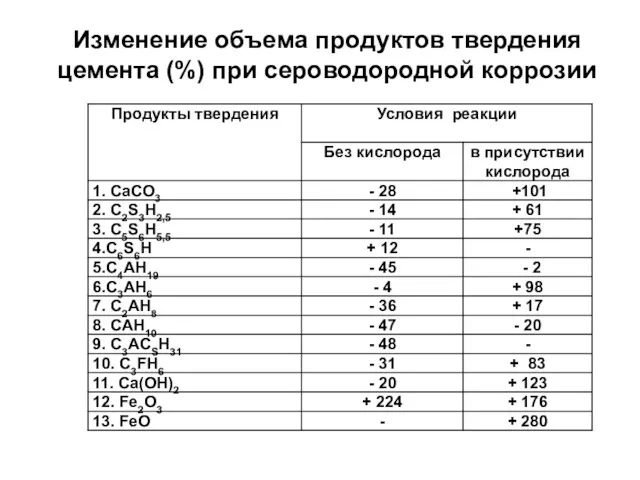
- 70. Изменение объема продуктов твердения цемента (%) при сероводородной коррозии
- 71. Коррозия цементного камня под действием газообразного сероводорода В условиях газовой сероводородной агрессии механизм поражения носит объемный
- 72. Коррозия камня из мономинералов в сероводороде С3S С3S C3A C4AF
- 73. Влияние углеводородов на процесс коррозии H2S H2S + конденсат
- 74. Примеры поражения цементного камня сероводородом Астрахань Оренбург
- 75. Микрофотографии образцов цементного камня до и после серовододной коррзии
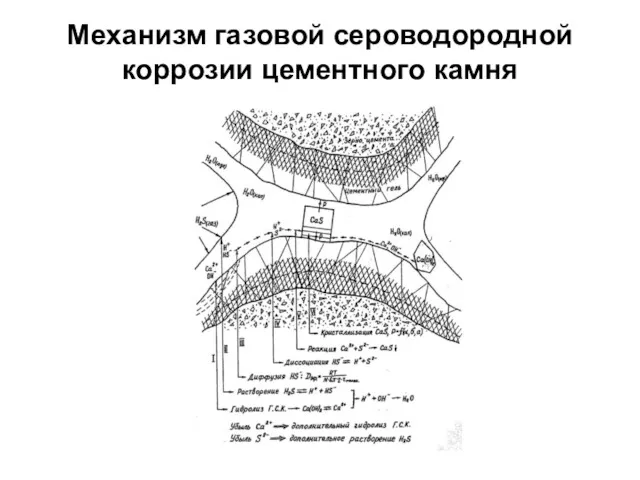
- 76. Механизм газовой сероводородной коррозии цементного камня
- 77. Даже небольшое количество продуктов коррозии, накопленное в порах или перегибах пор, вызывает резкое падение прочности и
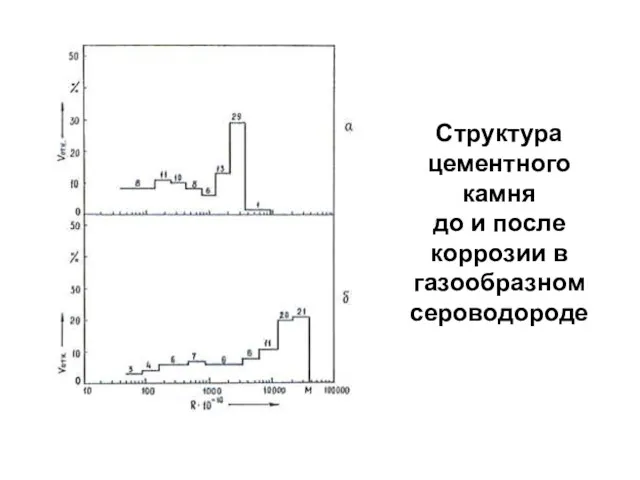
- 78. Структура цементного камня до и после коррозии в газообразном сероводороде
- 79. Тампонажные материалы, стойкие к газообразному сероводороду Шлаковые цементы; Песчанистые цементы; Белитокремнеземистые цементы; Глиноземистый цемент; Сульфоалюминатный цемент.
- 80. Коррозия цементного камня под действием растворенного сероводорода В зависимости от состава продуктов твердения цементный камень может
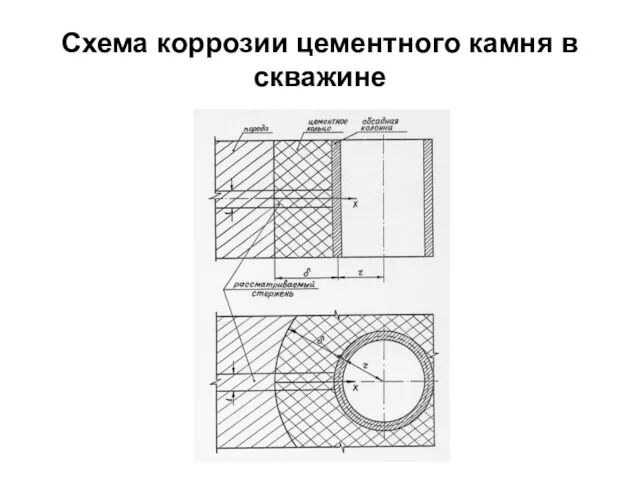
- 81. Схема коррозии цементного камня в скважине
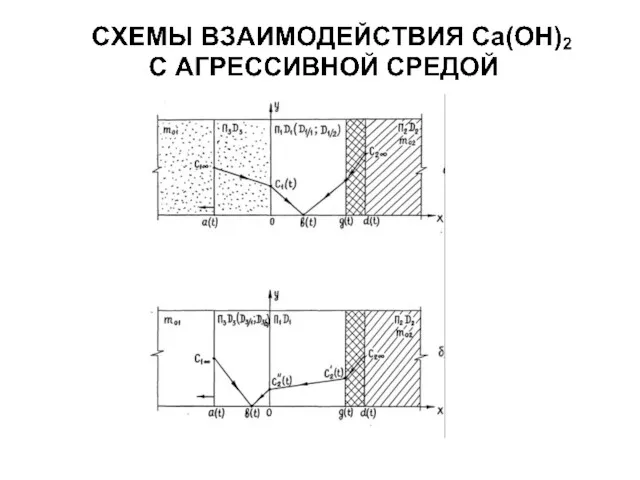
- 83. С точки зрения долговечности крепи более предпочтительным является встреча потока агрессора и гидроксида кальция за пределами
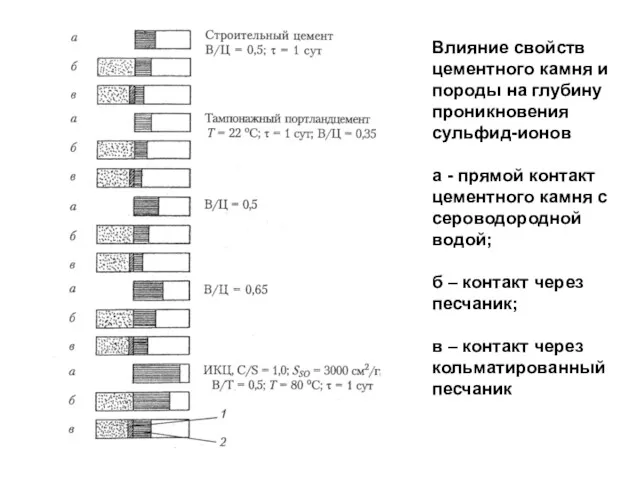
- 84. Влияние свойств цементного камня и породы на глубину проникновения сульфид-ионов а - прямой контакт цементного камня
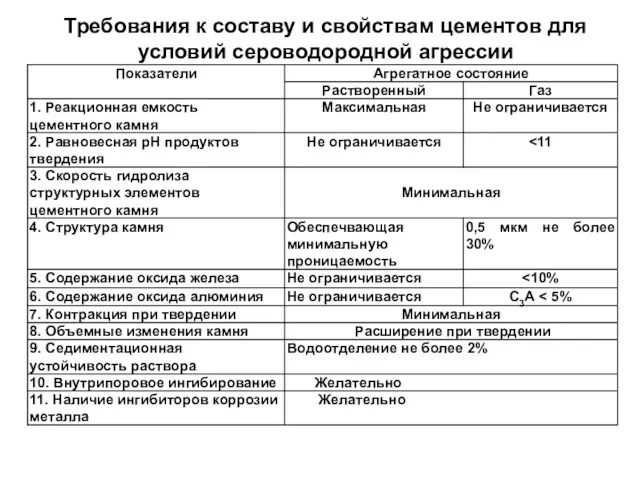
- 85. Требования к составу и свойствам цементов для условий сероводородной агрессии
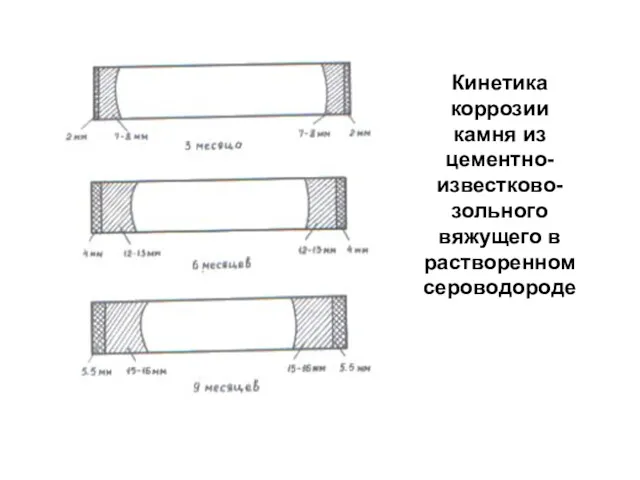
- 86. Кинетика коррозии камня из цементно-известково-зольного вяжущего в растворенном сероводороде
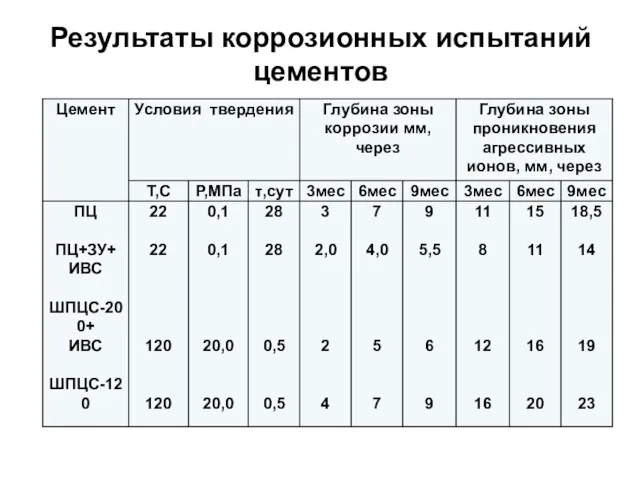
- 87. Результаты коррозионных испытаний цементов
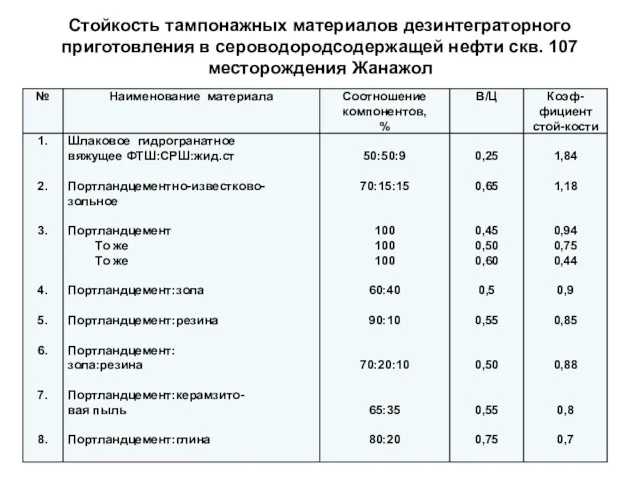
- 88. Стойкость тампонажных материалов дезинтеграторного приготовления в сероводородсодержащей нефти скв. 107 месторождения Жанажол
- 89. Пути повышения долговечности крепи скважин в агрессивных средах Материалы Регулируется реакционная емкость концентрация цементного камня; Добавки
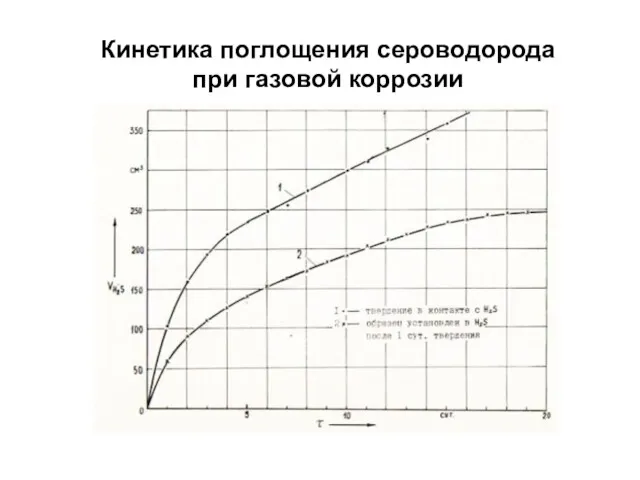
- 90. Кинетика поглощения сероводорода при газовой коррозии
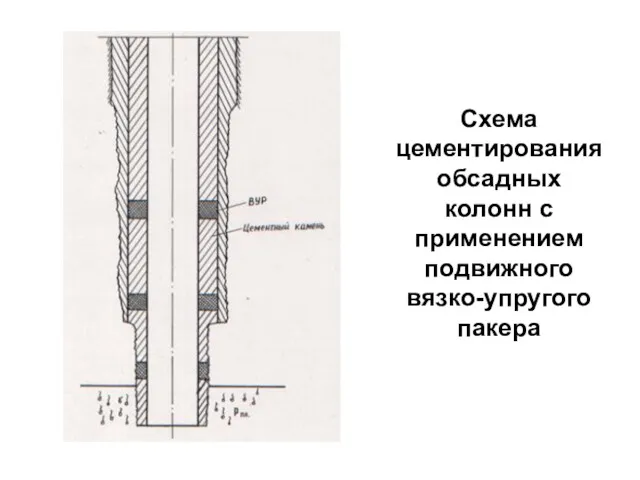
- 91. Схема цементирования обсадных колонн с применением подвижного вязко-упругого пакера
- 92. Лекция 6 Управление термостойкостью тампонажных растворов.
- 93. Термическая коррозия цементного камня Термическая коррозия обусловлена термодинамической неустойчивостью продуктов твердения их перекристаллизацией и переходом в
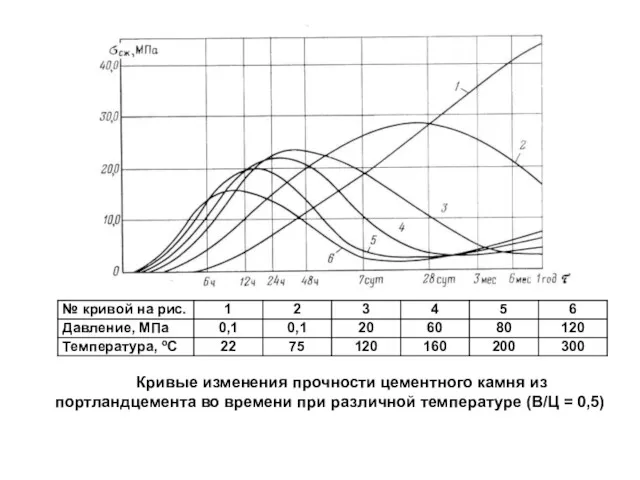
- 94. Кривые изменения прочности цементного камня из портландцемента во времени при различной температуре (В/Ц = 0,5)
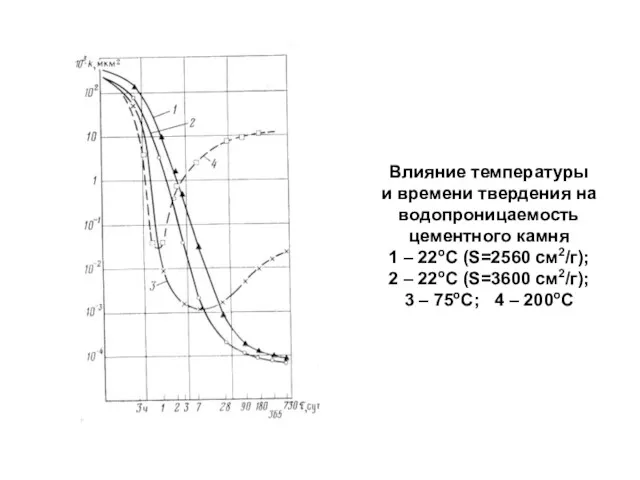
- 95. Влияние температуры и времени твердения на водопроницаемость цементного камня 1 – 22оС (S=2560 см2/г); 2 –
- 96. Внутрифазовая перекристаллизация, заключается в том, что образовавшие при твердении цемента мельчайшие продукты твердения начинают укрупняться. Межфазовая
- 97. Наибольшей склонностью межфазовых перекристаллизаций обладают высокоосновные продукты твердения, в которых CaO/ SiO2 = C/S > 1,2.
- 98. Наиболее эффективным способом предупреждения термической коррозии является уменьшение С/S в самом цементе. На практике этого можно
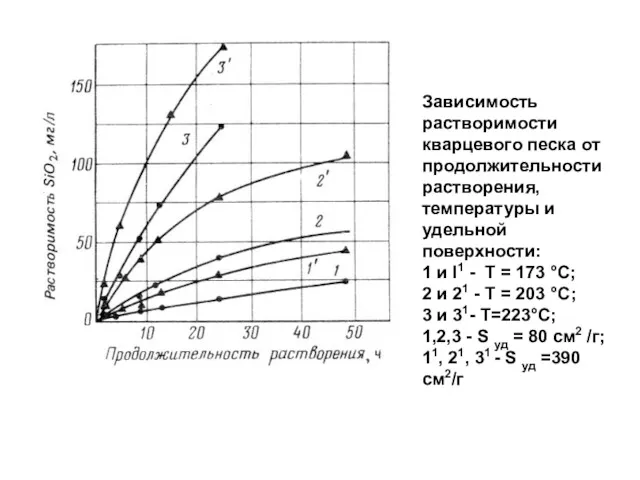
- 99. Зависимость растворимости кварцевого песка от продолжительности растворения, температуры и удельной поверхности: 1 и I1 - Т
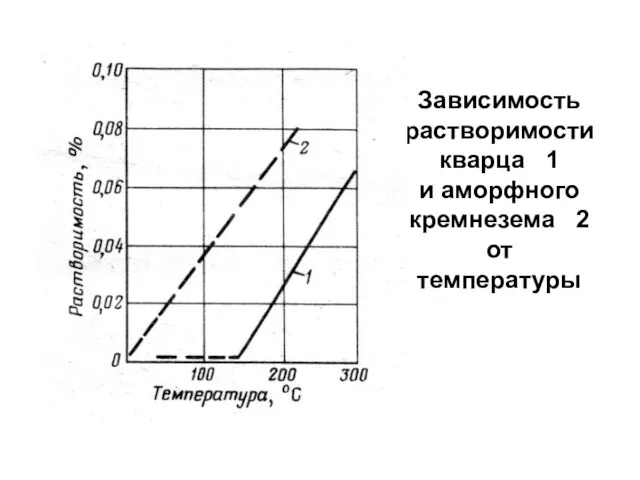
- 100. Зависимость растворимости кварца 1 и аморфного кремнезема 2 от температуры
- 101. Принципы получения высокотемпературных цементов 1. Понижение основности продуктов твердения; 2. Управление кинетикой фазообразования. Цель исключение образования
- 102. Термостойкие цементы Портландцементно-песчаные тампонажные смеси; Белито-кремнеземистые цементы; Известково кремнеземистый цемент; Цементы на основе доменных шлаков
- 104. Скачать презентацию






























































 Технология сотрудничества в начальных классах
Технология сотрудничества в начальных классах Малое предпринимательство
Малое предпринимательство Презентация к конкурсной семейной программе Как домовёнок Кузя семью искал
Презентация к конкурсной семейной программе Как домовёнок Кузя семью искал Длина окружности и площадь круга
Длина окружности и площадь круга Презентация по проблеме оценки качества труда учителя
Презентация по проблеме оценки качества труда учителя Центр развития и восстановления навыков вождения
Центр развития и восстановления навыков вождения презентация опыта работы
презентация опыта работы Презентация Социальный проект - Чистая вода - здоровье города.
Презентация Социальный проект - Чистая вода - здоровье города. Операционные системы
Операционные системы Методы добычи нефти и газа. Способы эксплуатации скважин
Методы добычи нефти и газа. Способы эксплуатации скважин Түрік лирасы
Түрік лирасы САПР Autocad 2015. Работа с текстом. Шаблоны оформления
САПР Autocad 2015. Работа с текстом. Шаблоны оформления Динамика и прогноз рождаемости, общей смертности в Алтайском крае
Динамика и прогноз рождаемости, общей смертности в Алтайском крае Инвестиционное предложение. Частное швейное предприятие
Инвестиционное предложение. Частное швейное предприятие Выбросить нельзя оставить...
Выбросить нельзя оставить... Методы принятия решений в группе
Методы принятия решений в группе Definition of Litotes
Definition of Litotes Гипподамова система: плюсы и минусы
Гипподамова система: плюсы и минусы Понятие организации, ее сущность и признаки
Понятие организации, ее сущность и признаки Prepositions of place
Prepositions of place Открытое занятие Интерфейс программы. Создание простейших программ
Открытое занятие Интерфейс программы. Создание простейших программ Past continuous tense
Past continuous tense Система охлаждения. Общие положения. Работа жидкостной системы охлаждения нефорсированного двигателя
Система охлаждения. Общие положения. Работа жидкостной системы охлаждения нефорсированного двигателя Доктора бывают разные
Доктора бывают разные Иммунологические аспекты климактерического синдрома. Иммунология старения
Иммунологические аспекты климактерического синдрома. Иммунология старения Принятие христианства на Руси
Принятие христианства на Руси Малая архитектурная форма в городской среде (остановка общественного транспорта)
Малая архитектурная форма в городской среде (остановка общественного транспорта) Требования к презентации. Правила проведения практических занятий (показ и обсуждение презентаций)
Требования к презентации. Правила проведения практических занятий (показ и обсуждение презентаций)