Содержание
- 2. История Ртуть – 1 из 7 металлов древности. Она известна более 1500 лет до н.э. в
- 3. Народам Индии и Китая самородная ртуть была известна за 2000 лет до н. э. Ими же,
- 4. Распространение Ртути в природе Ртуть принадлежит к числу весьма редких элементов. Приблизительно в таких количествах она
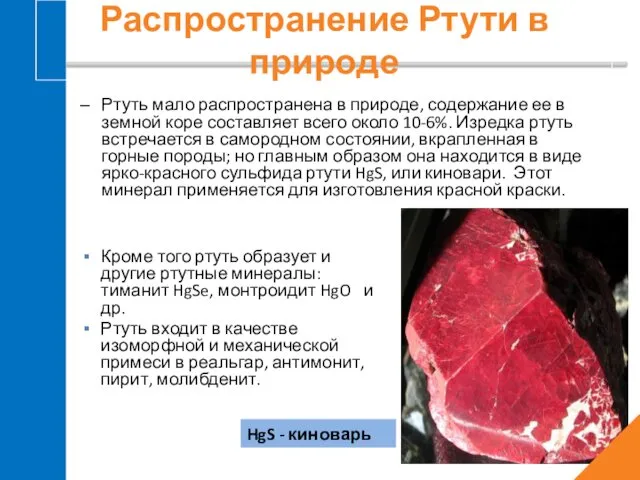
- 5. Ртуть мало распространена в природе, содержание ее в земной коре составляет всего около 10-6%. Изредка ртуть
- 6. Самородная ртуть Hg Ртуть на киноварь-кварцевом агрегате. Levigliani, Тоскана, Италия Ртуть на барите. Шахта Анна, Зигерланд,
- 7. Каломель (Hg2)2+(Cl,Br)2 Терлингуа, Техас San-Onofre. Мексика Авала, Сербия
- 8. Словенский город Идрия — крупнейший в Европе центр добычи ртути с XV века
- 9. Химический элемент Ртуть (Hg, от лат. Hydrargyrum) — элемент шестого периода периодической системы химических элементов Д.
- 10. Физические свойства Простое вещество ртуть — переходный металл, при комнатной температуре представляющий собой тяжёлую серебристо-белую жидкость,
- 11. Физические свойства Температура плавления составляет 234,32 K (-38,83 °C), кипит при 629,88 K (356,73 °C). Обладает
- 12. Химические свойства Для ртути характерны две степени окисления: +1 и +2. В степени окисления +1 ртуть
- 13. Химические свойства Ртуть — малоактивный металл. Она не растворяется в растворах кислот, не обладающих окислительными свойствами,
- 14. Химические свойства Также с трудом растворяется в серной кислоте при нагревании, с образованием сульфата ртути: При
- 15. Химические свойства При нагревании до 300 °C ртуть вступает в реакцию с кислородом: При этом образуется
- 16. Химические свойства При нагревании ртути с серой образуется сульфид ртути(II): Сульфид ртути Реакция демеркуризации
- 17. Химические свойства Ртуть также реагирует с галогенами (причём на холоде — медленно). Ртуть можно окислить также
- 18. Получение Ртуть получают обжигом киновари (сульфида ртути(II)) или металлотермическим методом: Пары ртути конденсируют и собирают. Этот
- 19. Ртуть широко применяется при изготовлении научных приборов:(барометры, термометры, манометры, вакуумные насосы и др.), в ртутных лампах,
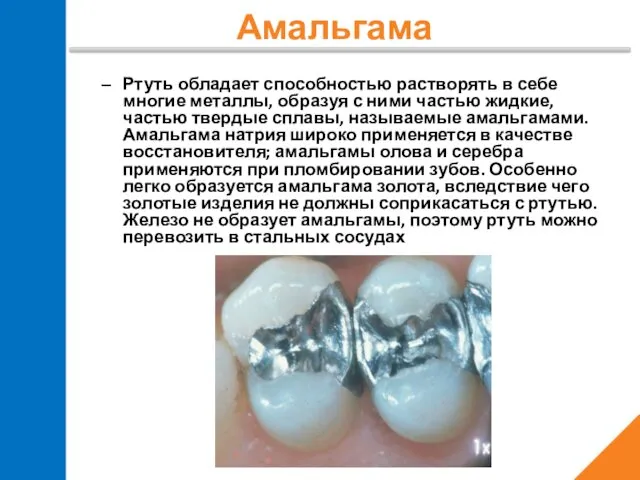
- 20. Ртуть обладает способностью растворять в себе многие металлы, образуя с ними частью жидкие, частью твердые сплавы,
- 21. Соединения ртути Оксид ртути(II) — HgO Это твёрдое непрочное при нормальных условиях вещество красного или оранжевого
- 22. Соединения ртути Фульминат ртути(II) Hg(ONC)2 («гремучая ртуть») издавна применяется в качестве инициирующего ВВ (Детонаторы). «Гремучую ртуть»
- 23. Соединения ртути Сулема - хлорид ртути HgCl2 был первым веществом на основе Hg, которое начали использовать
- 24. Соединения ртути Ка́ломель, хлористая ртуть, хлорид одновалентной ртути Hg2Cl2 - бесцветные, мало растворимые в воде кристаллы.
- 25. Соединения ртути Циани́д рту́ти(II) Hg(CN)2 — неорганическое соединение, ртутная соль синильной кислоты. Содержит 79% ртути. Белое
- 26. Основной опасность представляют пары металлической ртути, выделение которых с открытых поверхностей возрастает при повышении температуры воздуха.
- 27. Одно из тяжелейших загрязнений ртутью в истории случилось в японском городе Минамата в 1956 году, что
- 30. Скачать презентацию

























 Гражданское общество и правовое государство
Гражданское общество и правовое государство Интеграция логистической деятельности
Интеграция логистической деятельности Культура средневековой Европы
Культура средневековой Европы Особенности технологии и технические средства, применяемые при стабилизации и укреплении грунтов в строительстве дорог
Особенности технологии и технические средства, применяемые при стабилизации и укреплении грунтов в строительстве дорог Разнообразие природы Родного края Природа Удмуртии
Разнообразие природы Родного края Природа Удмуртии Морфогенез рака кишки
Морфогенез рака кишки Педсовет НАЦИОНАЛЬНАЯ СТРАТЕГИЯ ДЕЙСТВИЙ В ИНТЕРЕСАХ ДЕТЕЙ
Педсовет НАЦИОНАЛЬНАЯ СТРАТЕГИЯ ДЕЙСТВИЙ В ИНТЕРЕСАХ ДЕТЕЙ 20231016_dary_oseni
20231016_dary_oseni Возрастные особенности развития детей 5 – 6 лет
Возрастные особенности развития детей 5 – 6 лет Вредные привычки беседа
Вредные привычки беседа презентация Найди отличия
презентация Найди отличия Ротавирусная инфекция
Ротавирусная инфекция Сварка и пайка конструкционных материалов
Сварка и пайка конструкционных материалов презентация к элективному занятию по теме Элементы комбинаторики (правило суммы и произведения)
презентация к элективному занятию по теме Элементы комбинаторики (правило суммы и произведения) Сварка меди и медных сплавов
Сварка меди и медных сплавов Медико-социальные проблемы профилактической деятельности в учреждениях здравоохранения
Медико-социальные проблемы профилактической деятельности в учреждениях здравоохранения Дифференциальные уравнения первого порядка
Дифференциальные уравнения первого порядка Классификация камер сгорания
Классификация камер сгорания Презентация к уроку Христианская семья
Презентация к уроку Христианская семья Румыния
Румыния Первая медицинская помощь при обморожении и переохлаждении
Первая медицинская помощь при обморожении и переохлаждении Қарғалы селосының экологиясы
Қарғалы селосының экологиясы Мікропроцесорна техніка
Мікропроцесорна техніка современные требования к методическим разработкам
современные требования к методическим разработкам ivchenkova
ivchenkova Менеджмент как вид управления
Менеджмент как вид управления Родительское собрание Дети и Интернет
Родительское собрание Дети и Интернет Некоторые вопросы проведения санитарно-эпидемиологической экспертизы пищевых продуктов
Некоторые вопросы проведения санитарно-эпидемиологической экспертизы пищевых продуктов