Содержание
- 2. Характеристика подгруппы Электронное строение 1S2 2S1 1S2 3S2P6 3S1 [Ne] На внешнем энергетическом уровне – nS1
- 3. Характеристика простого вещества Физические свойства:
- 4. Характеристика простого вещества Физические свойства:
- 5. Характеристика простого вещества Физические свойства:
- 6. Характеристика простого вещества Получение: Электролизом расплавов солей или щелочей КCl Электролиз К + Cl2 Эл-з 2KCl
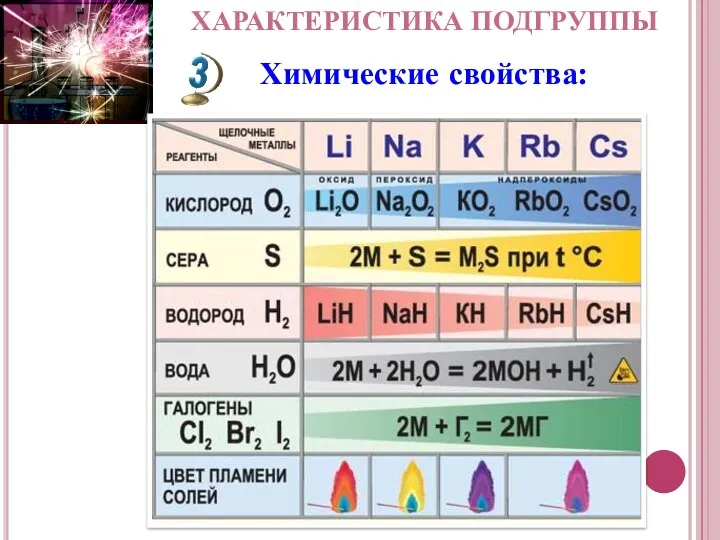
- 7. Характеристика подгруппы Ме0 – ē →Ме+ Химические свойства: восстановитель I. Взаимодействие с простыми веществами: Ме +
- 8. Характеристика подгруппы Химические свойства: Ii. Взаимодействие со сложными веществами: Ме + Н2О → MeОH + Н2↑
- 9. Характеристика подгруппы Химические свойства: Ii. Взаимодействие со сложными веществами: Ме + Н2О → MeОH + Н2↑
- 10. Характеристика подгруппы Химические свойства:
- 11. Характеристика подгруппы Химические свойства:
- 12. Характеристика подгруппы Химические свойства:
- 13. Характеристика подгруппы Химические свойства:
- 14. Характеристика подгруппы Химические свойства:
- 15. Характеристика подгруппы Химические свойства:
- 17. Скачать презентацию
![Характеристика подгруппы Электронное строение 1S2 2S1 1S2 3S2P6 3S1 [Ne]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/477386/slide-1.jpg)












 Закон больших чисел и центральная предельная теорема
Закон больших чисел и центральная предельная теорема Ну-ка вместе, ну-ка дружно!
Ну-ка вместе, ну-ка дружно! Корень. Родственные слова
Корень. Родственные слова взаимодействия классного руководителя с родителями в организации воспитательной работы учащихся начальной школы
взаимодействия классного руководителя с родителями в организации воспитательной работы учащихся начальной школы Эксплуатация водного транспорта, судовождение
Эксплуатация водного транспорта, судовождение Кроссворд
Кроссворд Үнді-будда мәдениеті
Үнді-будда мәдениеті Электрические машины постоянного тока. Назначение и устройство
Электрические машины постоянного тока. Назначение и устройство Окантовочный шов с открытым и закрытым срезом
Окантовочный шов с открытым и закрытым срезом немного обо мне
немного обо мне Презентация к уроку истории Путешествие в средневековый город
Презентация к уроку истории Путешествие в средневековый город презентация Современный урок в начальной школе с позиции формирования УУд
презентация Современный урок в начальной школе с позиции формирования УУд Нормативно-техническое регулирование в области пожарной безопасности
Нормативно-техническое регулирование в области пожарной безопасности Расселение восточных славян
Расселение восточных славян Триггеры
Триггеры Мифы Древней Греции
Мифы Древней Греции Фармакоэпидемиология и фармакоэкономика. Использование экономической оценки, как элемент принятия решений в медицине
Фармакоэпидемиология и фармакоэкономика. Использование экономической оценки, как элемент принятия решений в медицине Подвесная железная дорога
Подвесная железная дорога Синтаксичні особливості українського ділового мовлення
Синтаксичні особливості українського ділового мовлення Зуботехническое материаловедение
Зуботехническое материаловедение Координаты и векторы
Координаты и векторы презентация Новогодняя сказка
презентация Новогодняя сказка Политическая реклама как форма непрямой коммуникации
Политическая реклама как форма непрямой коммуникации Отчет о реализации первого этапа проекта. Счастливы вместе
Отчет о реализации первого этапа проекта. Счастливы вместе Георгий Валентинович Плеханов
Георгий Валентинович Плеханов Моя семья
Моя семья Entertainment
Entertainment Делимое, делитель, частное
Делимое, делитель, частное