Содержание
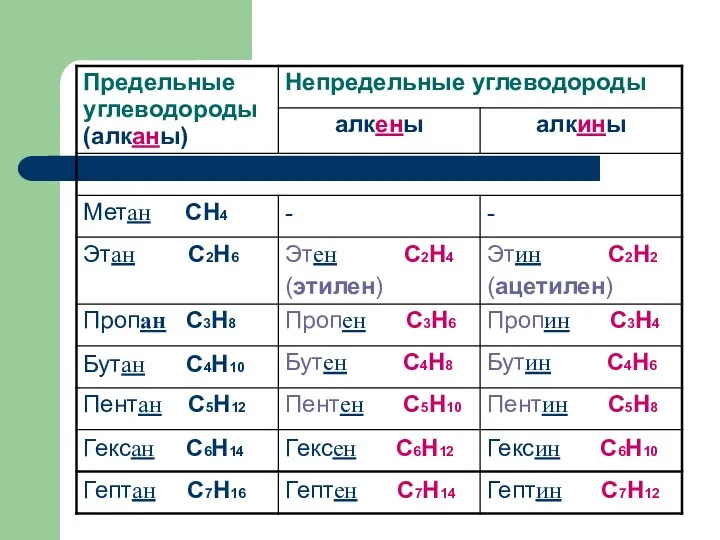
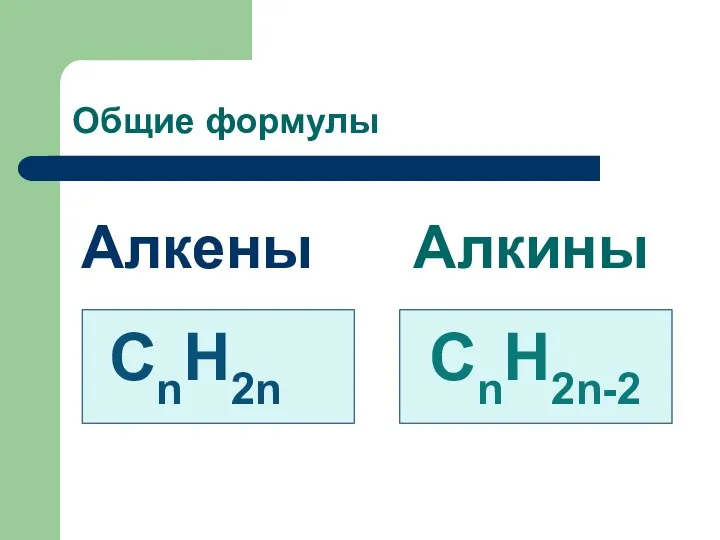
- 3. Общие формулы Алкены Алкины СnH2n CnH2n-2
- 4. Пространственное строение этилена sp2 - гибридизация одна s - орбиталь и две p - орбитали превращаются
- 5. «Гибридные" орбитали могут образовывать три σ-связи Негибридизованная р-орбиталь участвует в образовании π-связи Пространственное строение этилена
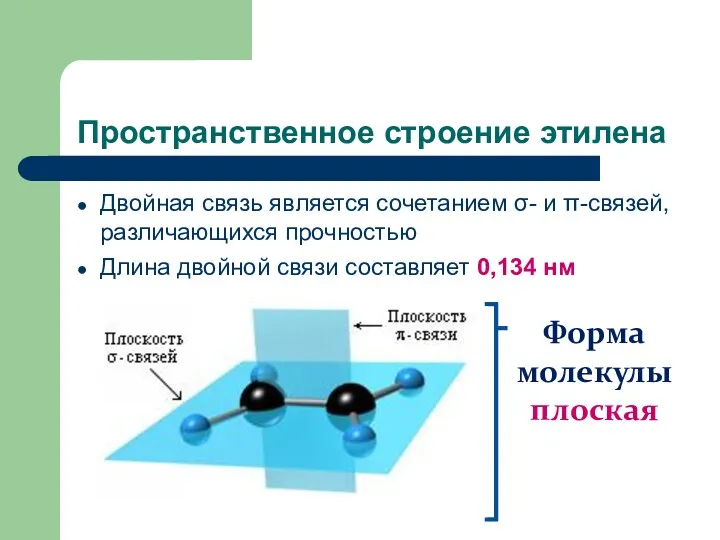
- 6. Пространственное строение этилена Двойная связь является сочетанием σ- и π-связей, различающихся прочностью Длина двойной связи составляет
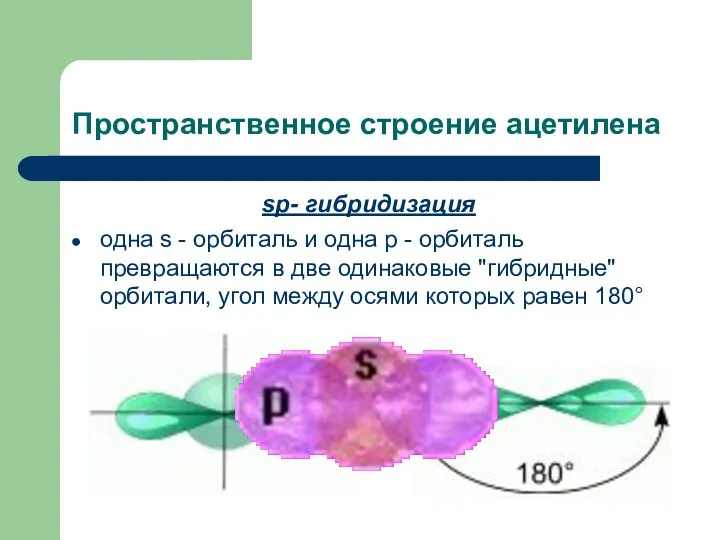
- 7. Пространственное строение ацетилена sp- гибридизация одна s - орбиталь и одна p - орбиталь превращаются в
- 8. Пространственное строение ацетилена Две р - орбитали не гибридизованы и расположены во взаимно перпендикулярных плоскостях
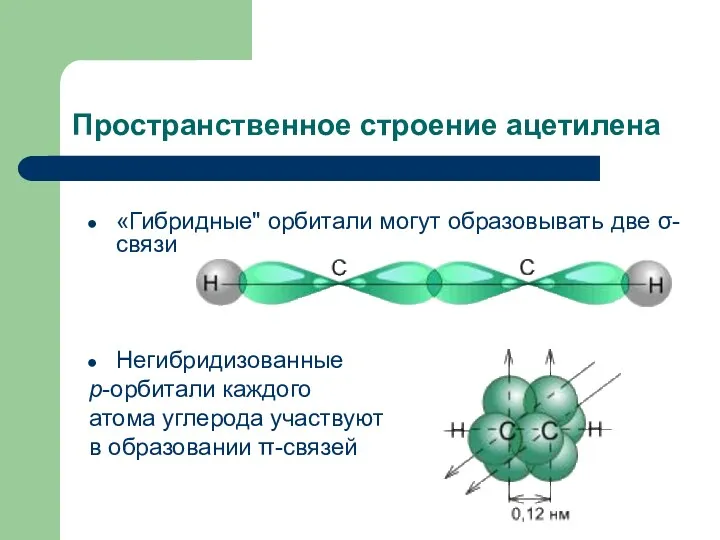
- 9. Пространственное строение ацетилена «Гибридные" орбитали могут образовывать две σ-связи Негибридизованные р-орбитали каждого атома углерода участвуют в
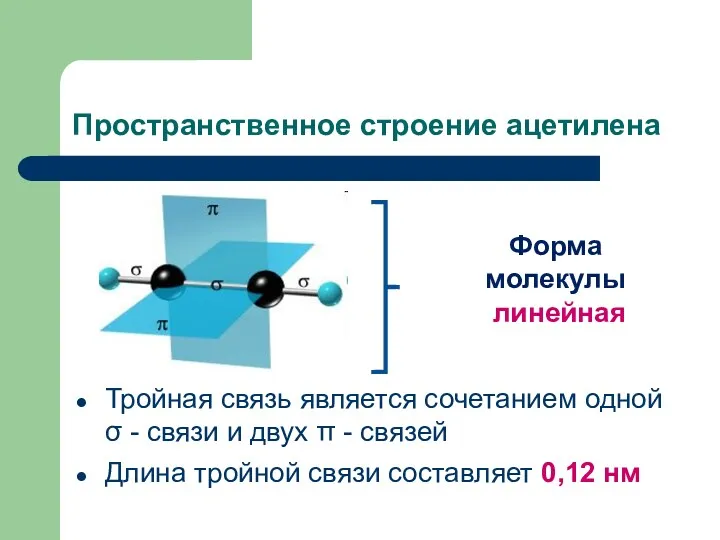
- 10. Пространственное строение ацетилена Тройная связь является сочетанием одной σ - связи и двух π - связей
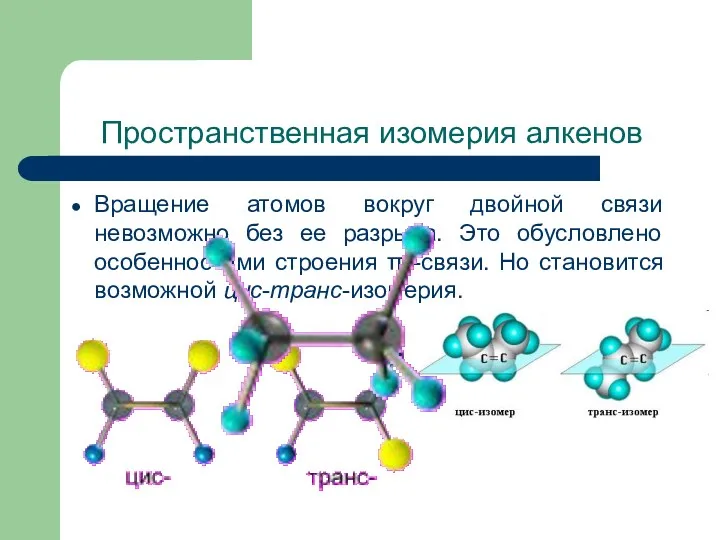
- 11. Пространственная изомерия алкенов Вращение атомов вокруг двойной связи невозможно без ее разрыва. Это обусловлено особенностями строения
- 13. Скачать презентацию



 Презентация_Селяева А.Д
Презентация_Селяева А.Д Презентация посвящённая 100-летию Г.В.Свиридова МБДОУ №25
Презентация посвящённая 100-летию Г.В.Свиридова МБДОУ №25 Важные изменения в законодательстве в 2019 году
Важные изменения в законодательстве в 2019 году Семья субъект социокультурной среды
Семья субъект социокультурной среды презентация по работе семейного клуба Счастливый ребёнок МКДОУ детский сад№4 Золотой петушок. с.Пригородное Ивановская область
презентация по работе семейного клуба Счастливый ребёнок МКДОУ детский сад№4 Золотой петушок. с.Пригородное Ивановская область Презентация 8 класс Рациональное использование природных ресурсов
Презентация 8 класс Рациональное использование природных ресурсов командная игра огонь - наш друг, огонь - наш враг
командная игра огонь - наш друг, огонь - наш враг Представление чисел в формате с плавающей запятой
Представление чисел в формате с плавающей запятой Газопламенное напыление
Газопламенное напыление Шагает эра космоса вперёд.
Шагает эра космоса вперёд. Алтайский заповедник
Алтайский заповедник Профотбор. Проблема отбора
Профотбор. Проблема отбора РобоПлатформа. Старт 2.0 Урок 10
РобоПлатформа. Старт 2.0 Урок 10 Отработка предлагаемых продаж и навыки презентации меню/
Отработка предлагаемых продаж и навыки презентации меню/ ВОИН о ВОЙНЕ работа посвящается Героям Отечества
ВОИН о ВОЙНЕ работа посвящается Героям Отечества 97 А класс әмбебап тігін машинасы
97 А класс әмбебап тігін машинасы Презентация Механические волны.
Презентация Механические волны. Презентация к уроку истории и культуры Санкт-Петербурга в 8 классе Памятники воинской славы в Санкт-Петербурге: Отечественная война 1812 года
Презентация к уроку истории и культуры Санкт-Петербурга в 8 классе Памятники воинской славы в Санкт-Петербурге: Отечественная война 1812 года Будова і технічне обслуговування транспортного засобу категорії В. Трансмісія, підвіска та механізми керування
Будова і технічне обслуговування транспортного засобу категорії В. Трансмісія, підвіска та механізми керування Рисуем пасхальные яйца
Рисуем пасхальные яйца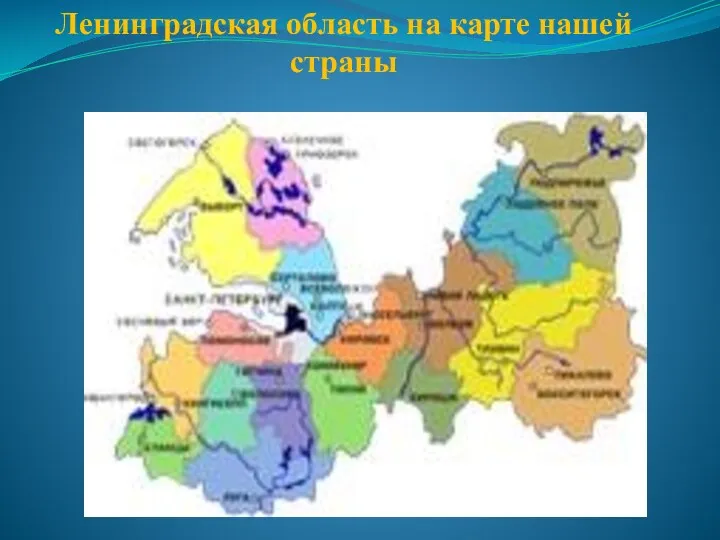 Ленинградская область на карте нашей страны
Ленинградская область на карте нашей страны Петровские преобразования: предпосылки, основные направления, результаты
Петровские преобразования: предпосылки, основные направления, результаты Заболачивание
Заболачивание Моя презентация
Моя презентация Метод щелевой разгрузки пласта в призабойной зоне скважин
Метод щелевой разгрузки пласта в призабойной зоне скважин Система входных приемных устройств 35ВВ РЛС 35Н6
Система входных приемных устройств 35ВВ РЛС 35Н6 Против неограниченной свободы
Против неограниченной свободы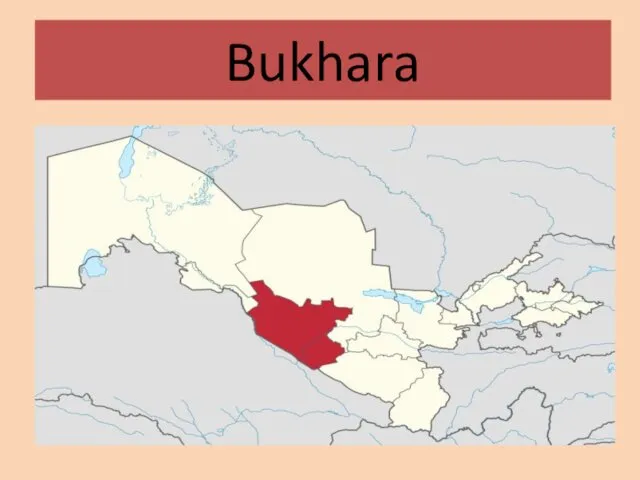 Bukhara
Bukhara