Содержание
- 2. Теория резонанса: определения Теория (метод) резонанса – способ описания сопряженных π-систем, демонстрирующий подвижность π-электронов под действием
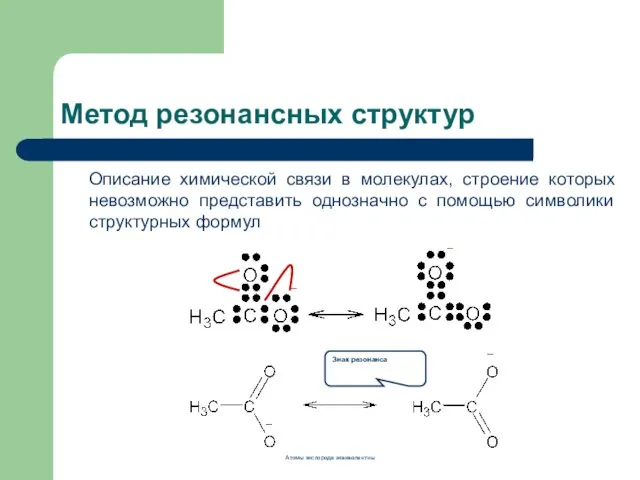
- 3. Метод резонансных структур Описание химической связи в молекулах, строение которых невозможно представить однозначно с помощью символики
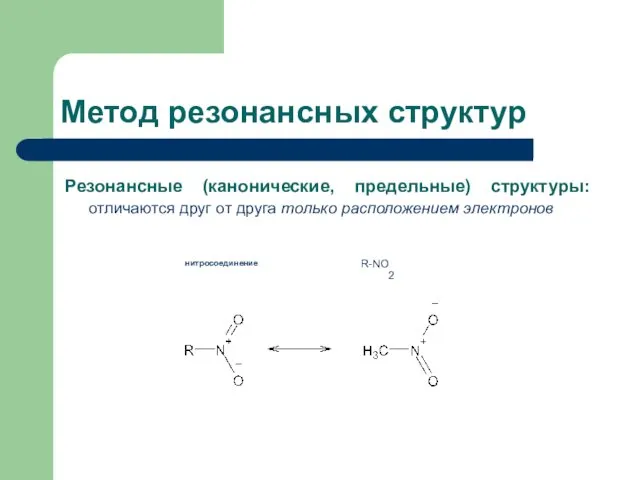
- 4. Резонансные (канонические, предельные) структуры: отличаются друг от друга только расположением электронов Метод резонансных структур
- 5. Положения метода резонанса Резонансные структуры не должны отличаться расположением атомов. 2) Каждая резонансная структура не должна
- 6. Критерии значимости резонансных структур Возможные (но неравнозначные) резонансные структуры этилена и бутадиена-1,3 Наименьшее количество неспаренных электронов
- 7. Теория резонанса развита в рамка метода ВС Распределение электронов в молекулах (сложных ионах или радикалах), является
- 9. Теория резонанса В своем простейшем виде она гласит, что если для соединения мы можем нарисовать две
- 10. Важно! О «резонансном гибриде» как замене классической формулы имеет смысл говорить лишь в том случае, если
- 11. Базовые правила 1. Положение ядер во всех канонических формах должно быть одинаковым. Изомеры, в том числе
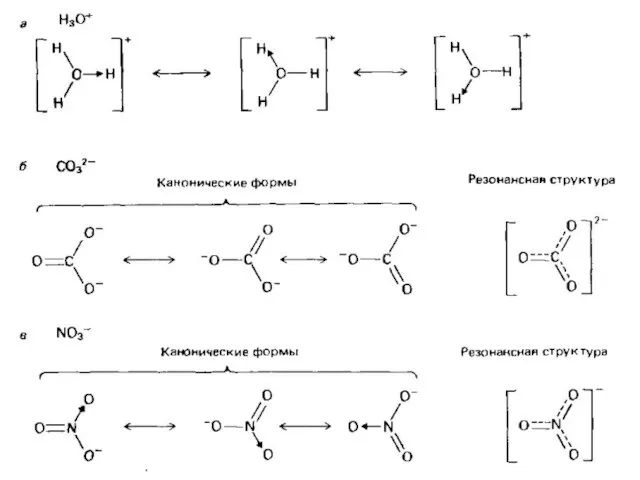
- 12. Для молекулы оксонитрида азота N2O можно записать шесть канонических форм: Реальный вклад в гибридно-резонансную структуру будут
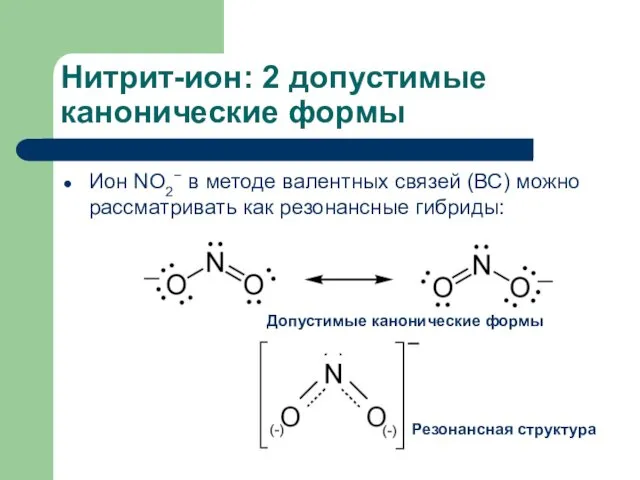
- 13. Нитрит-ион: 2 допустимые канонические формы Ион NO2− в методе валентных связей (ВС) можно рассматривать как резонансные
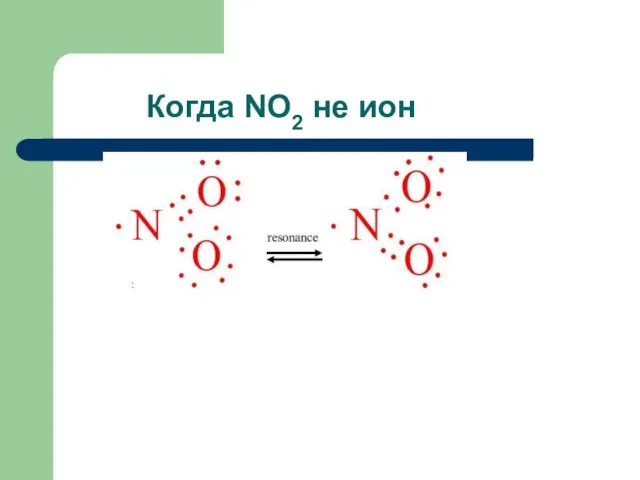
- 14. Когда NO2 не ион
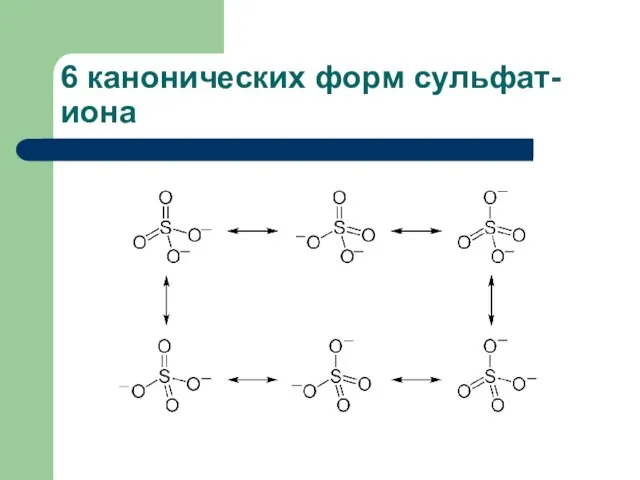
- 15. 6 канонических форм сульфат-иона
- 16. Значение электроотрицательности Почему не существует таких соединений, как H4S и H6S, где сера тоже проявляет валентность
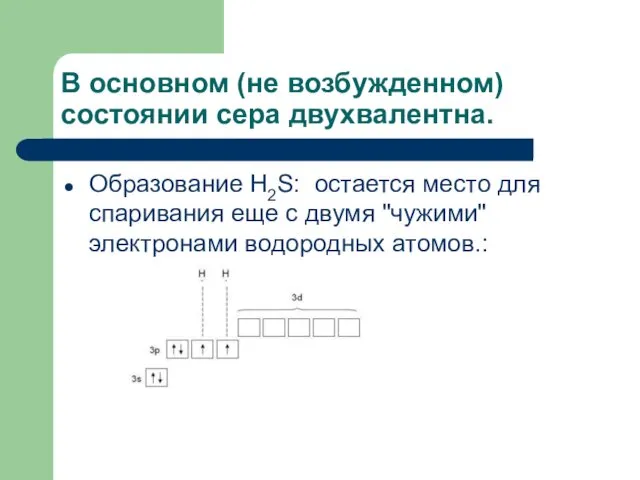
- 17. В основном (не возбужденном) состоянии сера двухвалентна. Образование H2S: остается место для спаривания еще с двумя
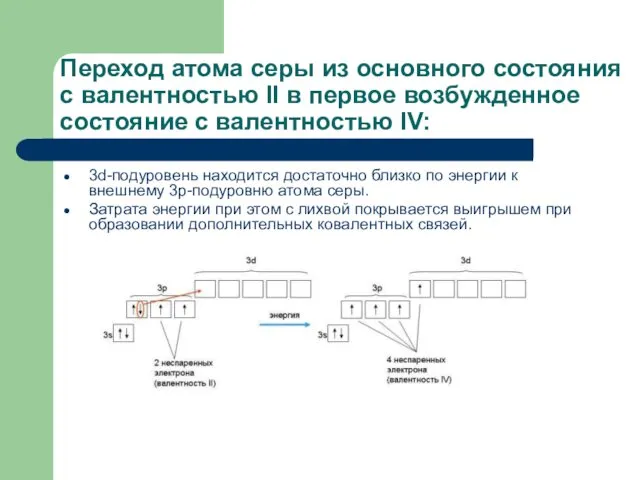
- 18. Переход атома серы из основного состояния с валентностью II в первое возбужденное состояние с валентностью IV:
- 19. Соблюдается ли правило октета? На первый взгляд, у атома серы оказывается избыток (10 электронов) и такая
- 20. Объяснение заключается в большой разнице электроотрицательностей серы (X = 2,58) и кислорода (X = 3,44) Можно
- 21. Аналогично на первый взгляд, у атома серы в триоксиде оказывается избыток (12 электронов). Строение SO3, описывается
- 22. Почему не существует H4S и H6S, где сера тоже проявляет валентность (IV) и (VI)? В этом
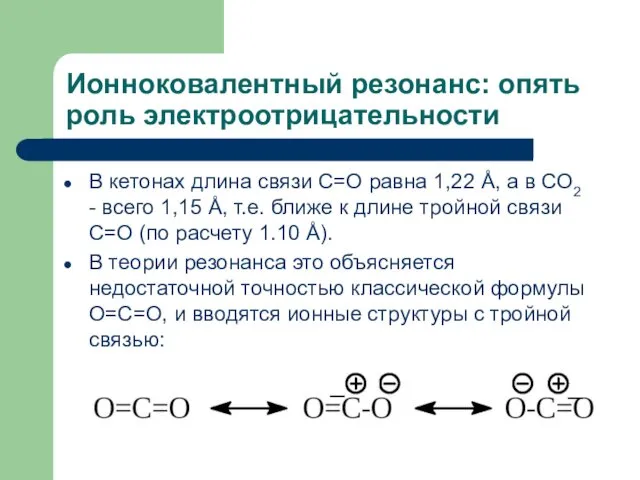
- 23. Ионноковалентный резонанс: опять роль электроотрицательности В кетонах длина связи С=О равна 1,22 Å, а в СО2
- 24. Трудности предсказания канонических форм с близкими энергиями Резонансные структуры не вытекают из квантовой механики, а в
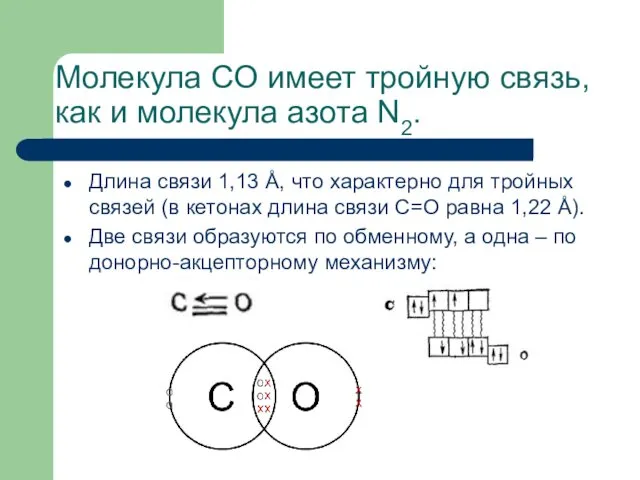
- 25. Молекула CO имеет тройную связь, как и молекула азота N2. Длина связи 1,13 Å, что характерно
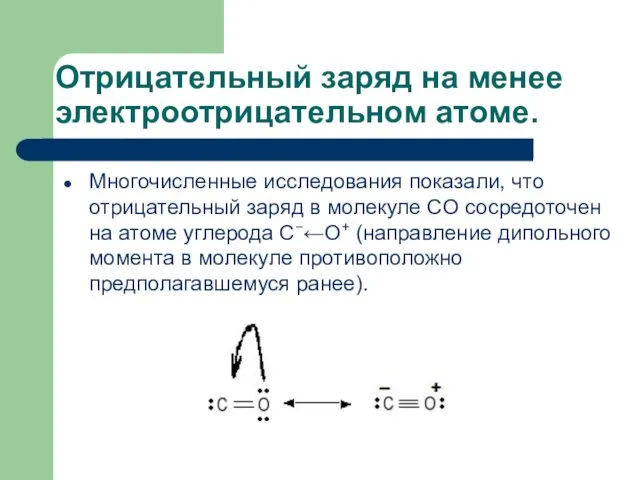
- 26. Отрицательный заряд на менее электроотрицательном атоме. Многочисленные исследования показали, что отрицательный заряд в молекуле CO сосредоточен
- 28. Скачать презентацию














 Презентация Дружба в виртуальном пространстве
Презентация Дружба в виртуальном пространстве Ультразвуковой дальномер и СОМ порт
Ультразвуковой дальномер и СОМ порт Проблемы применения новых оральных антикоагулянтов в клинической практике
Проблемы применения новых оральных антикоагулянтов в клинической практике Мои гости
Мои гости География всемирных экономических отношений
География всемирных экономических отношений ВПР 5 кл
ВПР 5 кл ОДЕЖДА ХАНТОВ И МАНСИ
ОДЕЖДА ХАНТОВ И МАНСИ Оболочки головного мозга
Оболочки головного мозга Разработка услуги по устранению дефектов кузова без повреждения лакокрасочного покрытия
Разработка услуги по устранению дефектов кузова без повреждения лакокрасочного покрытия Путешествие к истокам. Фотохроника. Волгоград, храм Николая Чудотворца на Тулака
Путешествие к истокам. Фотохроника. Волгоград, храм Николая Чудотворца на Тулака Фармакоэпидемиология и фармакоэкономика. Использование экономической оценки, как элемент принятия решений в медицине
Фармакоэпидемиология и фармакоэкономика. Использование экономической оценки, как элемент принятия решений в медицине Половинки (первый и последний звук)
Половинки (первый и последний звук) Рабочее место кассира Фрисби
Рабочее место кассира Фрисби Образец. 7 класс
Образец. 7 класс Unusual and extraordinary celebrations and festivals around the world
Unusual and extraordinary celebrations and festivals around the world Системы коммутации. Элементы сети ТфОП. (Лекция 3)
Системы коммутации. Элементы сети ТфОП. (Лекция 3) Безопасность детей в быту
Безопасность детей в быту ВИЧ-инфекция
ВИЧ-инфекция Методика проведения специсследований съемных носителей USB 3.0
Методика проведения специсследований съемных носителей USB 3.0 Атмосферное давление
Атмосферное давление  История развития интернета. Способы и скоростные характеристики подключения. Интернеттехнологии. Лекция 35-36
История развития интернета. Способы и скоростные характеристики подключения. Интернеттехнологии. Лекция 35-36 Платежный баланс Статистическая система мирохозяйственных связей
Платежный баланс Статистическая система мирохозяйственных связей Собрание
Собрание Плоскость, касательная к поверхности, нормаль поверхности
Плоскость, касательная к поверхности, нормаль поверхности Устройство шлюпки ЯЛ-6
Устройство шлюпки ЯЛ-6 Обмен углеводов
Обмен углеводов Резкость изображения
Резкость изображения Бег на средние дистанции
Бег на средние дистанции