Содержание
- 2. План Энергетика химических и фазовых превращений 1.1 Основные понятия термодинамики: система, энергия (внутренняя, тепловая, механическая), параметры
- 3. ТЕРМОДИНАМИКА ХИМИЧЕСКИХ ПРОЦЕССОВ Основные понятия: Химическая термодинамика – раздел химии, изучающий энергетику химических и фазовых превращений,
- 4. ТЕРМОДИНАМИКА ХИМИЧЕСКИХ ПРОЦЕССОВ Основные понятия: Термодинамическая система Окружающая среда Термодинамическая система – ограниченная часть окружающего нас
- 5. ТЕРМОДИНАМИКА ХИМИЧЕСКИХ ПРОЦЕССОВ Основные понятия: Термодинамическая система – это совокупность тел, способных обмениваться друг с другом
- 6. ТЕРМОДИНАМИКА ХИМИЧЕСКИХ ПРОЦЕССОВ Основные понятия: Термодинамические параметры – это величины, характеризующие термодинамическую систему Интенсивные параметры (их
- 7. ТЕРМОДИНАМИКА ХИМИЧЕСКИХ ПРОЦЕССОВ Основные понятия: Переход термодинамической системы из одного состояния в другое состояние I состояние
- 8. ТЕРМОДИНАМИКА ХИМИЧЕСКИХ ПРОЦЕССОВ Основные понятия: Внутренняя энергия системы (U) определяется суммарным запасом энергии составляющих систему молекул,
- 9. ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ A = pΔV – совершаемая системой работа Q = ΔU + A +
- 10. ТЕРМОДИНАМИКА ХИМИЧЕСКИХ ПРОЦЕССОВ Основные понятия: Энтальпия, Н – функция состояния, равная сумме U + pV: H
- 11. Тепловые эффекты и термохимические уравнения реакций Раздел химической термодинамики, в котором изучают теплоты (±Q) химических реакций
- 12. ТЕПЛОВЫЕ ЭФФЕКТЫ РЕАКЦИЙ И ТЕРМОХИМИЧЕСКИЕ УРАВНЕНИЯ Пример: Реакция образования воды из простых веществ выражается термохимическим уравнением:
- 13. ЗАКОН ГЕССА Изменение энтальпии ΔНр-ции (изменение теплового эффекта Qр-ции) химической реакции не зависит от промежуточных стадий
- 16. ЗАКОН ГЕССА Пример: Определить изменение энтальпии ΔHх в реакции взаимодействия газообразного аммиака с раствором хлороводородной кислоты
- 17. ЗАКОН ГЕССА, следствие, математическое выражение: ΔНºр-ции = Σ ni ∙ΔНºf (прод.) – Σ nj ∙ΔНºf (исх.
- 18. ТЕРМОДИНАМИКА ХИМИЧЕСКИХ РЕАКЦИЙ Основные понятия: Энтропия (S) – функция состояния системы, такая же фундаментальная и универсальная,
- 19. ВТОРОЕ НАЧАЛО (ЗАКОН) ТЕРМОДИНАМИКИ Р. Клаузиус, 1850 г.; У. Томпсон (лорд Кельвин), 1851 г. Предпосылки: исследования
- 20. ВТОРОЕ НАЧАЛО (ЗАКОН) ТЕРМОДИНАМИКИ – Все системы самопроизвольно стремятся достигнуть состояния с наибольшей разупорядоченностью (с бóльшим
- 21. ИЗМЕНЕНИЕ ЭНТРОПИИ, ΔS Энтропия всегда увеличивается (ΔS > 0) в процессах: при переходе из конденсированного состояния
- 22. Таблица 1 – Стандартные энтропии S° простых и сложных веществ
- 23. ТЕРМОДИНАМИКА ХИМИЧЕСКИХ РЕАКЦИЙ Основные понятия: Энергия Гиббса (G) (изобарно-изотермический потенциал, свободная энергия, Дж, кДж, кДж/моль) –
- 24. Таблица 2 – Критерии возможности самопроизвольного протекания процессов
- 25. ИЗМЕНЕНИЕ ЭНЕРГИИ ГИББСА Стандартные значения ΔНºf, Sº, ΔGºf приведены в справочных таблицах. ΔНºf и ΔGºf –
- 26. Таблица 3 – Возможность и условия протекания реакций в зависимости от характера изменения энтальпии ΔНº ,
- 28. Скачать презентацию
 Презентация Поэзия Северного сияния
Презентация Поэзия Северного сияния Художественно - эстетическое развитие в первой младшей группе
Художественно - эстетическое развитие в первой младшей группе Fiziko-khimicheskie_pokazateli_i_biokhimicheskie_svoystva_moloka_2011-2012_uch_god_1
Fiziko-khimicheskie_pokazateli_i_biokhimicheskie_svoystva_moloka_2011-2012_uch_god_1 Презентация к классному часу Путешествие по Галактике Здоровья
Презентация к классному часу Путешествие по Галактике Здоровья Цветная металлургия
Цветная металлургия Словосочетание. Состав словосочетания
Словосочетание. Состав словосочетания Паренхиматозные дистрофии
Паренхиматозные дистрофии Прочностной мониторинг как составная часть научно-технического сопровождения
Прочностной мониторинг как составная часть научно-технического сопровождения История Древнего мира: социально-экономические и внутриполитические процессы
История Древнего мира: социально-экономические и внутриполитические процессы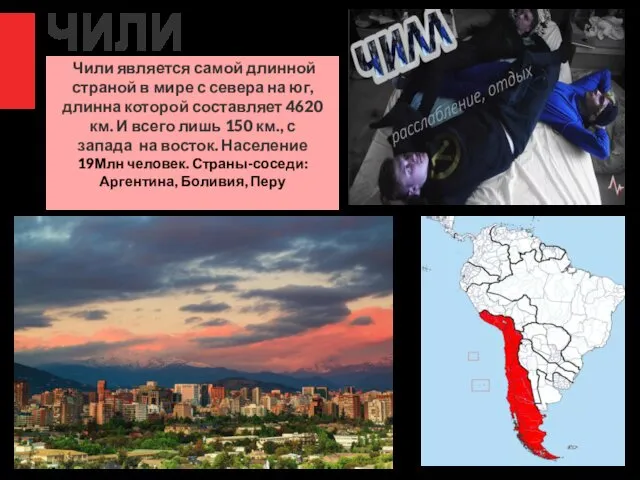 Государство Чили
Государство Чили Прогулка 2 младшей группы Звездочки -Елочка- красавица
Прогулка 2 младшей группы Звездочки -Елочка- красавица Табиғи және техногенді радияциялық фон. Иондық сәулелену көзінің адам ағзасына әсерінің салдары
Табиғи және техногенді радияциялық фон. Иондық сәулелену көзінің адам ағзасына әсерінің салдары Электрооборудование экскаваторов с приводом от двигателей внутреннего сгорания
Электрооборудование экскаваторов с приводом от двигателей внутреннего сгорания способы сжатия текста
способы сжатия текста Методическая разработка урока по теме Ткани растений для учащихся 5 класса
Методическая разработка урока по теме Ткани растений для учащихся 5 класса Неотложная помощь при ишемическом инсульте
Неотложная помощь при ишемическом инсульте Транзисторы. Реальная структура транзистора
Транзисторы. Реальная структура транзистора КНБК
КНБК Безнең эшләребез.
Безнең эшләребез. Александр Сергеевич Пушкин. Последние годы. Дуэль и смерть
Александр Сергеевич Пушкин. Последние годы. Дуэль и смерть Водоросли
Водоросли Бесплатный онлайн-курс Дизайнер сайтов с нуля до профи
Бесплатный онлайн-курс Дизайнер сайтов с нуля до профи Кофейная акварель
Кофейная акварель Семинар. Игровая технология в образовательном - воспитательном процессе ДОУ. Слайд 4
Семинар. Игровая технология в образовательном - воспитательном процессе ДОУ. Слайд 4 Прибавление числа 9
Прибавление числа 9 Верую во единаго Бога Отца
Верую во единаго Бога Отца Методический семинар: Ролевые игры - как средство вхождения ребёнка в социум.
Методический семинар: Ролевые игры - как средство вхождения ребёнка в социум. Архангельск - город воинской славы
Архангельск - город воинской славы