Содержание
- 2. Из меня состоит все живое: Я - графит, антрацит и алмаз. Я на улице, в школе
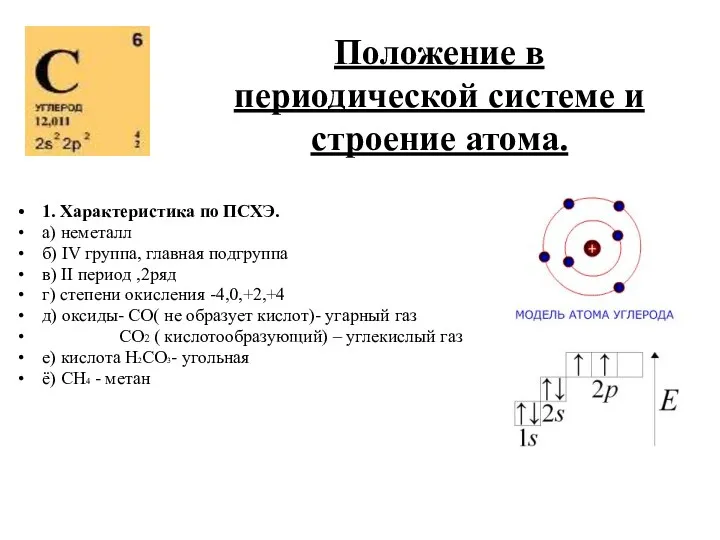
- 3. Положение в периодической системе и строение атома. 1. Характеристика по ПСХЭ. а) неметалл б) IV группа,
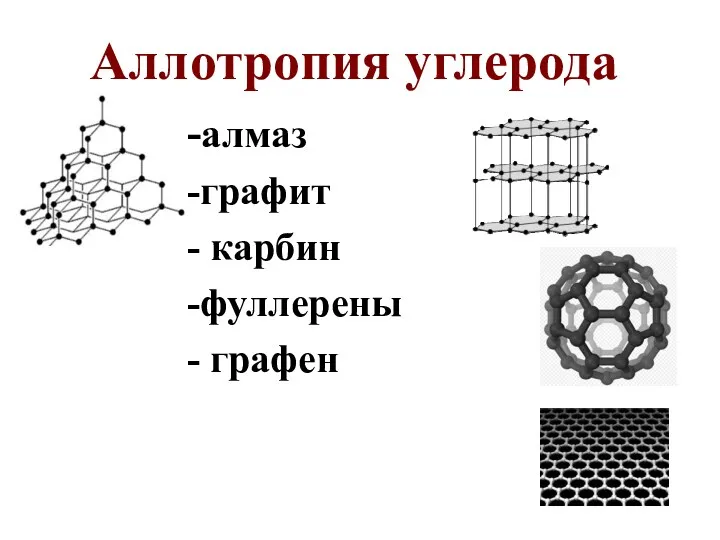
- 4. Аллотропия углерода -алмаз -графит - карбин -фуллерены - графен
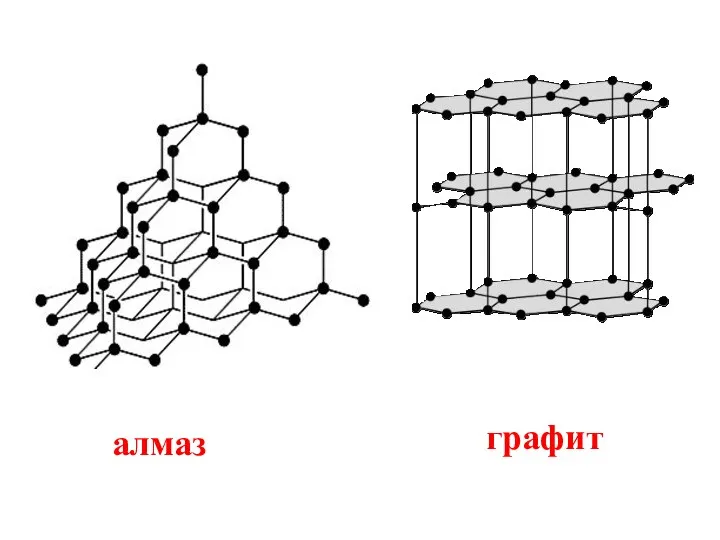
- 5. алмаз графит
- 6. Алмаз Прозрачный кристаллический Тугоплавкий Очень твердый Не проводит электрический ток Высокая светоотражаемость Графит Темно-серый кристалический Тугоплавкий
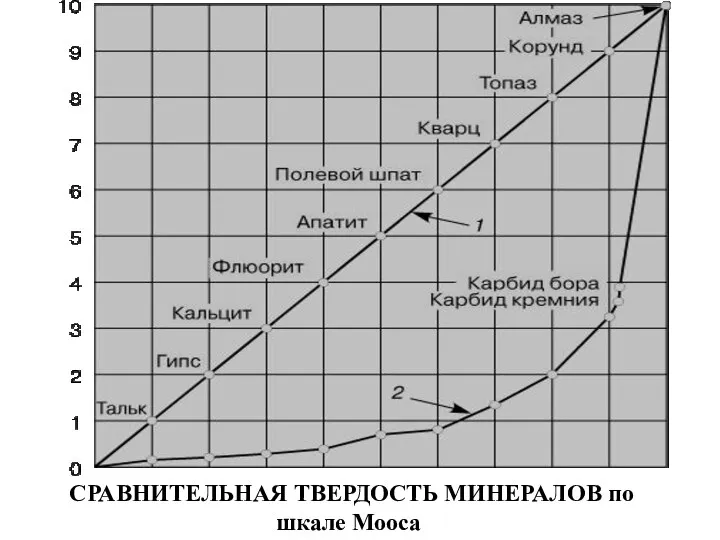
- 7. СРАВНИТЕЛЬНАЯ ТВЕРДОСТЬ МИНЕРАЛОВ по шкале Мооса
- 8. Применение алмазов.
- 9. Применение графита. электроды нагреватели
- 10. электроды В каких изделиях использован графит, а в каких алмаз?
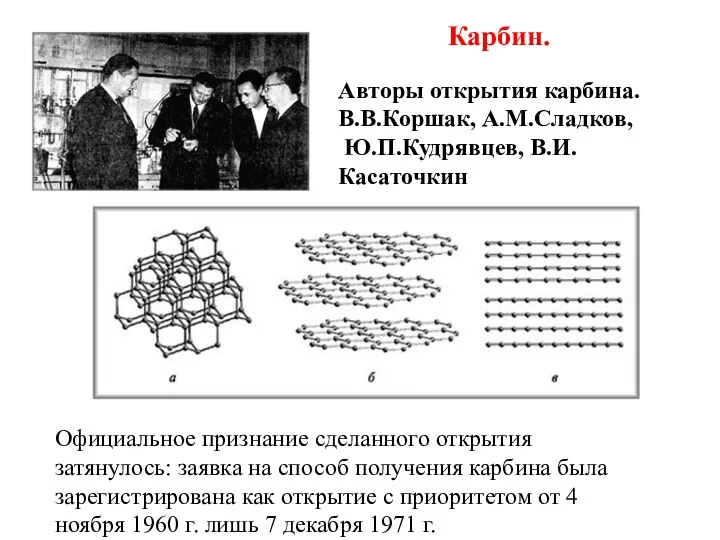
- 11. Авторы открытия карбина. В.В.Коршак, А.М.Сладков, Ю.П.Кудрявцев, В.И.Касаточкин Официальное признание сделанного открытия затянулось: заявка на способ получения
- 12. Фуллерены 1985 год - Ричард Смэлли, Роберт Керл и Гарольд Крото открыли фуллерены. Впервые сумели измерить
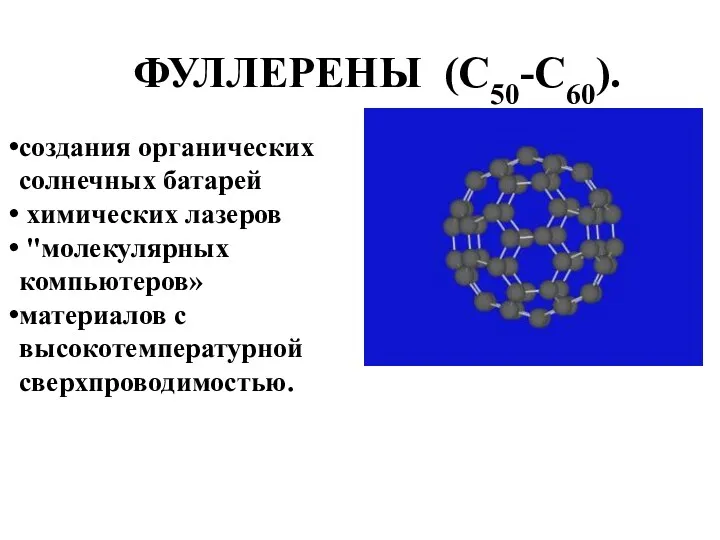
- 13. ФУЛЛЕРЕНЫ (С50-С60). создания органических солнечных батарей химических лазеров "молекулярных компьютеров» материалов с высокотемпературной сверхпроводимостью.
- 14. ДВАДЦАТИЭТАЖНЫЙ ГЕОДЕЗИЧЕСКИЙ КУПОЛ из стали и пластмасс на всемирной выставке в Монреале (1967).
- 16. Количества материала весом всего несколько граммов достаточно для того, чтобы покрыть футбольное поле
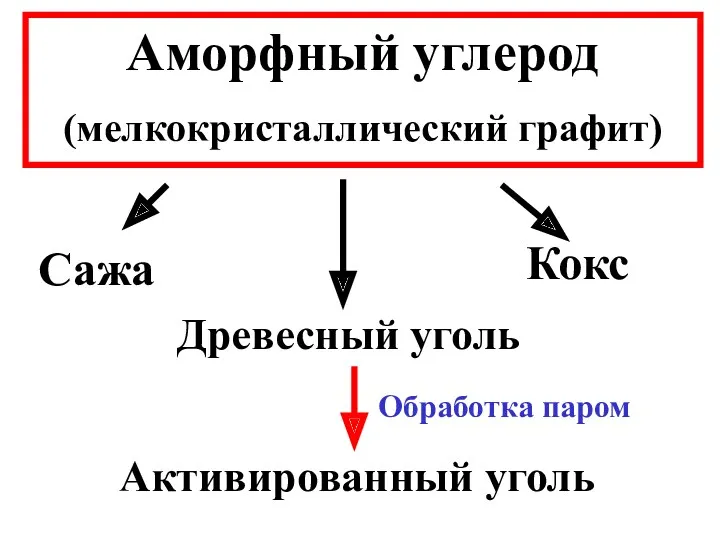
- 17. Аморфный углерод (мелкокристаллический графит) Сажа Кокс Древесный уголь Активированный уголь Обработка паром
- 18. Что вы знаете об активированном угле?
- 19. АДСОРБЦИЯ – способность твердого вещества поглощать газы и растворенные вещества.
- 21. Зелинский Николай Дмитриевич
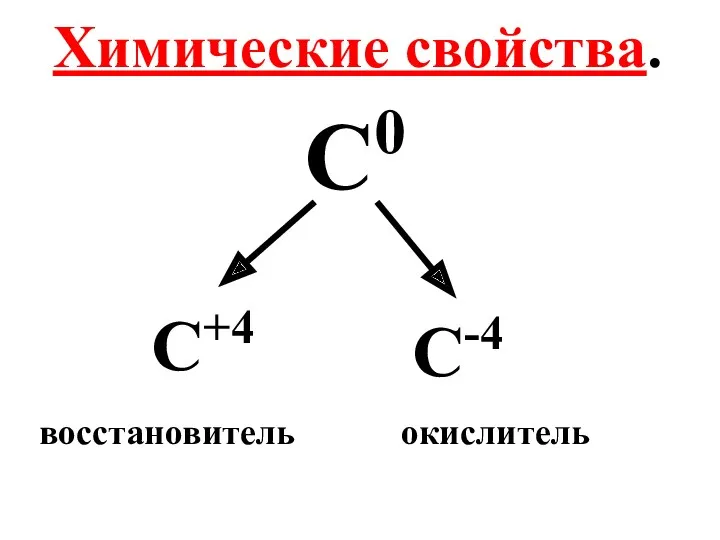
- 22. Химические свойства. С0 С+4 С-4 восстановитель окислитель
- 23. C+2H2→CH4 ( метан) Как изменяется степень окисления углерода в этих реакциях? Какие свойства проявляет углерод? 3C+4Al→Al4C3
- 24. Al4C3 + 12H2O → 4Al(OH)3 + 3CH4↑ CaC2 – карбид кальция CaC2 + 2H2O → Ca(OH)2
- 25. C+O2→CO2 Как изменяется степень окисления углерода в этих реакциях? Как называются продукты этих реакций? 2C+O2→2CO
- 26. ЗАДАЧА. Известно, что легковой автомобиль загрязняет воздух выбросами, на каждые 10 км пути с его выхлопами
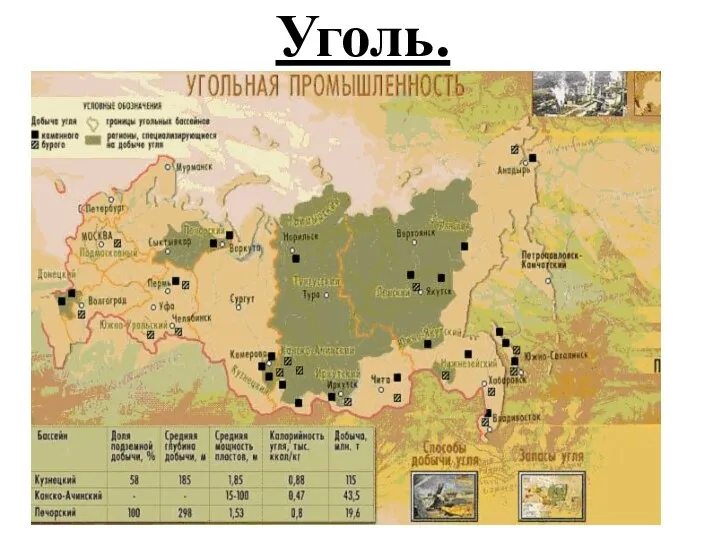
- 27. Уголь.
- 28. Нефть.
- 31. Скачать презентацию



















 Инновационные технологии
Инновационные технологии Презентация классного руководителя, часть 2
Презентация классного руководителя, часть 2 Боги и люди в Синтоизме
Боги и люди в Синтоизме Потенциальная помехоустойчивость. Лекции №3
Потенциальная помехоустойчивость. Лекции №3 Слет МС и МР на Б/о Кичигино ООО Газпром трансгаз Екатеринбург. Мероприятия на 2018 год
Слет МС и МР на Б/о Кичигино ООО Газпром трансгаз Екатеринбург. Мероприятия на 2018 год Выступление на педсовете. Презентация. Повышение качества знаний
Выступление на педсовете. Презентация. Повышение качества знаний Презентация: Дополнительная образовательная программа - аэробика.
Презентация: Дополнительная образовательная программа - аэробика. Петли быстрых планет. Марс, Венера
Петли быстрых планет. Марс, Венера Презентация Теоретический семинар Подготовка обучающихся к участию в олимпиадах
Презентация Теоретический семинар Подготовка обучающихся к участию в олимпиадах Атлас профессий Братского политехнического колледжа
Атлас профессий Братского политехнического колледжа Презентация Культовые сооружения Саратова
Презентация Культовые сооружения Саратова Презентация исследовательской работы Подвиг подольских курсантов
Презентация исследовательской работы Подвиг подольских курсантов Философия. Введение в курс
Философия. Введение в курс Виды компьютерных модемов
Виды компьютерных модемов Лазерные системы сигнализации на железнодорожных переездах
Лазерные системы сигнализации на железнодорожных переездах Микропроцессорные устройства для систем автоматического управления
Микропроцессорные устройства для систем автоматического управления Смольный институт благородных девиц
Смольный институт благородных девиц Домашние птицы. Для дошкольников
Домашние птицы. Для дошкольников Энергетический обмен
Энергетический обмен Российское движение школьников: опыт и перспективы
Российское движение школьников: опыт и перспективы История пилотки (презентация PowerPoint)
История пилотки (презентация PowerPoint) Презентация Реализация системно-деятельностного подхода в работе с детьми дошкольного возраста
Презентация Реализация системно-деятельностного подхода в работе с детьми дошкольного возраста Основные сведения о грунтоведении
Основные сведения о грунтоведении Методы проектирования образовательных программ и индивидуальных образовательных маршрутов обучающихся общеобразовательных школ
Методы проектирования образовательных программ и индивидуальных образовательных маршрутов обучающихся общеобразовательных школ The Beatles - британская рок-группа из Ливерпуля
The Beatles - британская рок-группа из Ливерпуля Датчики. Реле
Датчики. Реле Платежный баланс Статистическая система мирохозяйственных связей
Платежный баланс Статистическая система мирохозяйственных связей Развитие лексико - грамматического строя речи для детей (4 - 7 лет) презентация. Тема: Дикие животные наших лесов
Развитие лексико - грамматического строя речи для детей (4 - 7 лет) презентация. Тема: Дикие животные наших лесов