Содержание
- 2. Основы хроматографических методов «Никакое другое открытие не оказало на исследования в органической химии такого огромного продолжительного
- 3. Из истории хроматографии Михаил Семёнович Цвет (1872—1919) День рождения хроматографии – 21 марта 1903г. Доклад М.С.
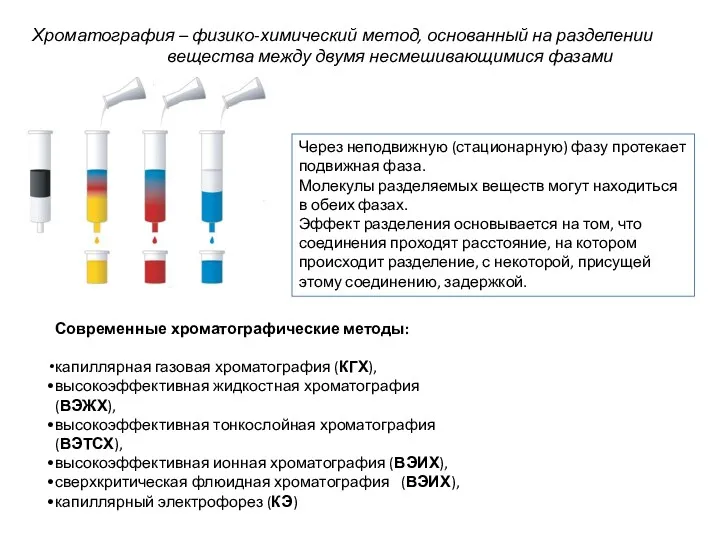
- 4. Хроматография – физико-химический метод, основанный на разделении вещества между двумя несмешивающимися фазами Через неподвижную (стационарную) фазу
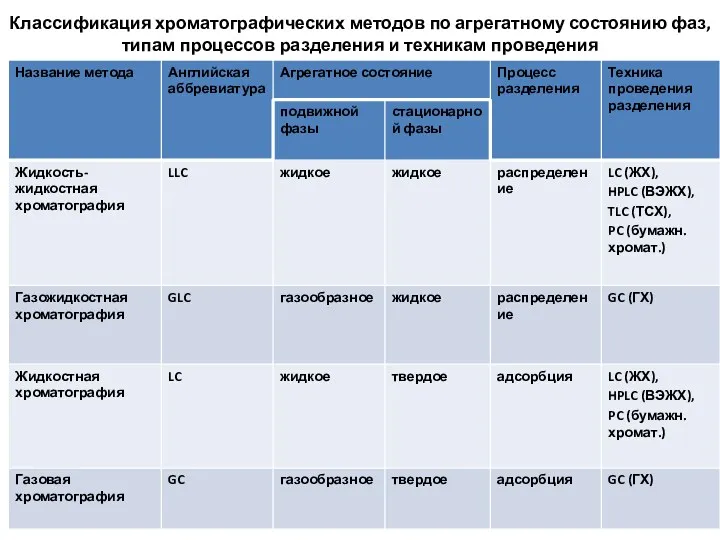
- 5. Классификация хроматографических методов по агрегатному состоянию фаз, типам процессов разделения и техникам проведения
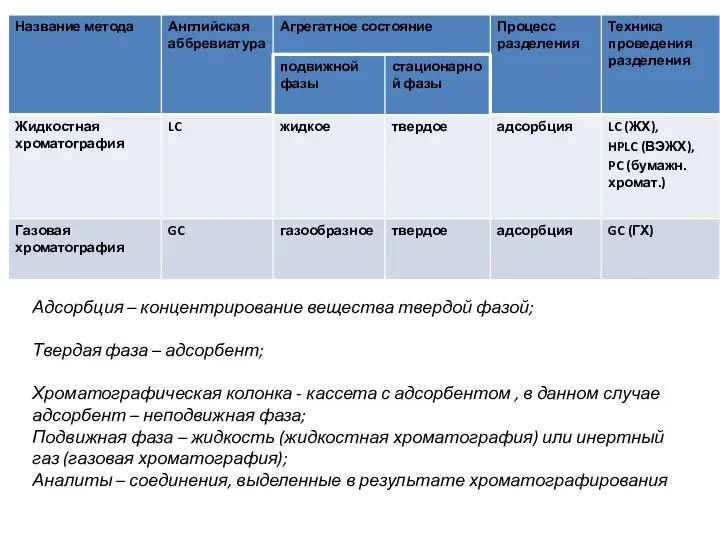
- 6. Адсорбция – концентрирование вещества твердой фазой; Твердая фаза – адсорбент; Хроматографическая колонка - кассета с адсорбентом
- 7. Жидкостная хроматография низкого давления (low pressure liguid chromatography, LPLC) используется в основном для выделения чистых веществ
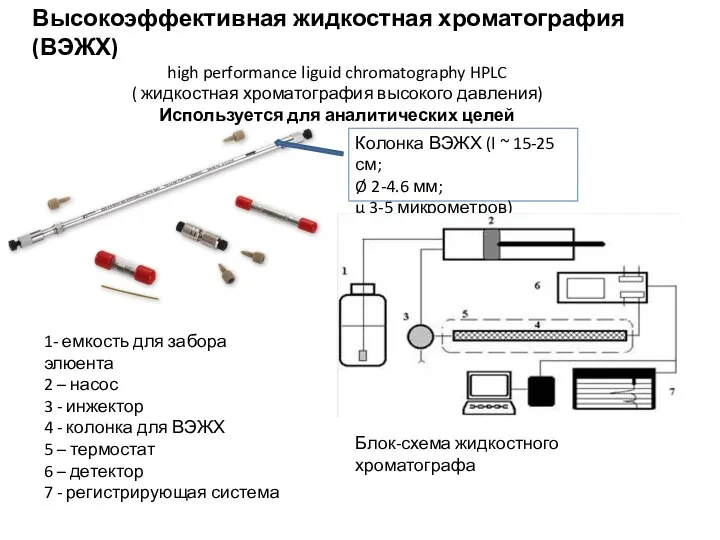
- 8. Высокоэффективная жидкостная хроматография (ВЭЖХ) high performance liguid chromatography HPLC ( жидкостная хроматография высокого давления) Используется для
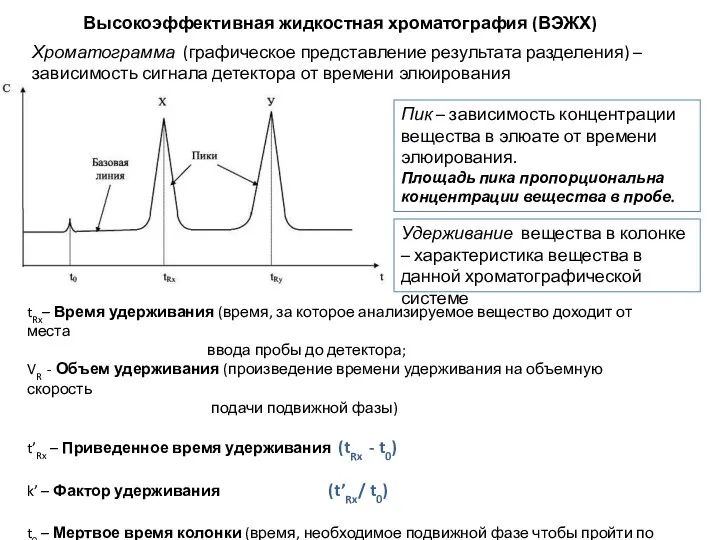
- 9. Высокоэффективная жидкостная хроматография (ВЭЖХ) Пик – зависимость концентрации вещества в элюате от времени элюирования. Площадь пика
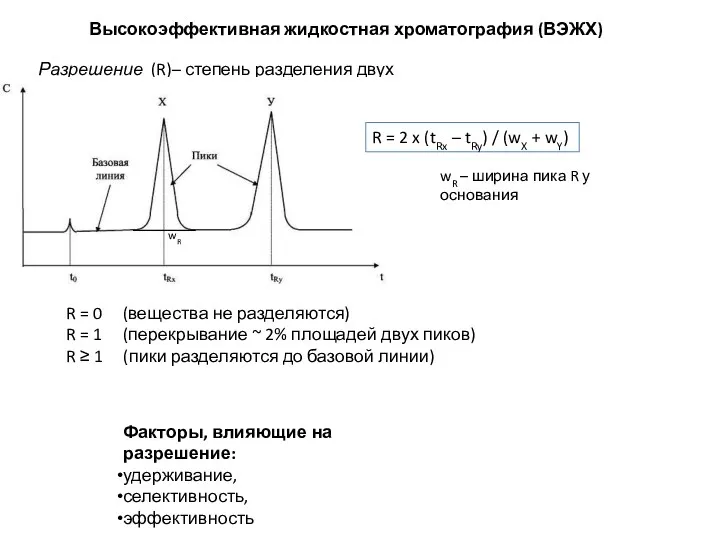
- 10. Высокоэффективная жидкостная хроматография (ВЭЖХ) Разрешение (R)– степень разделения двух веществ R = 2 x (tRx –
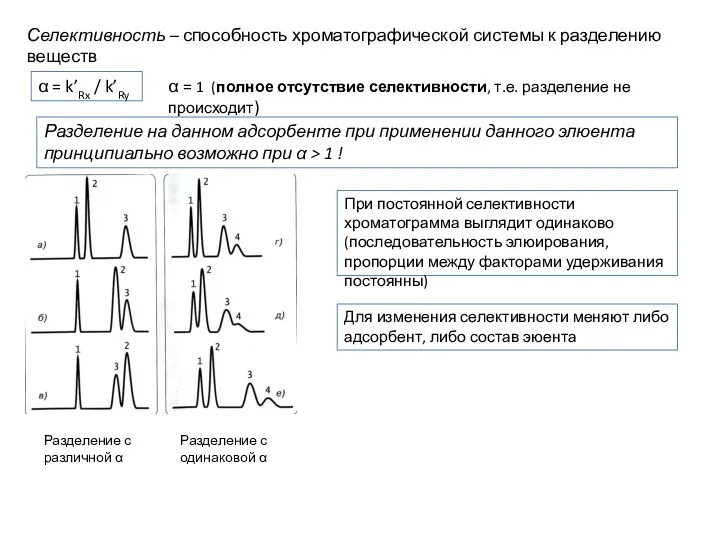
- 11. Селективность – способность хроматографической системы к разделению веществ α = k’Rx / k’Ry α = 1
- 12. Эффективность хроматографической колонки – величина размывания хроматографической зоны Эффективность (N) – свойство хроматографической колонки, определяется: размером
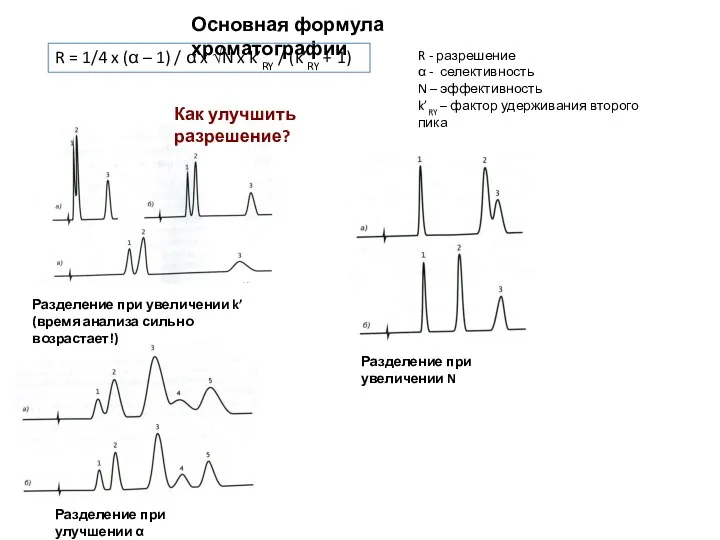
- 13. Основная формула хроматографии R = 1/4 x (α – 1) / α x √N x k’RY
- 14. Как управлять временем удерживания? Принцип «Подержать и отпустить»: в хроматографии все должно смываться, но постепенно
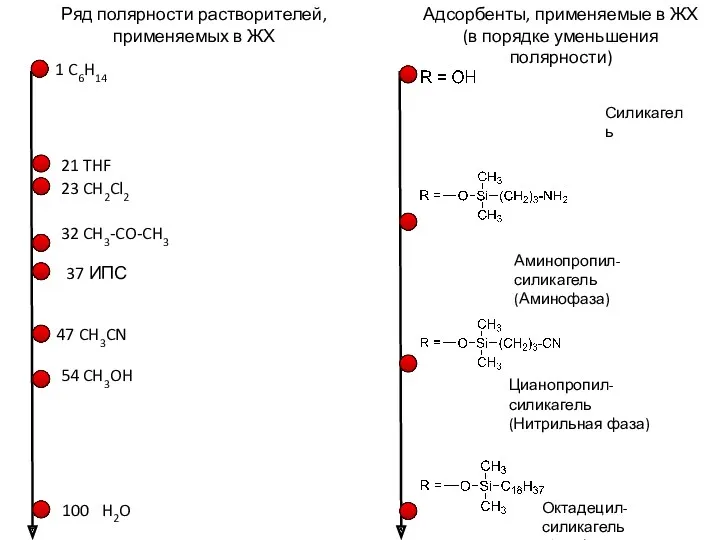
- 15. 100 H2O 54 CH3OH 47 CH3CN 37 ИПС 32 CH3-CO-CH3 23 CH2Cl2 21 THF 1 C6H14
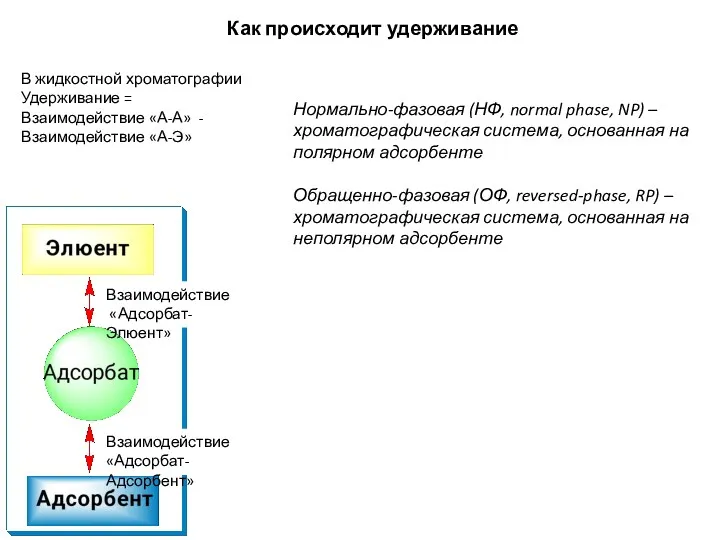
- 16. В жидкостной хроматографии Удерживание = Взаимодействие «А-А» - Взаимодействие «А-Э» Взаимодействие «Адсорбат-Элюент» Как происходит удерживание Нормально-фазовая
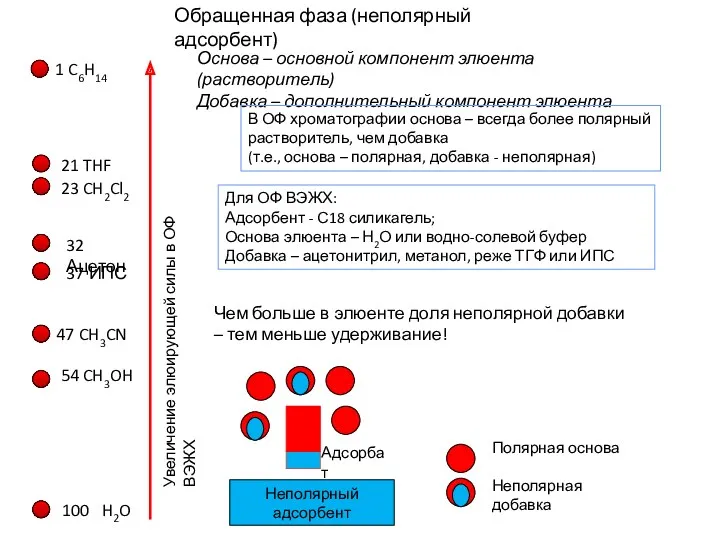
- 17. Обращенная фаза (неполярный адсорбент) Основа – основной компонент элюента (растворитель) Добавка – дополнительный компонент элюента В
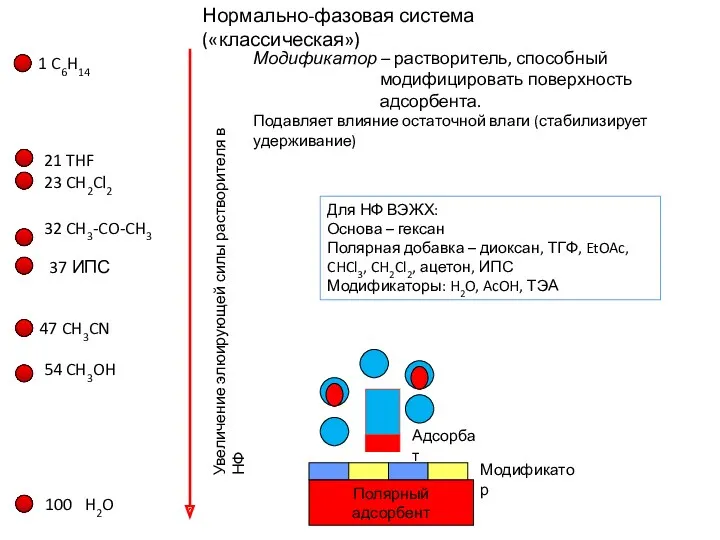
- 18. Нормально-фазовая система («классическая») 100 H2O 54 CH3OH 47 CH3CN 37 ИПС 32 CH3-CO-CH3 23 CH2Cl2 21
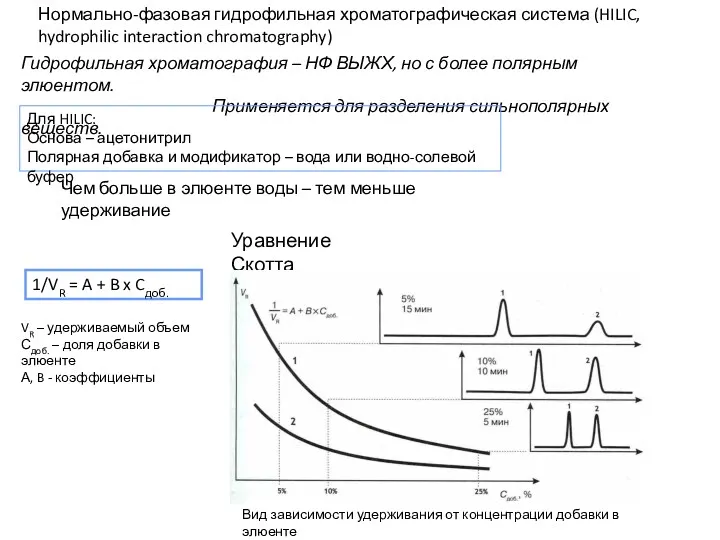
- 19. Нормально-фазовая гидрофильная хроматографическая система (HILIC, hydrophilic interaction chromatography) Гидрофильная хроматография – НФ ВЫЖХ, но с более
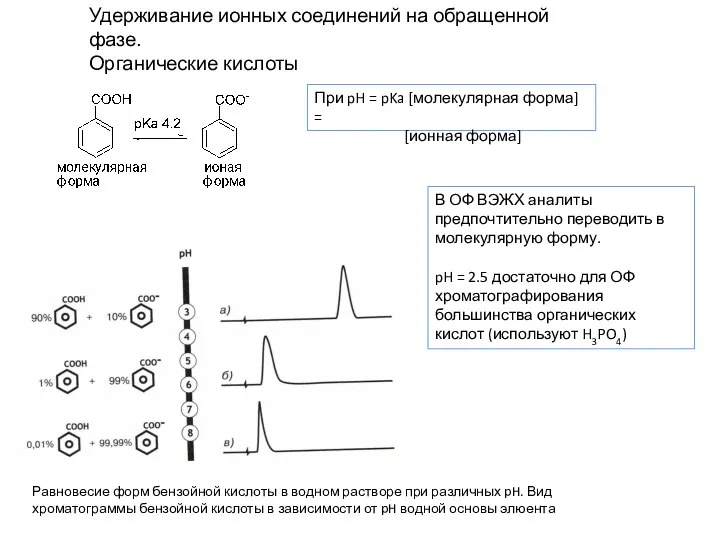
- 20. Удерживание ионных соединений на обращенной фазе. Органические кислоты При pH = pKa [молекулярная форма] = [ионная
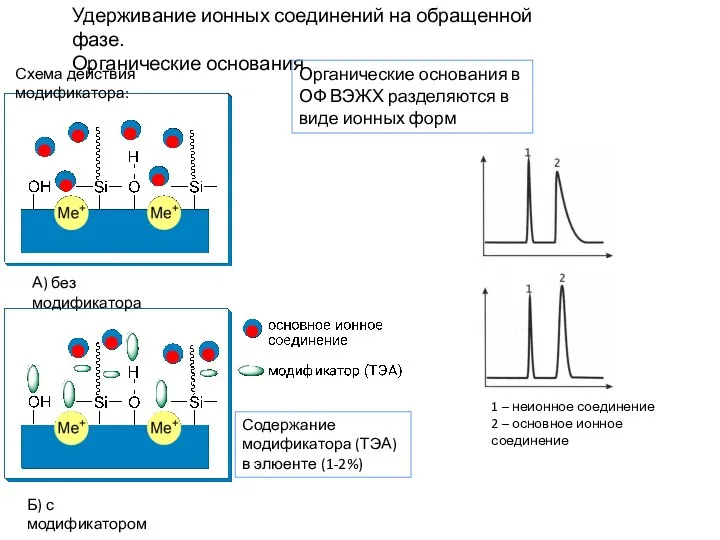
- 21. Удерживание ионных соединений на обращенной фазе. Органические основания Органические основания в ОФ ВЭЖХ разделяются в виде
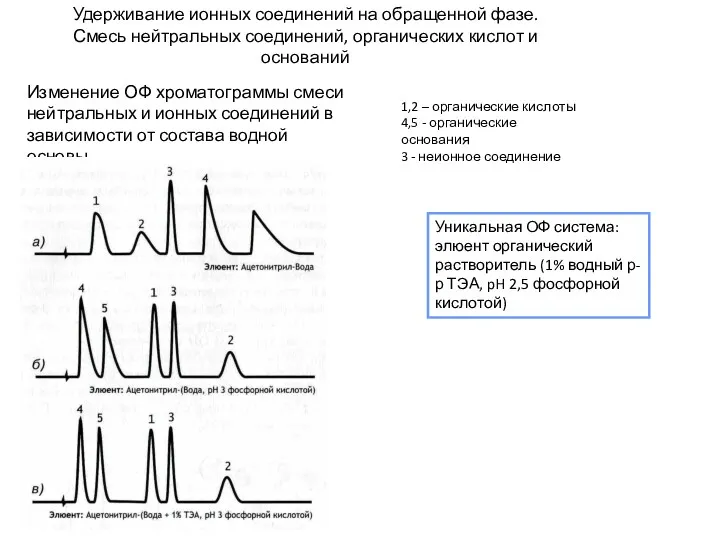
- 22. Удерживание ионных соединений на обращенной фазе. Смесь нейтральных соединений, органических кислот и оснований Уникальная ОФ система:
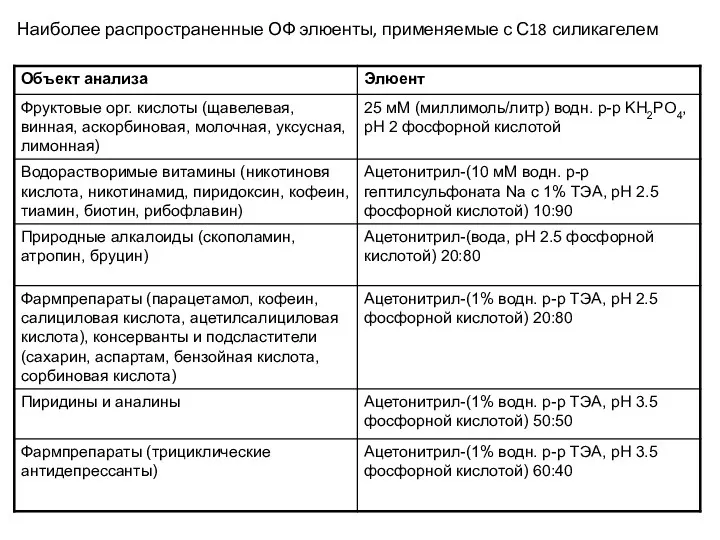
- 23. Наиболее распространенные ОФ элюенты, применяемые с С18 силикагелем
- 25. Скачать презентацию





 Удобрения, их свойства и применение
Удобрения, их свойства и применение Понятие Сбалансированное питание
Понятие Сбалансированное питание Фізіологія занього, середнього та проміжного мозку
Фізіологія занього, середнього та проміжного мозку Соединительные ткани
Соединительные ткани Сон и сновидения
Сон и сновидения Russian desman
Russian desman Изменчивость: наследственная и ненаследственная
Изменчивость: наследственная и ненаследственная Пентозо-фосфатный путь окисления глюкозы
Пентозо-фосфатный путь окисления глюкозы Кровеносная система. Внутренняя среда организма. Кровь
Кровеносная система. Внутренняя среда организма. Кровь Презентация по биологии Своя игра (обобщение по всему курсу) 8 класс
Презентация по биологии Своя игра (обобщение по всему курсу) 8 класс Микробиология зерновых продуктов
Микробиология зерновых продуктов Строение и работа сердца
Строение и работа сердца Итоговая контрольная работа. 6 класс
Итоговая контрольная работа. 6 класс Цели физического воспитания
Цели физического воспитания Способы культивирования вирусов
Способы культивирования вирусов Термодинамика биологических процессов(new)
Термодинамика биологических процессов(new) Химический состав клетки. Нуклеиновые кислоты. ДНК
Химический состав клетки. Нуклеиновые кислоты. ДНК Мутационная изменчивость
Мутационная изменчивость Гормоны поджелудочной железы
Гормоны поджелудочной железы Отряд Перепончатокрылые
Отряд Перепончатокрылые Урок на тему :Совместная жизнь видов в биогеоценозе.
Урок на тему :Совместная жизнь видов в биогеоценозе. Неорганические вещества клетки
Неорганические вещества клетки Презентация по теме Кайнозойская эра, 11 класс
Презентация по теме Кайнозойская эра, 11 класс Водоросли и их классификация
Водоросли и их классификация Строение и функции кожи
Строение и функции кожи Генетика. Наследственность. Изменчивость
Генетика. Наследственность. Изменчивость Энзимология. Структура и механизм действия ферментов. (Лекция 2)
Энзимология. Структура и механизм действия ферментов. (Лекция 2) Подготовка к ЕГЭ по биологии. 10 класс
Подготовка к ЕГЭ по биологии. 10 класс