Содержание
- 2. 1. Строение белков и история их открытия В состав белков входят химические элементы C, H, O,
- 3. Белки обладают рядом особенностей, прежде всего громадной молекулярной массой: альбумин – 36 000, гемоглобин – 152
- 4. Структура белка. Первичная структура Вторичная структура Третичная структура Четвертичная структура
- 5. Первичная структура белка. Последовательность аминокислотных звеньев в полипептидной цепочке (между звеньями -ковалентные связи)
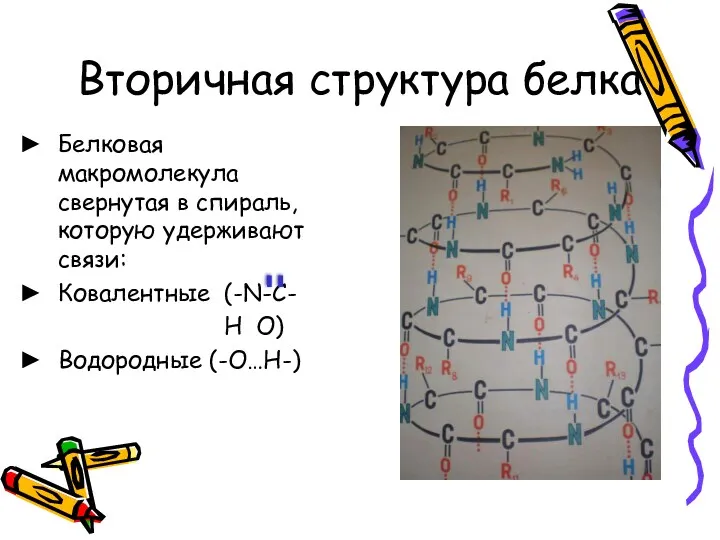
- 6. Вторичная структура белка Белковая макромолекула свернутая в спираль, которую удерживают связи: Ковалентные (-N-C- H O) Водородные
- 7. Третичная структура белка Молекула белка скручена (уложена)в фибриллу или глобулу. Связи : -ковалентные -водородные -дисульфидные(-S…S-) -ионные
- 8. Четвертичная структура белка Сложный агрегат из многих полимерных цепей. Присутствует весь комплекс перечисленных типов химических связей.
- 9. Связи: Водородные Дисульфидные Ионные Ковалентные
- 10. Функции белка Строительная Каталитическая Регуляторная Двигательная Транспортная Защитная Энергетическая
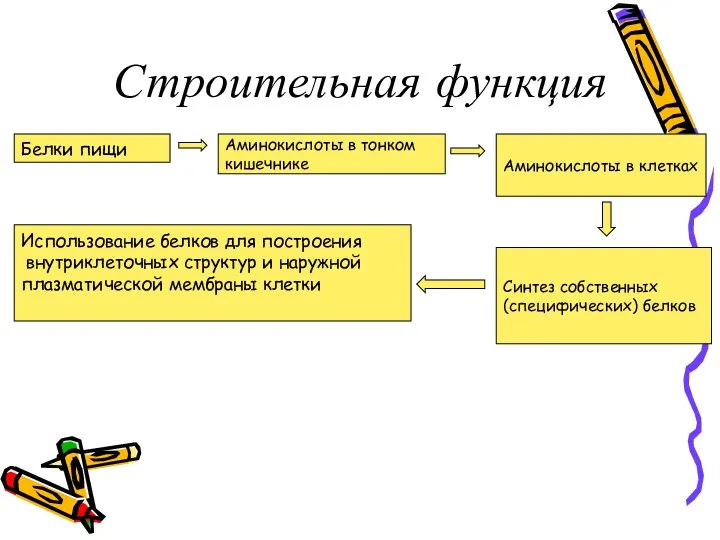
- 11. Строительная функция Белки пищи Аминокислоты в тонком кишечнике Аминокислоты в клетках Использование белков для построения внутриклеточных
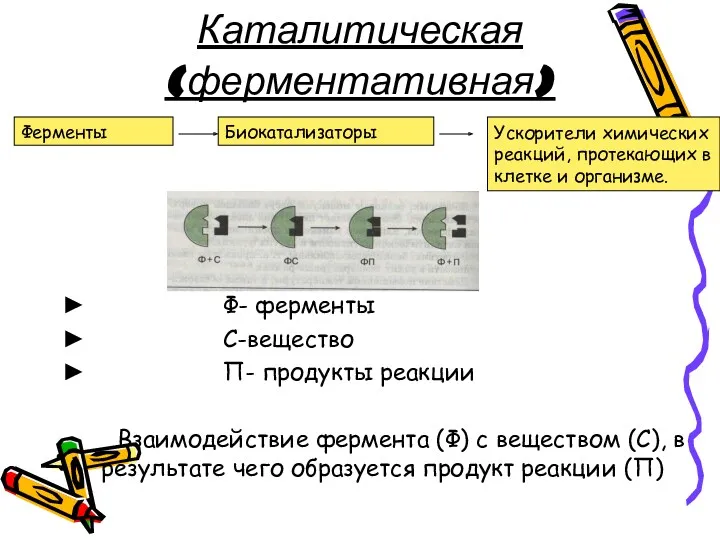
- 12. Каталитическая (ферментативная) Ф- ферменты С-вещество П- продукты реакции Взаимодействие фермента (Ф) с веществом (С), в результате
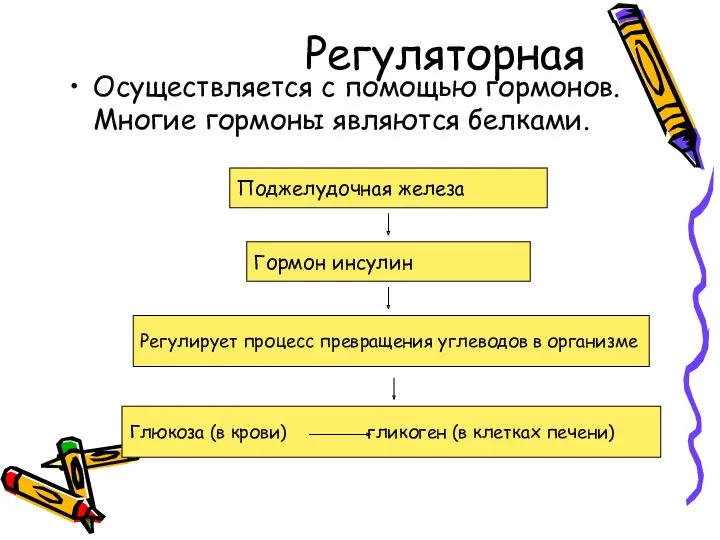
- 13. Регуляторная Осуществляется с помощью гормонов. Многие гормоны являются белками. Поджелудочная железа Гормон инсулин Регулирует процесс превращения
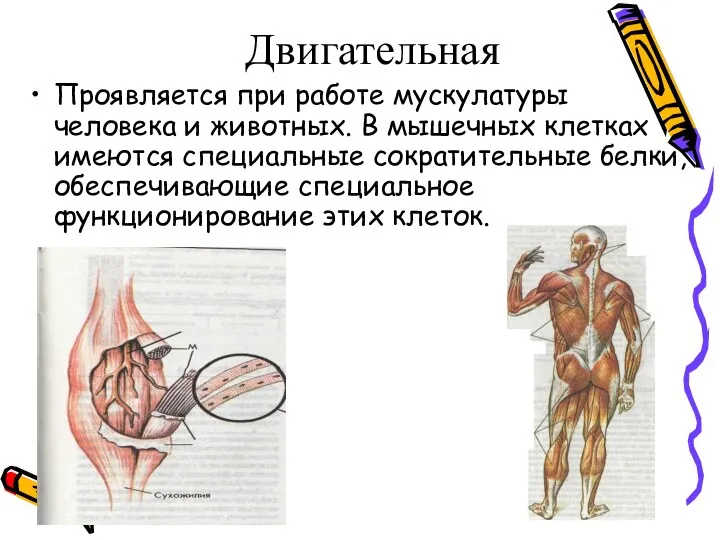
- 14. Двигательная Проявляется при работе мускулатуры человека и животных. В мышечных клетках имеются специальные сократительные белки, обеспечивающие
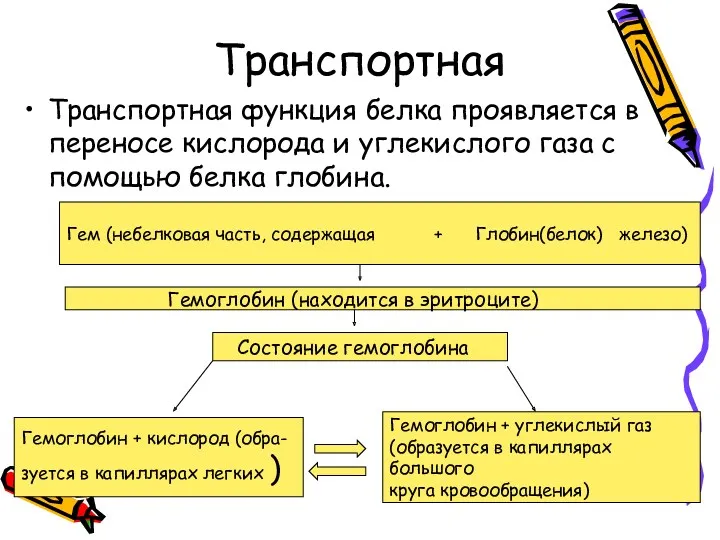
- 15. Транспортная Транспортная функция белка проявляется в переносe кислорода и углекислого газа с помощью белка глобина. Гем
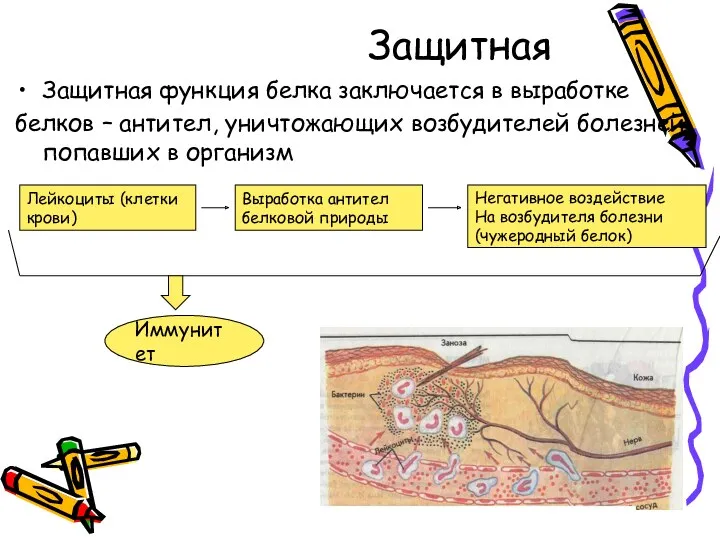
- 16. Защитная Защитная функция белка заключается в выработке белков – антител, уничтожающих возбудителей болезней, попавших в организм
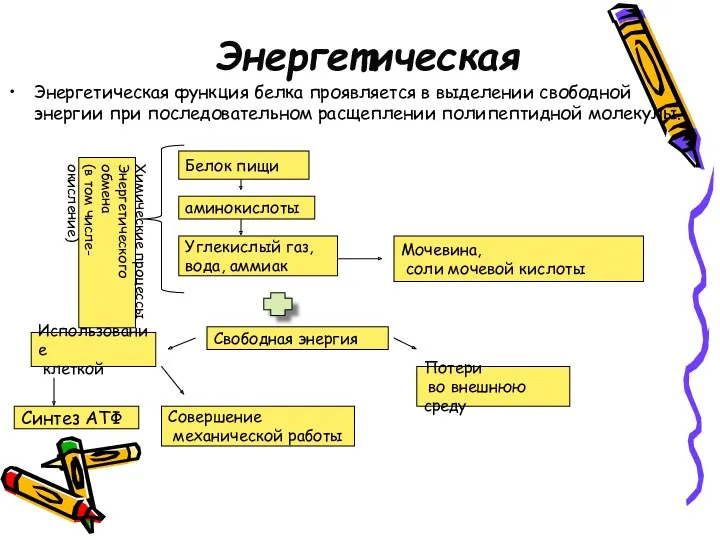
- 17. Энергетическая Энергетическая функция белка проявляется в выделении свободной энергии при последовательном расщеплении полипептидной молекулы. Белок пищи
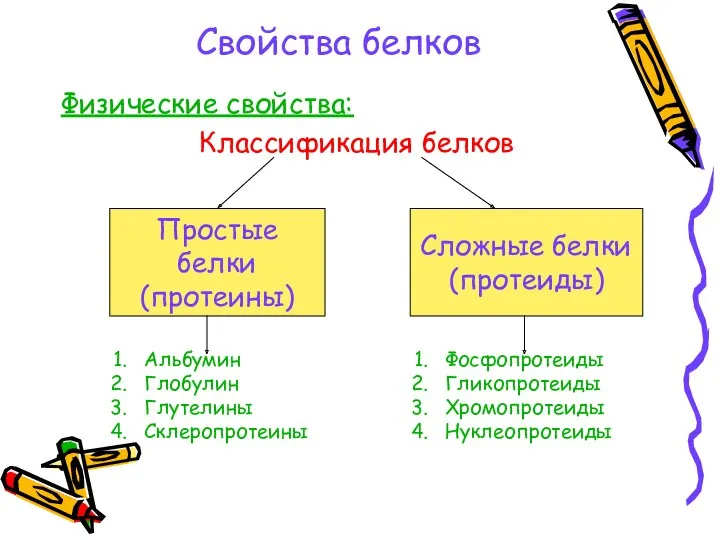
- 18. Свойства белков Физические свойства: Классификация белков Простые белки (протеины) Сложные белки (протеиды) Альбумин Глобулин Глутелины Склеропротеины
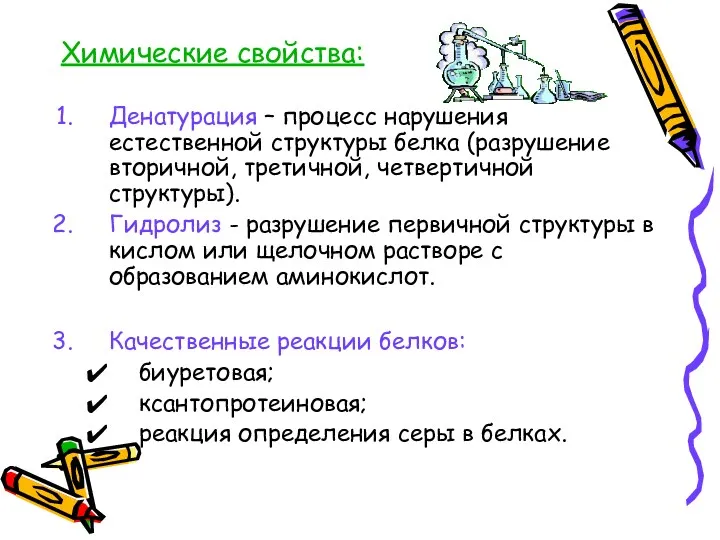
- 19. Химические свойства: Денатурация – процесс нарушения естественной структуры белка (разрушение вторичной, третичной, четвертичной структуры). Гидролиз -
- 20. Характерной реакцией на белок является биуретовая реакция. При действии водного раствора медного купороса и едкой щелочи
- 21. Денатурация белка В пробирку налили раствор яичного белка и добавили насыщенный раствор сульфата аммония. Появляется муть
- 22. пробирку с раствором белка нагрели в пламени горелки. Появляется осадок.
- 23. 1. Укажите группу химических элементов,содержание которых в клетке составляет в сумме98%: H, O, S, P H,
- 24. 2. Назовите функцию, которую выполняет основная масса белков семян растений и яйцеклеток животных: защитная строительная запасающая
- 25. 3. Назовите белок, из которого состоят рога,копыта, когти, перья и волосы животных: коллаген кератин тубулин миозин
- 26. 4. К какому виду химических связей относят пептидную связь? ионные водородные ковалентные гидрофобные
- 27. 5. Как называется структура белка, которая представляет собой цепь из аминокислот, с помощью ковалентных связей соединенных
- 28. 6. Назовите в молекуле аминокислот химическую группировку, которая придает одним аминокислотам гидрофильные, а другим –гидрофобные свойства.
- 29. 7. Назовите белки-ферменты, которые расщепляют другие белки. пепсин, трипсин гемоглобин, карбоангидраза инсулин, глюкагон коллаген, кератин актин,
- 30. 8. Как называется процесс потери белком четвертичной и третичной структур, ведущий к утрате им биологической активности?
- 31. 9. При гидролизе белков образуются: амины аминокислоты углеводы жиры
- 32. 10. Что является побочным продуктом в реакции образования белков? аммиак вода оксид углерода IV водород
- 33. 11. Назовите реакции, которые дают возможность распознать белки среди других веществ: черные цветные красные синие
- 35. Скачать презентацию






















 Происхождение собак: история и интересные факты
Происхождение собак: история и интересные факты Черепно-мозговые нервы
Черепно-мозговые нервы Рост и развитие растений
Рост и развитие растений С днём рождения, лягушка
С днём рождения, лягушка Антропогенез. Этапы антропогенеза. Эволюция приматов
Антропогенез. Этапы антропогенеза. Эволюция приматов Развитие систем регуляции организма человека
Развитие систем регуляции организма человека презентация Развитие насекомых
презентация Развитие насекомых Костная система человека
Костная система человека Строение и работа сердца. Круги кровообращения. Расположение сердца в теле человека
Строение и работа сердца. Круги кровообращения. Расположение сердца в теле человека Озеленения придомовой территории
Озеленения придомовой территории Хризофиты – золотистые водоросли
Хризофиты – золотистые водоросли Как звери зимой в лесу живут
Как звери зимой в лесу живут Среды жизни и места обитания животных. Взаимосвязь животных в природе
Среды жизни и места обитания животных. Взаимосвязь животных в природе Обмін білків
Обмін білків Здоровьесберегающие технологии на уроках биологии
Здоровьесберегающие технологии на уроках биологии Птицы города
Птицы города Взаимодействие генов
Взаимодействие генов Ресурсы диких копытных РОС РГОО “БООР” Городокского района
Ресурсы диких копытных РОС РГОО “БООР” Городокского района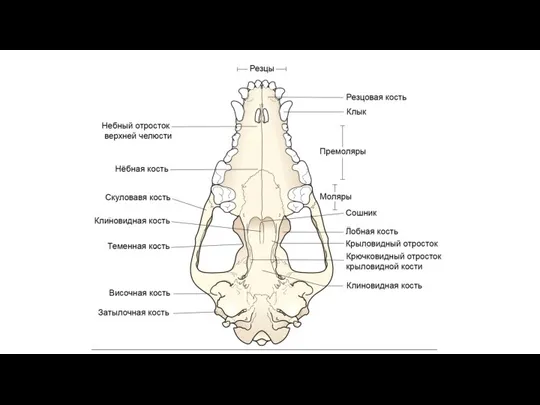 Кости черепа
Кости черепа Подцарство Многоклеточные. Тип Кишечнополостные
Подцарство Многоклеточные. Тип Кишечнополостные Кобчик - птица 2021 года
Кобчик - птица 2021 года Важелі в тілі людини
Важелі в тілі людини Биология полорогих: дзерена, сайгака, горала
Биология полорогих: дзерена, сайгака, горала Подготовка к ЕГЭ по биологии
Подготовка к ЕГЭ по биологии Царство растения. Методическая разработка. 7 класс
Царство растения. Методическая разработка. 7 класс презентация для урока биологии в 7 классе по теме: Класс Паукообразные. Строение, жизнедеятельность, размножение, многообразие, паутина и её роль. Клещи, переносчики энцефалита, меры защиты. Роль в биоценозах.
презентация для урока биологии в 7 классе по теме: Класс Паукообразные. Строение, жизнедеятельность, размножение, многообразие, паутина и её роль. Клещи, переносчики энцефалита, меры защиты. Роль в биоценозах. Сон и сновидения
Сон и сновидения Физиология психических функций. Функциональная система поведенческого акта
Физиология психических функций. Функциональная система поведенческого акта