Содержание
- 2. Цель урока: Ввести понятие термодинамических величин. Уметь записывать количественные зависимости между термодинамическими параметрами в газовых законах.
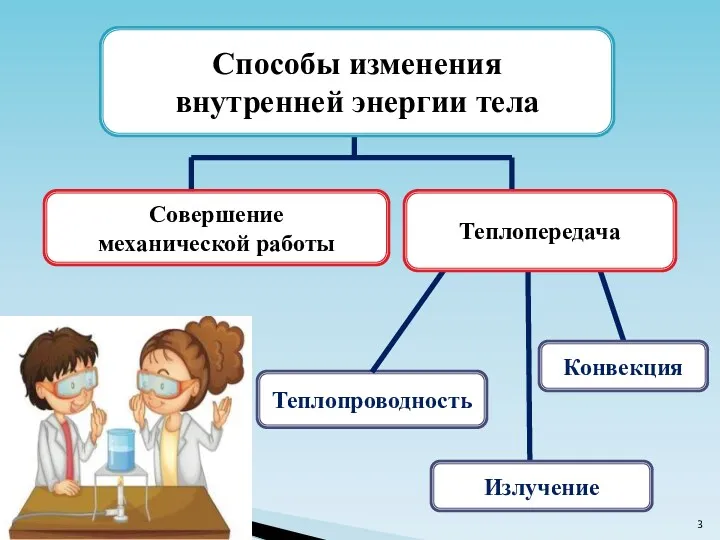
- 3. Теплопроводность Конвекция Способы изменения внутренней энергии тела Излучение Совершение механической работы Теплопередача
- 4. Количество теплоты Теплопередача – это передача внутренней энергии от одного тела к другому в процессе взаимодействия
- 5. Количество теплоты. Единицы количества теплоты. Энергия, которую получает или теряет тело при теплопередаче называется количеством теплоты.
- 6. Q – количество теплоты – мера энергии, переданной телу или отданной телом. Основной единицей измерения ее
- 7. Калория – это количество теплоты, которое необходимо передать 1г воды для ее нагревания на 10С. 1
- 8. Нагреем на двух одинаковых спиртовках разное количество воды, имеющей одинаковую начальную температуру. Одинаковое ли количество теплоты
- 9. Нагреем на двух одинаковых спиртовках равное количество воды, взятой при разных начальных температурах. Одинаковое ли количество
- 10. Нагреем на двух одинаковых спиртовках одинаковое количество воды и масла, взятых при равных начальных температурах. Одинаковое
- 11. Количество теплоты Q зависит: От массы вещества m, От изменения температуры Δt От рода вещества
- 12. Табличные данные
- 13. При каких процессах тело получает энергию? При каких процессах тело отдает энергию?
- 14. Известные вам три состояния вещества (твёрдое, жидкое, газообразное) называются агрегатными состояниями. Молекулы одного и того же
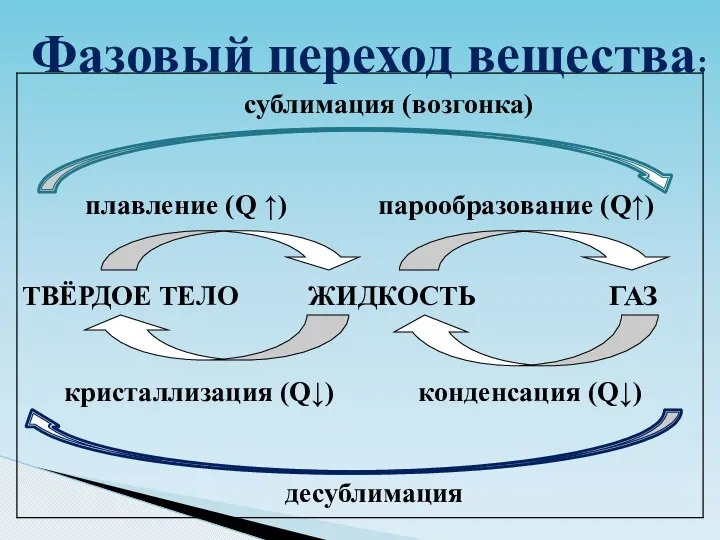
- 15. Фазовый переход вещества: десублимация
- 16. Примеры фазового перехода вещества в природе:
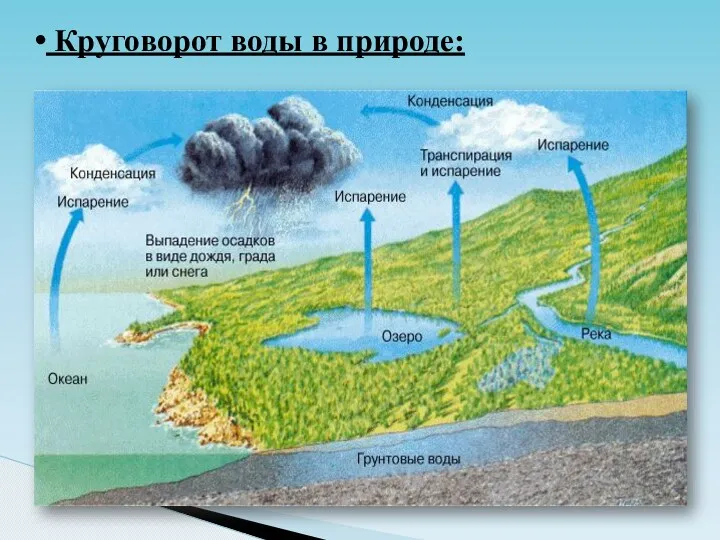
- 17. Круговорот воды в природе:
- 18. Образование осадков: ТУМАН
- 19. Образование осадков: СНЕЖИНКИ, СНЕГ, ГРАД
- 20. Образование осадков:
- 21. Сублимация - переход из твердого вещества в газообразное. Другое название сублимации – вазгонка.
- 22. Что такое сублимация? Сублимация (возгонка) — переход вещества из твёрдого состояния сразу в газообразное, минуя жидкое.
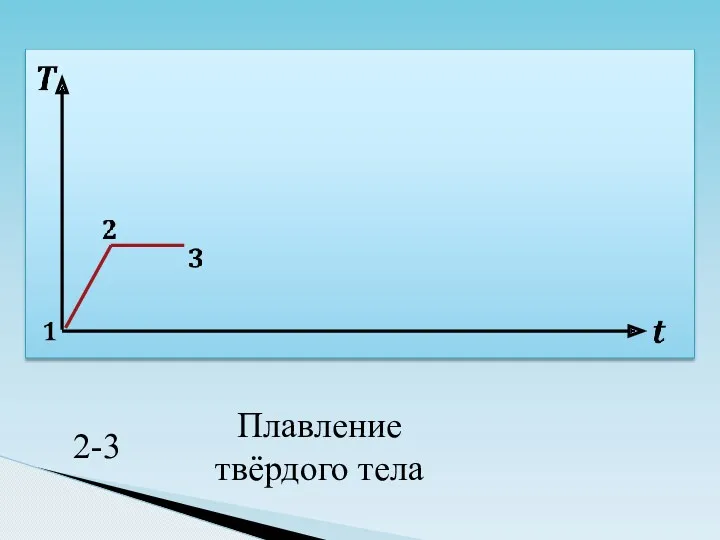
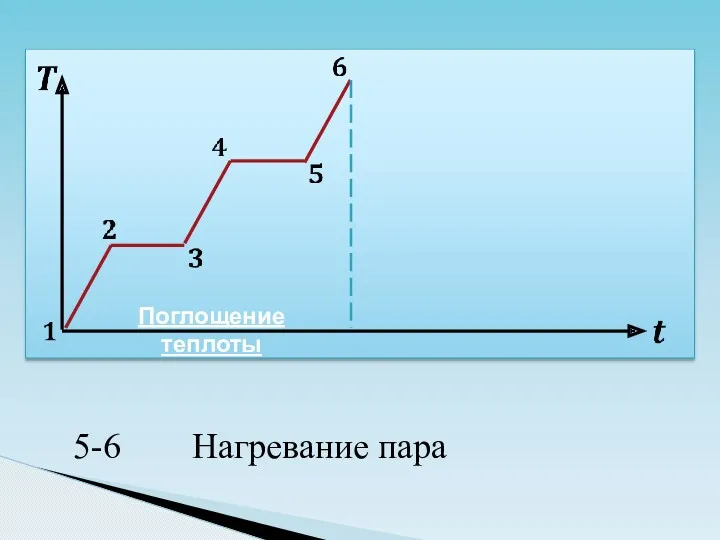
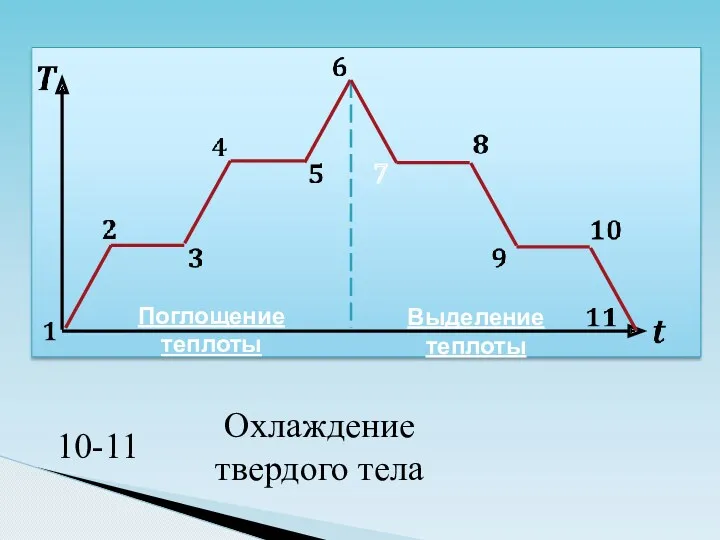
- 27. Поглощение теплоты
- 28. 7 Поглощение теплоты
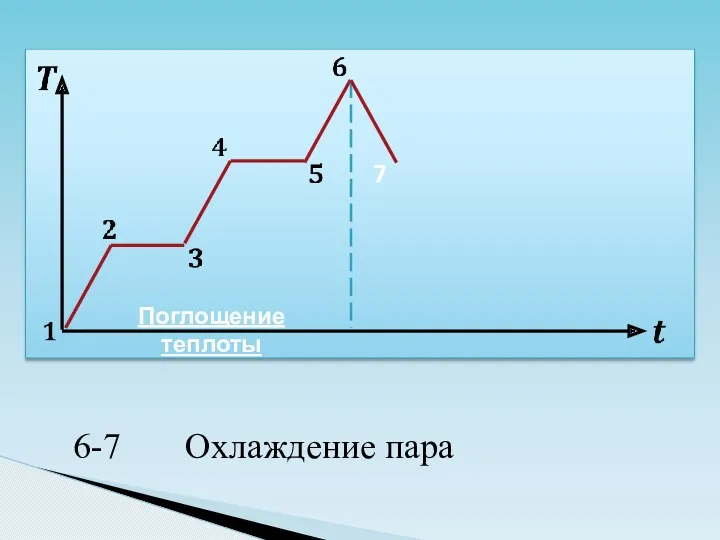
- 29. 7 Поглощение теплоты
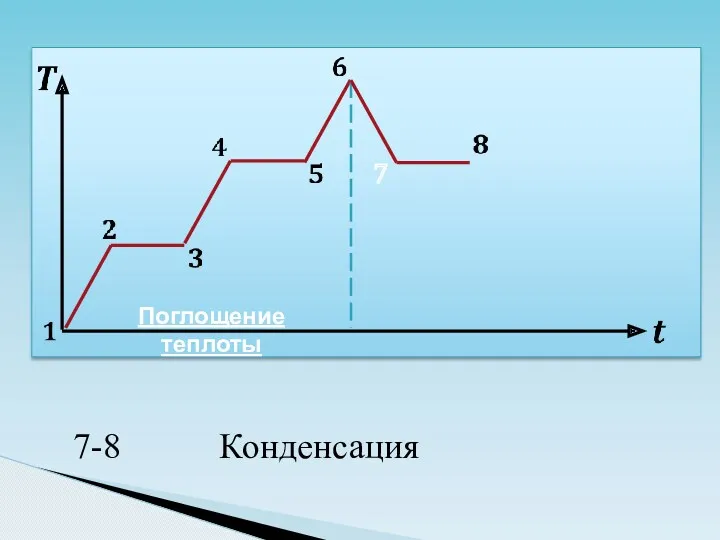
- 30. 7 Поглощение теплоты
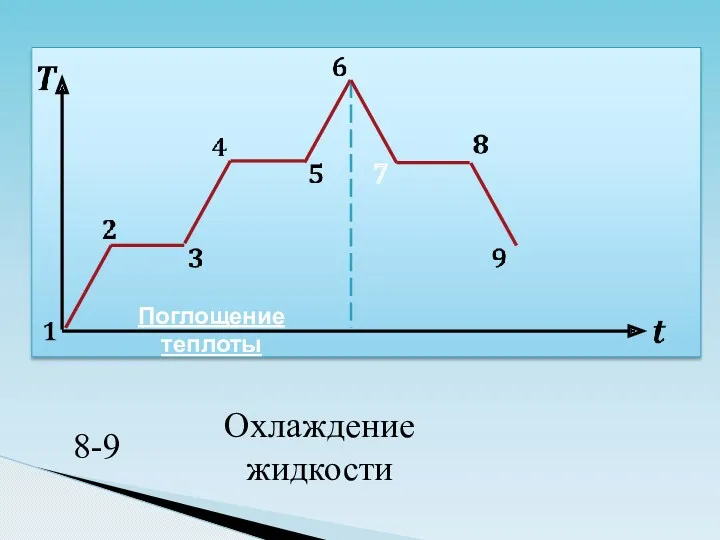
- 31. 7 Поглощение теплоты
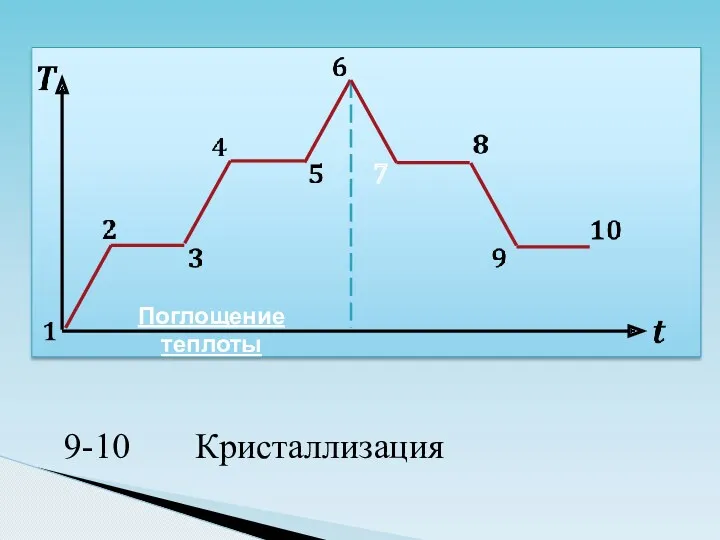
- 32. 7 Поглощение теплоты Выделение теплоты
- 33. Уравнение теплового баланса. Если в изолированной системе происходит теплообмен между несколькими телами, то Q₁+Q₂+Q₃+…+Qn=0
- 34. Закон сохранения массы Масса веществ в начальном состоянии равна массе веществ в конечном.
- 35. Калориметр – прибор для измерения количества теплоты.
- 36. Алгоритм решения задач на уравнение теплового баланса Записать краткое условие задачи. Определить, какие вещества участвуют в
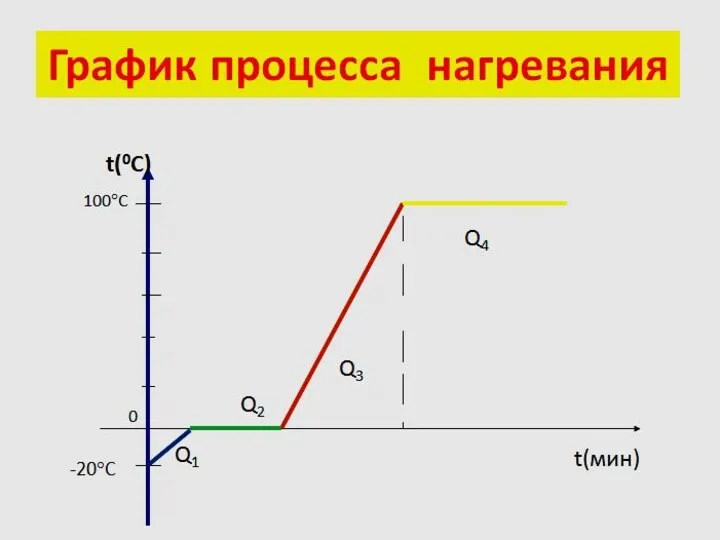
- 37. ЗАДАЧА Какое количество теплоты необходимо, чтобы из льда массой 2 кг, взятого при температуре -10°C, получить
- 39. Какие процессы происходят и с какой последовательностью? 1.Кристаллизация 2.Плавление 3.Нагревание 4.Конденсация 5.Сублимация 6.Охлаждение 7.Возгонка 8.Парообразование
- 40. Процессы 1.Нагревание (чего?) льда ….от-10°C до 0°C 2.Плавление(чего?) льда при 0°C 3.Нагревание(чего?) воды ….от 0°C до100°C
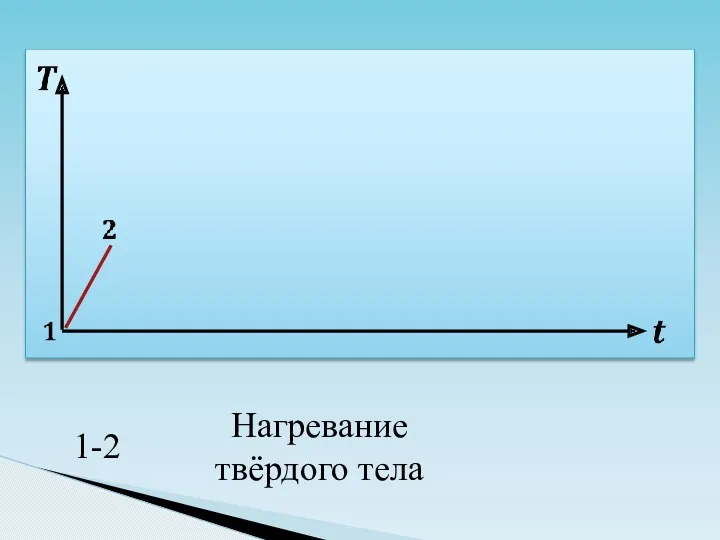
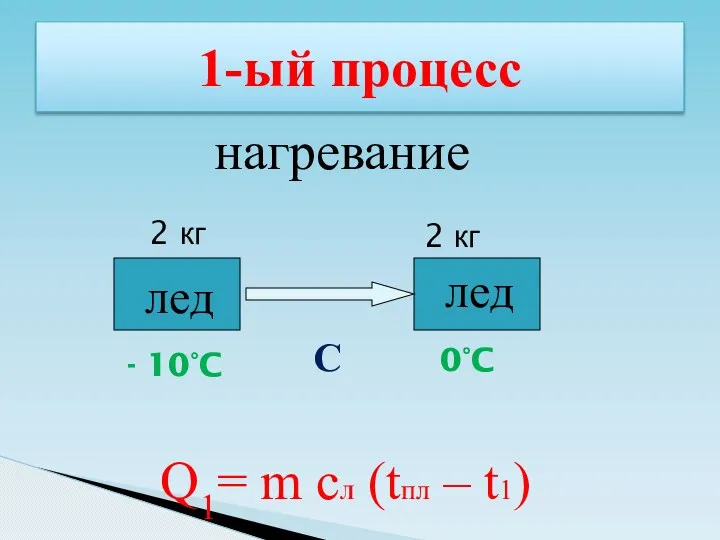
- 41. 1-ый процесс лед лед нагревание - 10°C 0°C С 2 кг 2 кг Q1= m сЛ
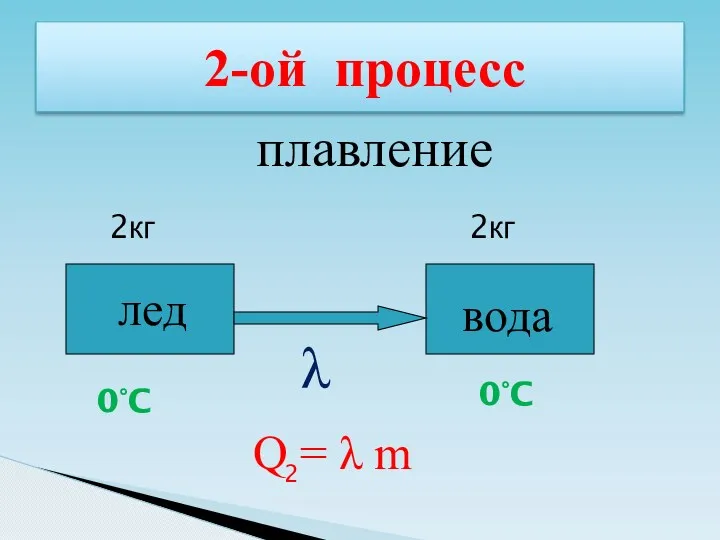
- 42. 2-ой процесс лед вода 0°C 0°C плавление Q = λ m 2кг 2кг λ 2
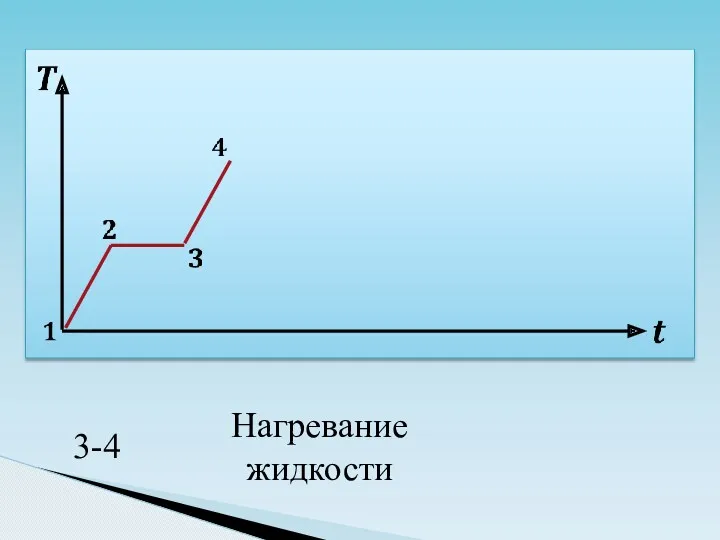
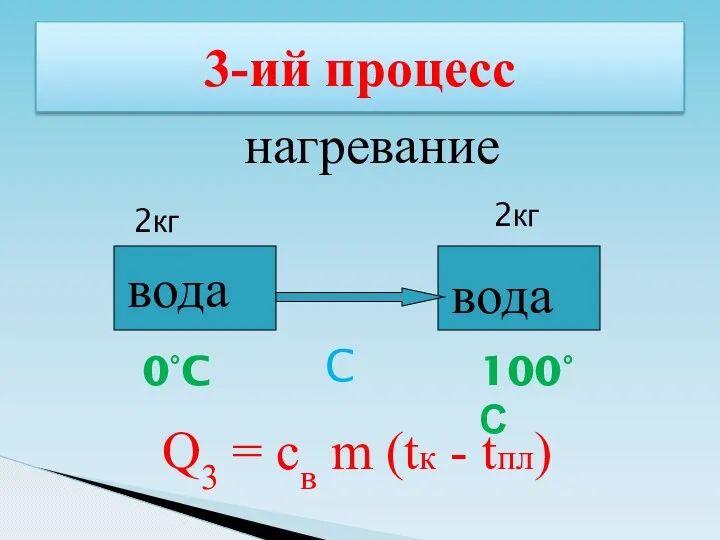
- 43. 3-ий процесс вода вода 0°C нагревание C Q3 = cв m (tк - tпл) 2кг 2кг
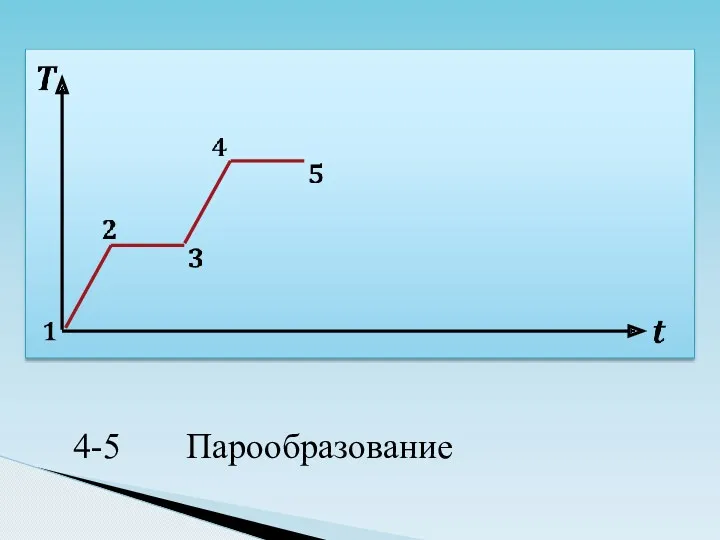
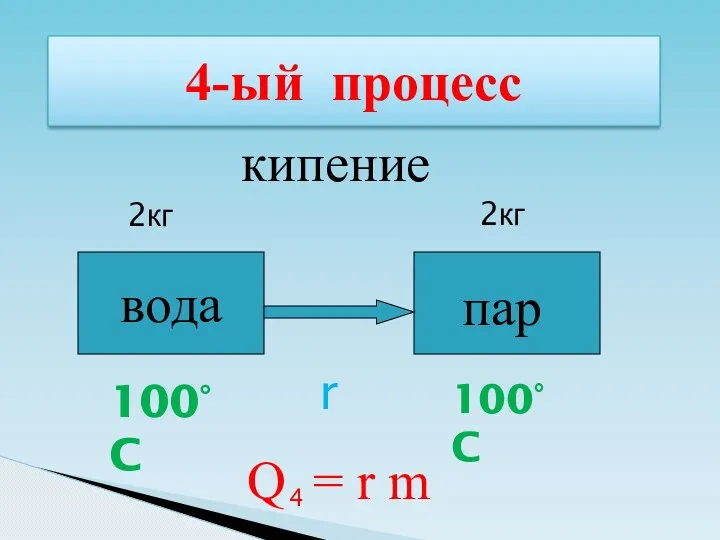
- 44. 4-ый процесс вода 100°C пар 100°C кипение r Q = r m 4 2кг 2кг
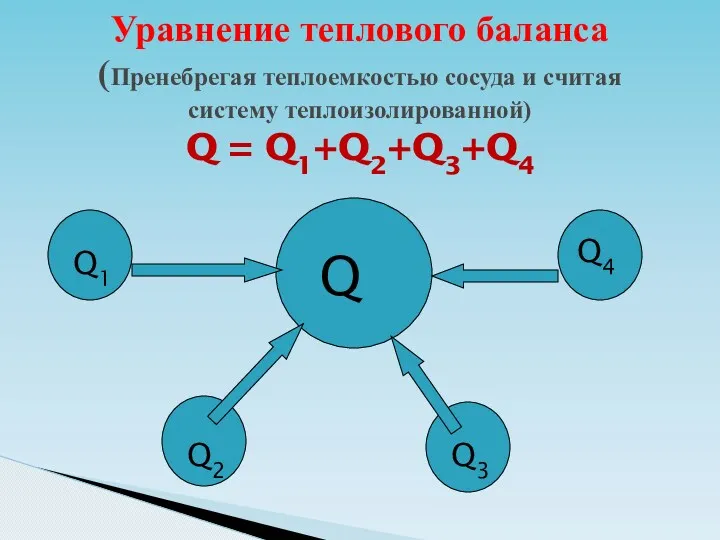
- 45. Уравнение теплового баланса (Пренебрегая теплоемкостью сосуда и считая систему теплоизолированной) Q = Q1+Q2+Q3+Q4 Q1 Q2 Q3
- 47. Скачать презентацию

























 Вільне падіння. Прискорення вільного падіння
Вільне падіння. Прискорення вільного падіння Классификация систем автоматического регулирования
Классификация систем автоматического регулирования Снятие, замена приводного ремня ГРМ Chevrolet Lacetti
Снятие, замена приводного ремня ГРМ Chevrolet Lacetti Молекулярно-кинетические свойства коллоидных систем
Молекулярно-кинетические свойства коллоидных систем Презентация-игра, 7-8 класс
Презентация-игра, 7-8 класс Элементарные частицы
Элементарные частицы История появления квадрокоптеров
История появления квадрокоптеров Делимость электрического заряда
Делимость электрического заряда Урок по теме Электризация тел 8 класс
Урок по теме Электризация тел 8 класс Радиоактивность. Урок физики 9 класс
Радиоактивность. Урок физики 9 класс Сила тока. Единицы силы тока
Сила тока. Единицы силы тока Газораспределительный механизм
Газораспределительный механизм Спидометр
Спидометр Kernfusion in der sonne
Kernfusion in der sonne Глава 5. Пьезоэлектрический эффект и электрострикция
Глава 5. Пьезоэлектрический эффект и электрострикция Агрегатные состояния вещества. Урок в 7 классе
Агрегатные состояния вещества. Урок в 7 классе Презентация Способы изменения внутренней энергии 8 класс
Презентация Способы изменения внутренней энергии 8 класс Элементы теории атомного ядра
Элементы теории атомного ядра Шпонды және шлицты қосылыстар
Шпонды және шлицты қосылыстар методическая разработка раздела курса физики 7 класса Давление
методическая разработка раздела курса физики 7 класса Давление Урок по теме Расчёт пути и времени движения 7 класс
Урок по теме Расчёт пути и времени движения 7 класс Акустика помещений
Акустика помещений Закон всемирного тяготения. Сила тяжести. Невесомость
Закон всемирного тяготения. Сила тяжести. Невесомость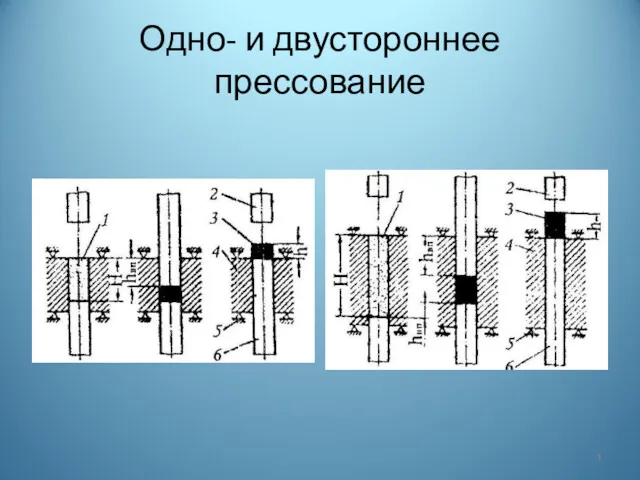 Одно- и двустороннее прессование деталей
Одно- и двустороннее прессование деталей Количество теплоты. Единицы количества теплоты. Удельная теплоемкость. 8 класс
Количество теплоты. Единицы количества теплоты. Удельная теплоемкость. 8 класс сказка физического содержания Добро и зло
сказка физического содержания Добро и зло Понятие о трехфазных цепях
Понятие о трехфазных цепях Основы генерирования и формирования сигналов. Лекция 2
Основы генерирования и формирования сигналов. Лекция 2