Содержание
- 2. Удельная адсорбция (Г) – избыточное количество вещества на единичной площади поверхности раздела фаз N – общее
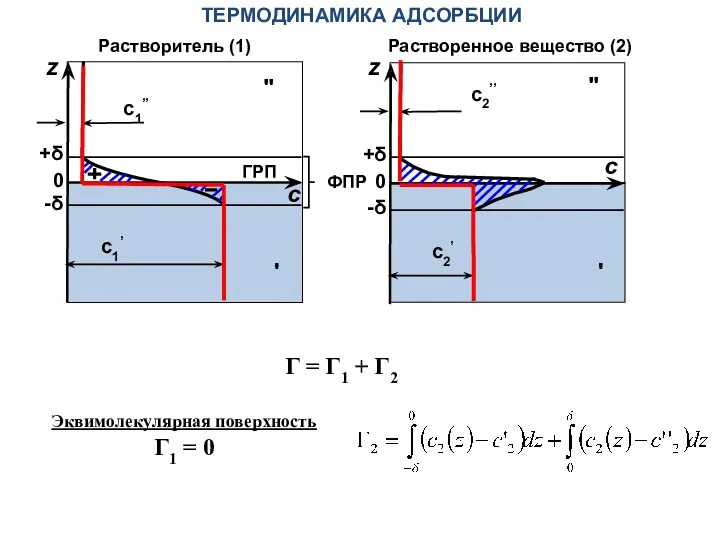
- 3. Растворитель (1) Растворенное вещество (2) z c 0 ' -δ +δ c1’ c1’’ " z c
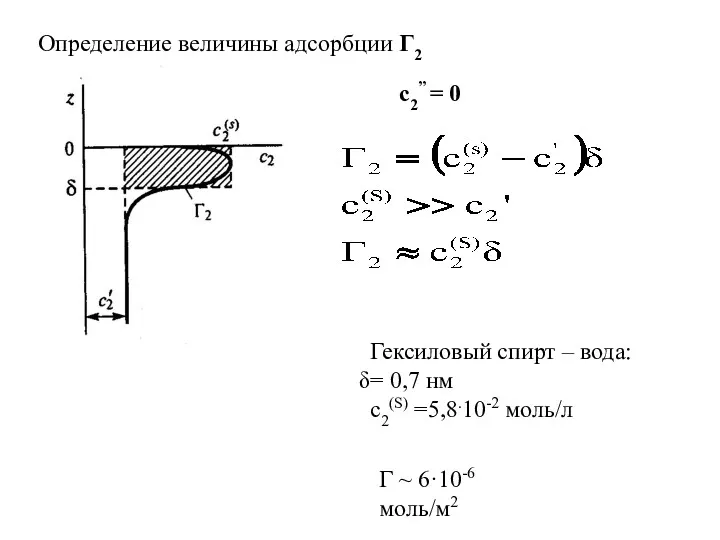
- 4. Гексиловый спирт – вода: = 0,7 нм с2(S) =5,8.10-2 моль/л Γ ~ 6·10-6 моль/м2 c2” =
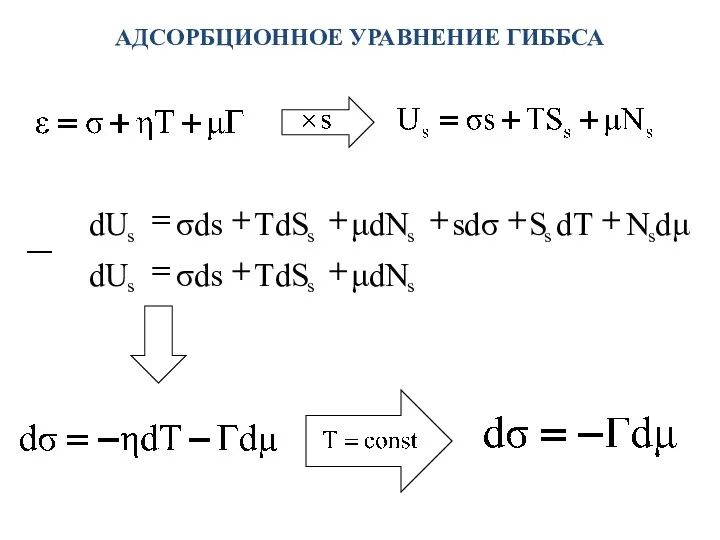
- 5. АДСОРБЦИОННОЕ УРАВНЕНИЕ ГИББСА
- 6. АДСОРБЦИОННОЕ УРАВНЕНИЕ ГИББСА при α = 1
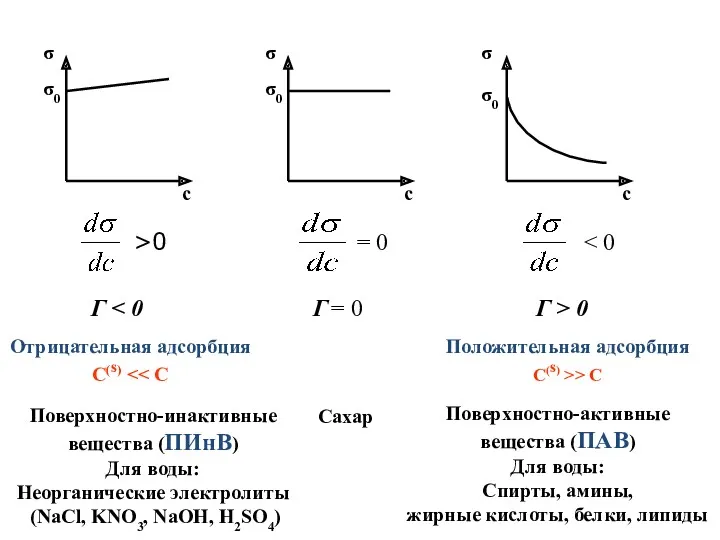
- 7. Отрицательная адсорбция С(s) Поверхностно-инактивные вещества (ПИнВ) Для воды: Неорганические электролиты (NaCl, KNO3, NaOH, H2SO4) Сахар Положительная
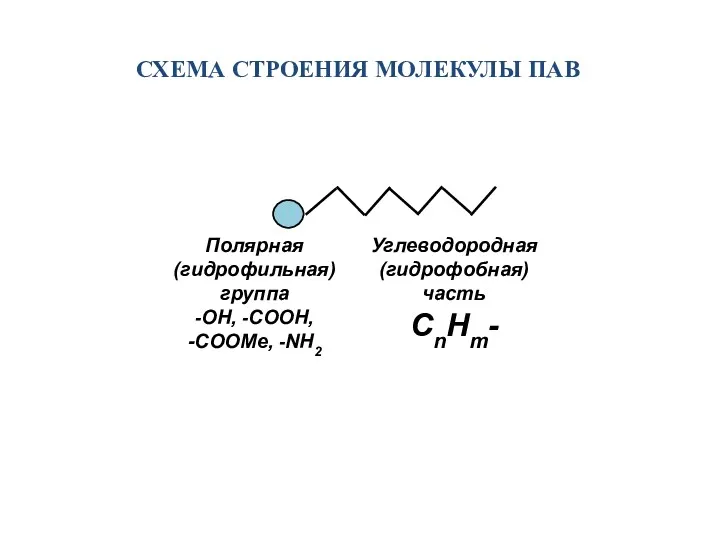
- 8. СХЕМА СТРОЕНИЯ МОЛЕКУЛЫ ПАВ
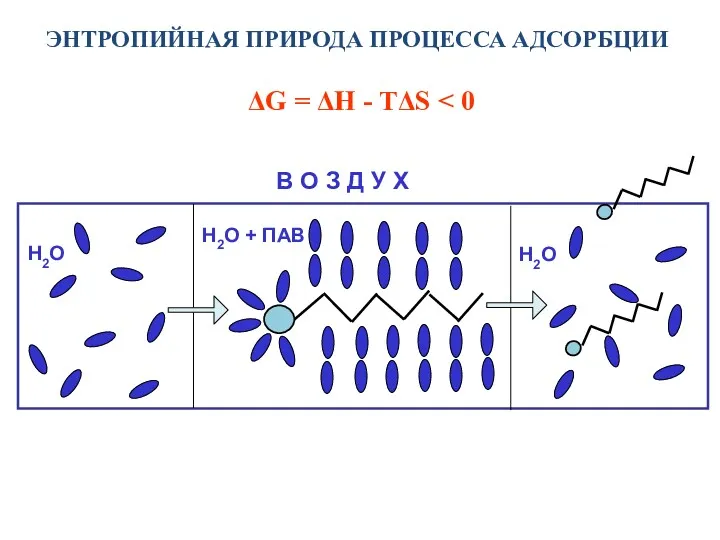
- 9. ЭНТРОПИЙНАЯ ПРИРОДА ПРОЦЕССА АДСОРБЦИИ ΔG = ΔH - TΔS В О З Д У Х
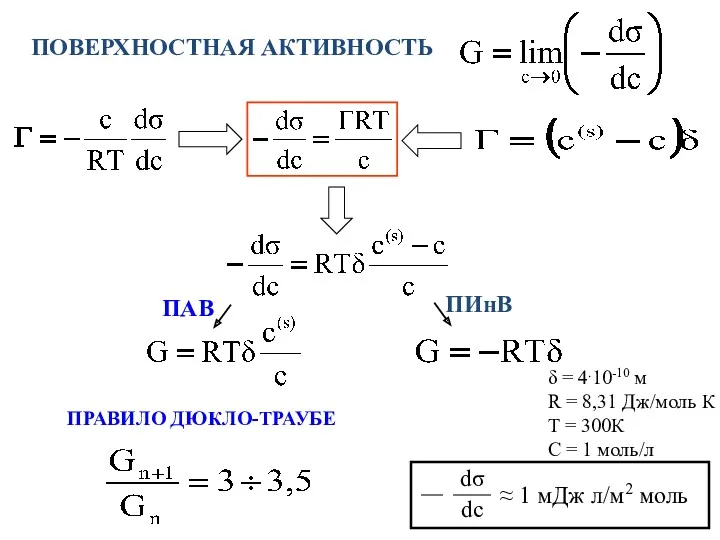
- 10. ПОВЕРХНОСТНАЯ АКТИВНОСТЬ ПРАВИЛО ДЮКЛО-ТРАУБЕ δ = 4.10-10 м R = 8,31 Дж/моль К Т = 300К
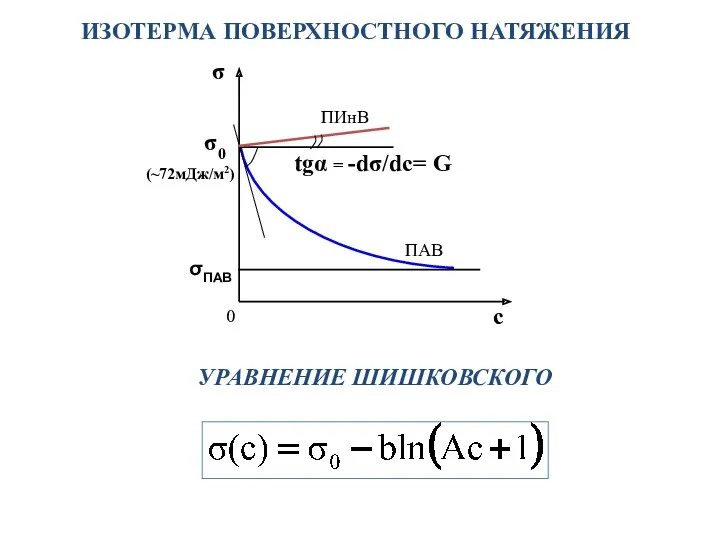
- 11. УРАВНЕНИЕ ШИШКОВСКОГО ИЗОТЕРМА ПОВЕРХНОСТНОГО НАТЯЖЕНИЯ
- 12. АНАЛИЗ УРАВНЕНИЯ ШИШКОВСКОГО (Область Генри) ПРАВИЛО ДЮКЛО-ТРАУБЕ
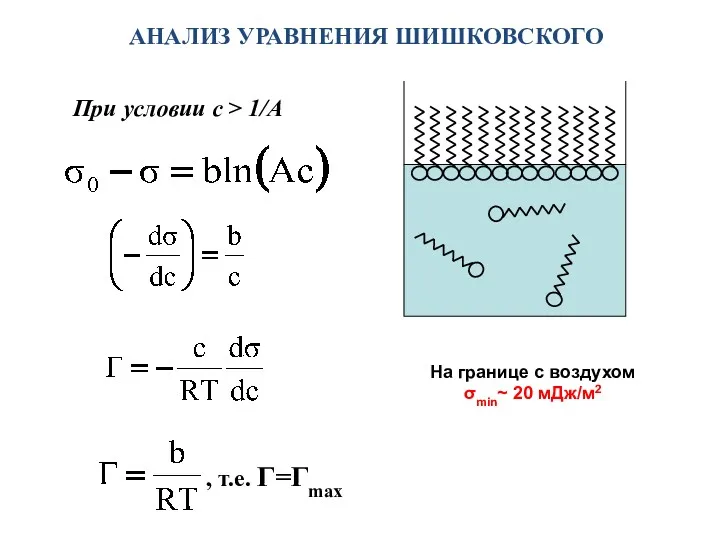
- 13. При условии c > 1/A АНАЛИЗ УРАВНЕНИЯ ШИШКОВСКОГО , т.е. Г=Гmax На границе с воздухом σmin~
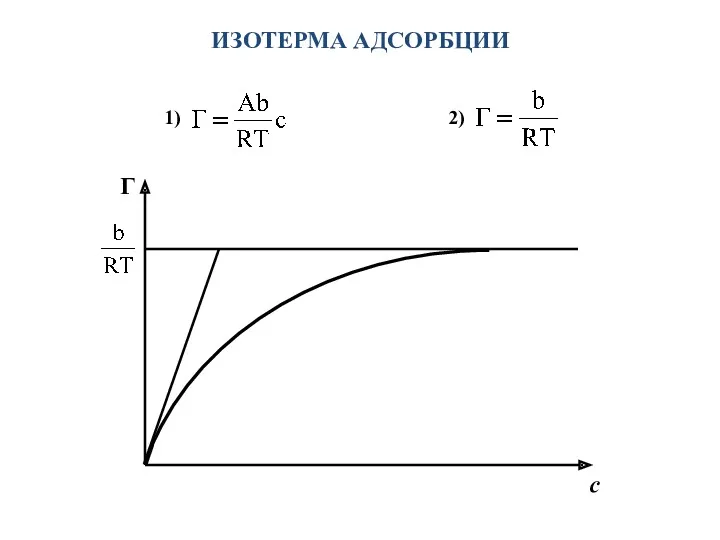
- 14. ИЗОТЕРМА АДСОРБЦИИ
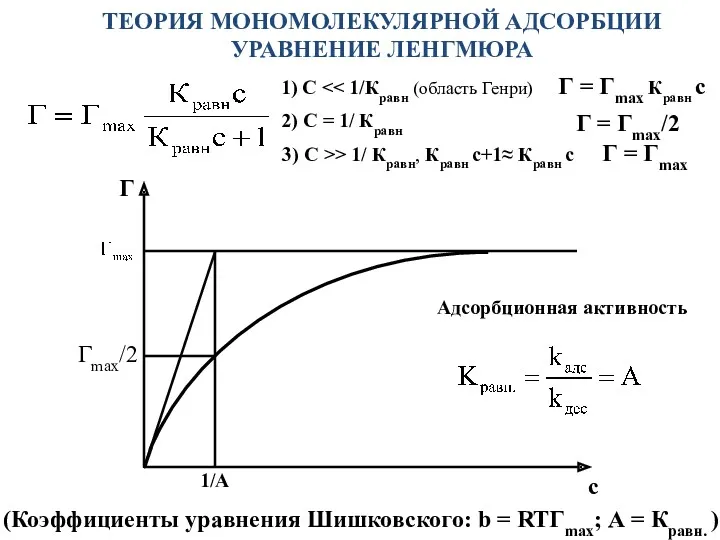
- 15. ТЕОРИЯ МОНОМОЛЕКУЛЯРНОЙ АДСОРБЦИИ УРАВНЕНИЕ ЛЕНГМЮРА (Коэффициенты уравнения Шишковского: b = RTГmax; А = Кравн. )
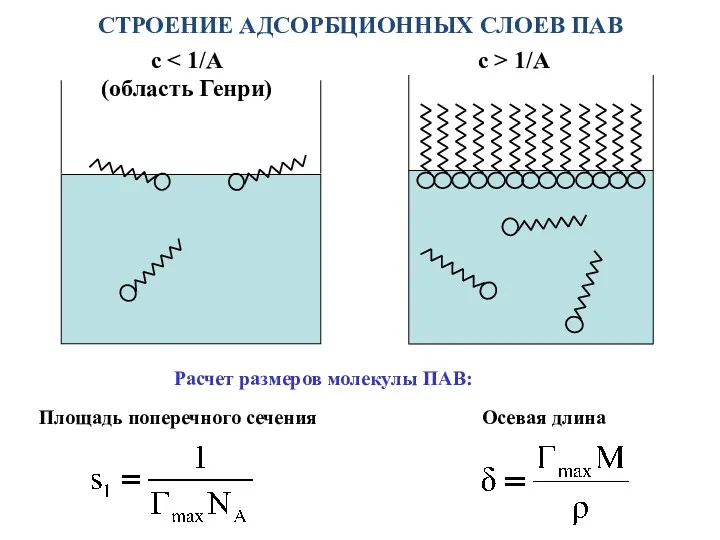
- 16. СТРОЕНИЕ АДСОРБЦИОННЫХ СЛОЕВ ПАВ с (область Генри) с > 1/A Расчет размеров молекулы ПАВ: Площадь поперечного
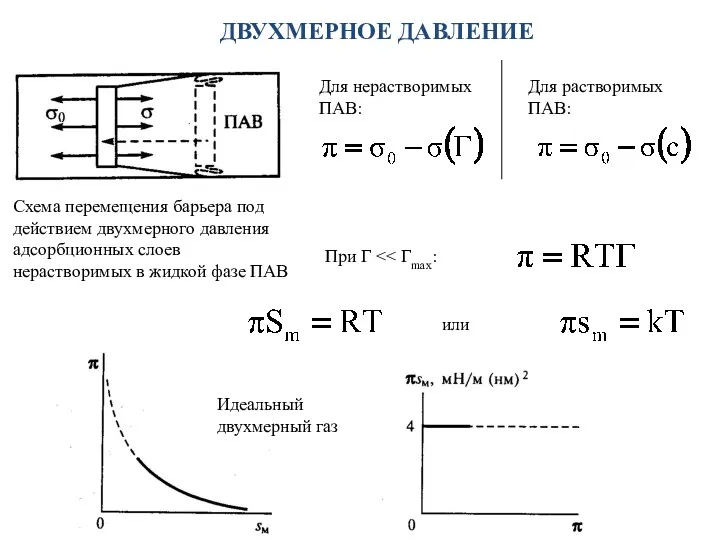
- 17. ДВУХМЕРНОЕ ДАВЛЕНИЕ Схема перемещения барьера под действием двухмерного давления адсорбционных слоев нерастворимых в жидкой фазе ПАВ
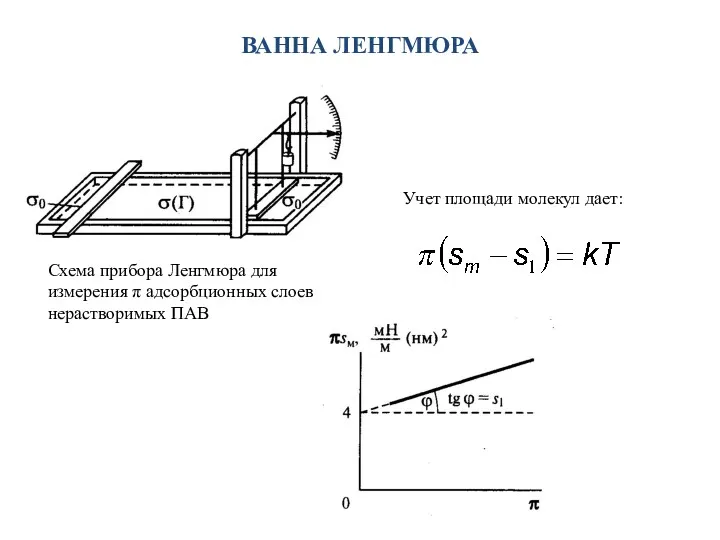
- 18. ВАННА ЛЕНГМЮРА Схема прибора Ленгмюра для измерения π адсорбционных слоев нерастворимых ПАВ Учет площади молекул дает:
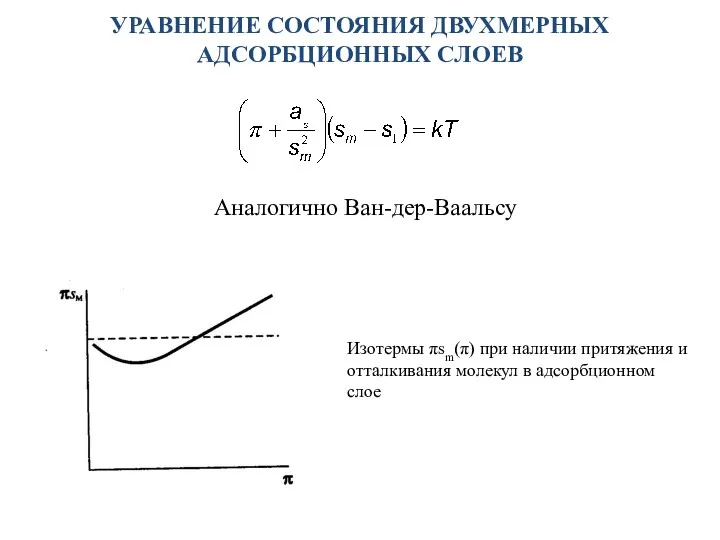
- 19. УРАВНЕНИЕ СОСТОЯНИЯ ДВУХМЕРНЫХ АДСОРБЦИОННЫХ СЛОЕВ Аналогично Ван-дер-Ваальсу Изотермы πsm(π) при наличии притяжения и отталкивания молекул в
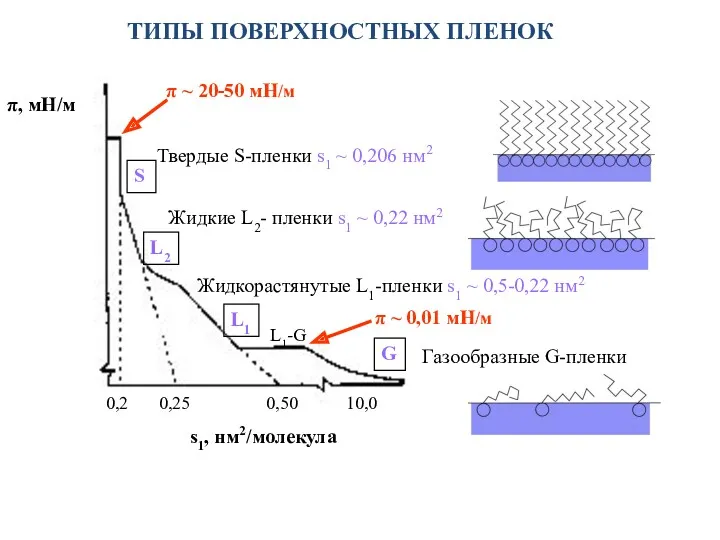
- 20. ТИПЫ ПОВЕРХНОСТНЫХ ПЛЕНОК π, мН/м 0,2 0,25 0,50 10,0 s1, нм2/молекула S L2 L1 L1-G G
- 21. СТРУКТУРНАЯ ФОРМУЛА ФОСФОХОЛИНА: Ethanaminium, 2-[[[(2,2-dipentadecyl-1,3-dioxolan-4-yl)methoxy]hydroxyphosphinyl]oxy]-N,N,N-trimethyl-, inner salt
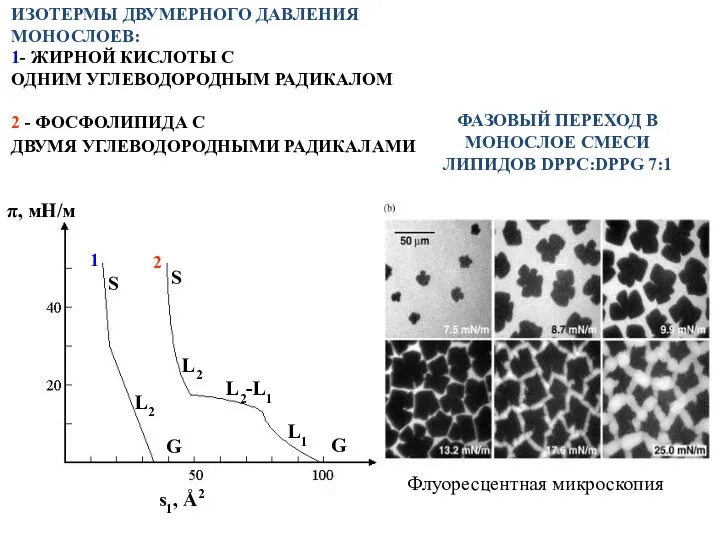
- 22. ИЗОТЕРМЫ ДВУМЕРНОГО ДАВЛЕНИЯ МОНОСЛОЕВ: 1- ЖИРНОЙ КИСЛОТЫ С ОДНИМ УГЛЕВОДОРОДНЫМ РАДИКАЛОМ 2 - ФОСФОЛИПИДА С ДВУМЯ
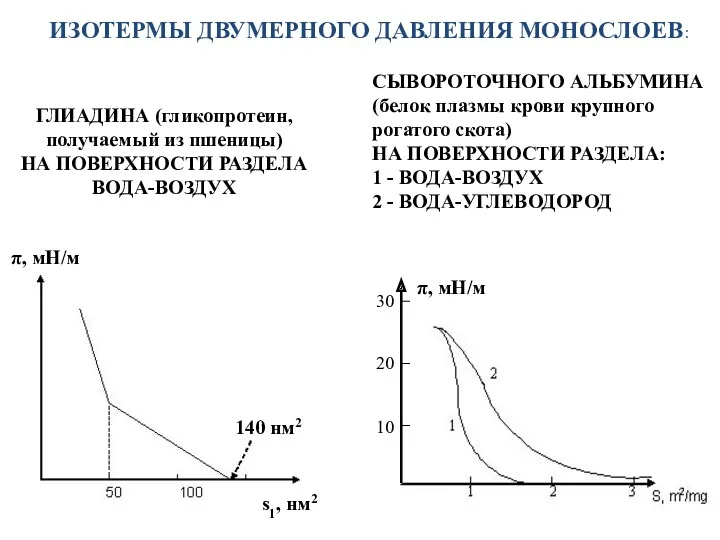
- 23. ИЗОТЕРМЫ ДВУМЕРНОГО ДАВЛЕНИЯ МОНОСЛОЕВ: ГЛИАДИНА (гликопротеин, получаемый из пшеницы) НА ПОВЕРХНОСТИ РАЗДЕЛА ВОДА-ВОЗДУХ СЫВОРОТОЧНОГО АЛЬБУМИНА (белок
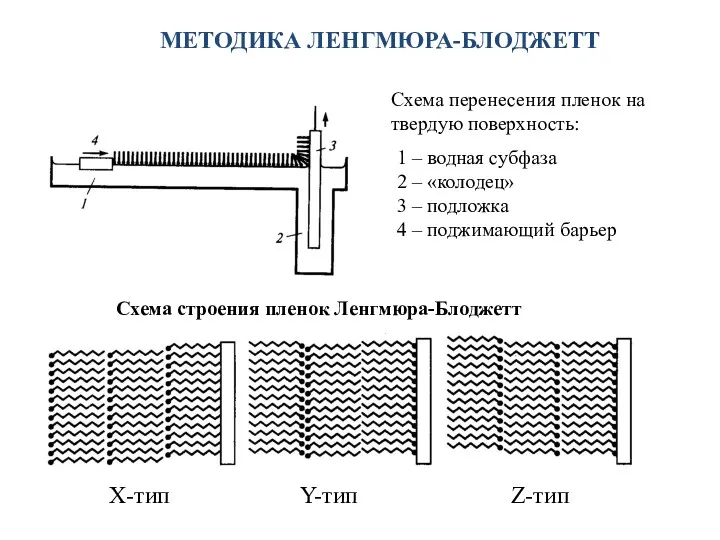
- 24. МЕТОДИКА ЛЕНГМЮРА-БЛОДЖЕТТ Схема перенесения пленок на твердую поверхность: 1 – водная субфаза 2 – «колодец» 3
- 25. АДСОРБЦИЯ НА ГРАНИЦЕ ДВУХ КОНДЕНСИРОВАННЫХ ФАЗ Правило уравнивания полярностей Ребиндера: Для границы 2-х конденсированных фаз поверхностно-активным
- 26. АДСОРБЦИЯ ИЗ РАСТВОРОВ НА ТВЕРДОЙ ПОВЕРХНОСТИ С0 – исходная концентрация ПАВ; С равн – равновесная концентрация
- 28. Скачать презентацию



![СТРУКТУРНАЯ ФОРМУЛА ФОСФОХОЛИНА: Ethanaminium, 2-[[[(2,2-dipentadecyl-1,3-dioxolan-4-yl)methoxy]hydroxyphosphinyl]oxy]-N,N,N-trimethyl-, inner salt](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/269153/slide-20.jpg)


 Плавление и отвердевание кристаллических тел
Плавление и отвердевание кристаллических тел Дополнительный материал по физике для 8 класса.
Дополнительный материал по физике для 8 класса. Линзы. Построение изображений в линзах
Линзы. Построение изображений в линзах Динамика. Основные понятия
Динамика. Основные понятия Исследовательская работа Посудомоечная машина
Исследовательская работа Посудомоечная машина Ток кескіш. Токтың сатылы қорғанысы
Ток кескіш. Токтың сатылы қорғанысы Урок по физике в 7 классе Выталкивающая сила
Урок по физике в 7 классе Выталкивающая сила Свайные фундаменты. Классификация. (Лекция 6)
Свайные фундаменты. Классификация. (Лекция 6) Emission spectrum of H
Emission spectrum of H Основы массообмена
Основы массообмена Сила и сила трения
Сила и сила трения Измерение аберраций оптических систем
Измерение аберраций оптических систем Физико - математическая игра Эрудит
Физико - математическая игра Эрудит Характеристика и конструкция швейных машин и полуавтоматов (пуговичные полуавтоматы)
Характеристика и конструкция швейных машин и полуавтоматов (пуговичные полуавтоматы) Расчет цепи постоянного тока
Расчет цепи постоянного тока Типы оптических спектров. Спектральный анализ
Типы оптических спектров. Спектральный анализ Источники и приемники оптического излучения
Источники и приемники оптического излучения Город будущего
Город будущего авторская программа Средства связи
авторская программа Средства связи Тепловые машины
Тепловые машины История развития энергетики. Циклы этногенеза
История развития энергетики. Циклы этногенеза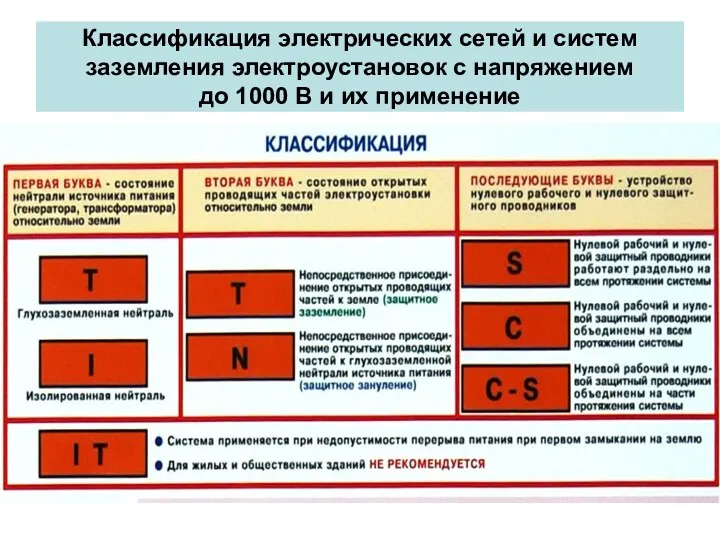 Классификация электрических сетей и систем заземления электроустановок с напряжением до 1000 В и их применение
Классификация электрических сетей и систем заземления электроустановок с напряжением до 1000 В и их применение Механикалық толқынның
Механикалық толқынның Неразъемные соединения
Неразъемные соединения КПД простых механизмов. 7 класс
КПД простых механизмов. 7 класс Неразъемные соединения
Неразъемные соединения Модель атома Резерфорда. Атомные спектры. Постулаты Бора. Опыт Франка и Герца. Элементарная боровская теория водородного атома
Модель атома Резерфорда. Атомные спектры. Постулаты Бора. Опыт Франка и Герца. Элементарная боровская теория водородного атома Импульс тела. Закон сохранения импульса. 9-й класс
Импульс тела. Закон сохранения импульса. 9-й класс