Содержание
- 2. Элементарлы бөлшектердің қасиеттері Электрон – теріс зарядталған, массасы ≈ 0,511 МэВ элементар бөлшек, спины 0,5 ћ.
- 3. Сутегі және оның изотроптары Сутегінің 3 изотоптары бар: протий, дейтерий және тритий. H D T Массасы
- 4. Дейтерий және тритий Массасы 2-ге тең ауыр сутегі, оны дейтерий деп атайды. Оны 2Н символымен белгілейді
- 5. Микроәлемнің заңдары Нейтрондар еркін кезде протон, электрон және антинейтриноға тарайды. Неге лептондардың жұптары туындайды? Сонда антинейтрино
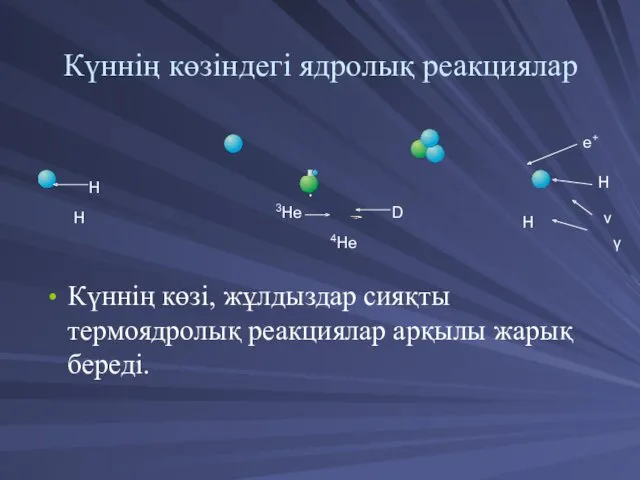
- 6. Күннің көзіндегі ядролық реакциялар Күннің көзі, жұлдыздар сияқты термоядролық реакциялар арқылы жарық береді. H H D
- 7. Жоғары энергиясы бар протондар жақындағанда, олардың біреуі протон, екіншісі позитрон және нейтриноға айналуы мүмкін. Сол кезде
- 8. π-мезон Ядродағы протондар мен нейтрондар көп әсер ететін бөліктермен - шамамен электроннан 270 рет ауыр π-мезондармен
- 9. Мюон және ауыр лептон Мюон электронға қатты ұқсайды, бірақ 200 есе ауыр болып келеді.Сонымен қатар мюон
- 10. Ядронның құрылымы Элементарлы бөлшектердің кестесін құру кезінде барлық топтастардың негізінде, кварк топтастары ретінде - (-⅓, -⅔,
- 11. Атом моделі 9. 9.1.
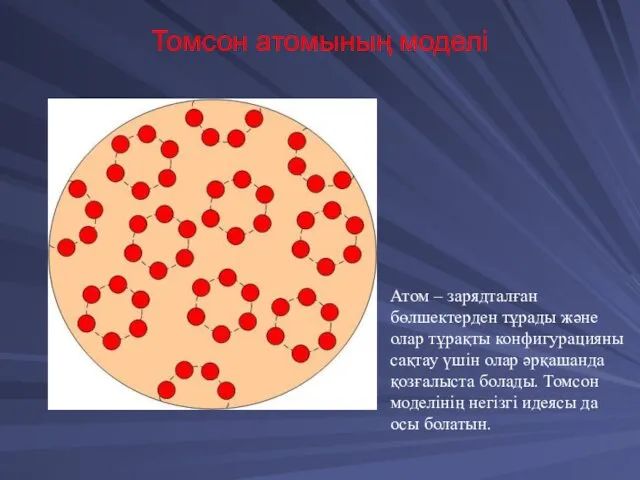
- 12. Томсон атомының моделі Атом – зарядталған бөлшектерден тұрады және олар тұрақты конфигурацияны сақтау үшін олар әрқашанда
- 13. Нагаоке атомның моделі Нагаоке атомның моделі – «сатурнтәрізді». Мұндағы электрондар оң зарядталған денені айналатын шеңбер. Нагаоке
- 14. Планеталық атом моделі Ескі атом моделі – планеталық болған. Көптеген оқымыстылар осы атом моделі жайлы айтқан
- 15. Атомның құрылымы. Радиоактивтіліктің ашылуы. 9. 9.2.
- 16. Радиоактивтіліктің ашылуы 1 март 1896 ж.
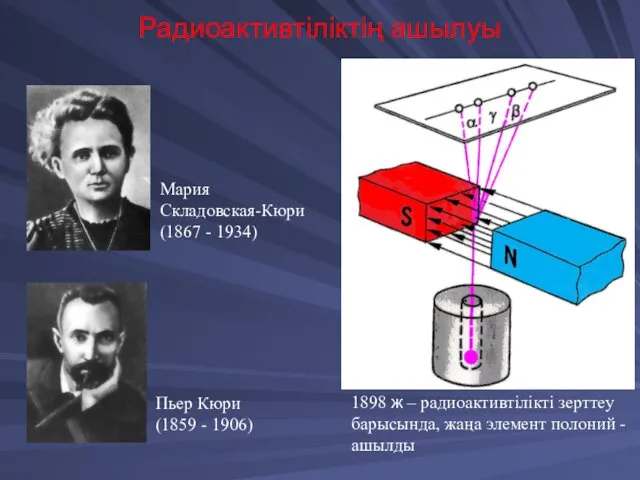
- 17. Радиоактивтіліктің ашылуы 1898 ж – радиоактивтілікті зерттеу барысында, жаңа элемент полоний - ашылды
- 18. Резерфордтың α-бөлшектердің таралуы жайлы тәжірибелері 9.3.
- 19. Эрнест Резерфорд Жаңа Зеландияда фермер жанұясында 1871 жылы өмірге келген. 1885 жылдан бастап ол Кавендиш лабораториясында
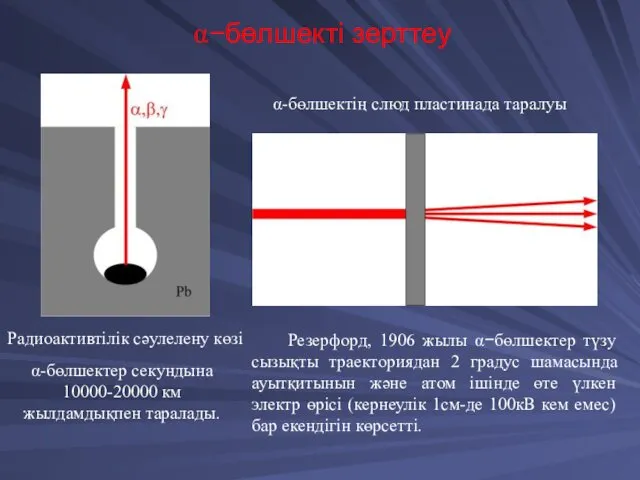
- 20. α−бөлшекті зерттеу α-бөлшектер секундына 10000-20000 км жылдамдықпен таралады. α-бөлшектің слюд пластинада таралуы Резерфорд, 1906 жылы α−бөлшектер
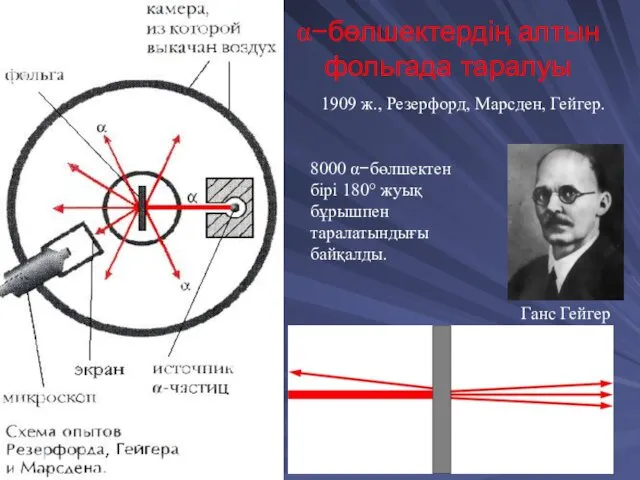
- 21. α−бөлшектердің алтын фольгада таралуы 1909 ж., Резерфорд, Марсден, Гейгер. 8000 α−бөлшектен бірі 180° жуық бұрышпен таралатындығы
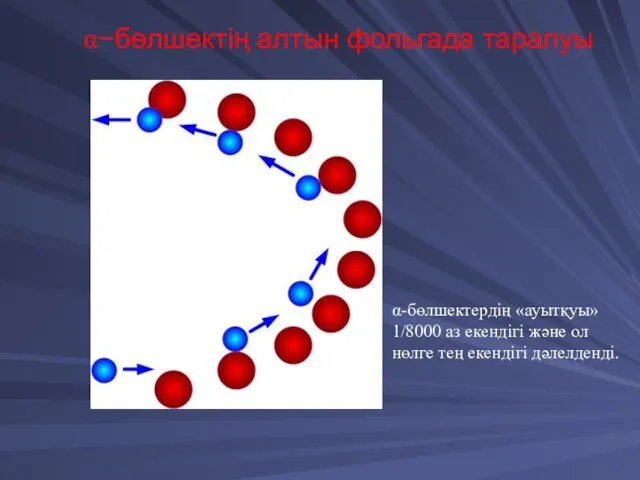
- 22. α−бөлшектің алтын фольгада таралуы α-бөлшектердің «ауытқуы» 1/8000 аз екендігі және ол нөлге тең екендігі дәлелденді.
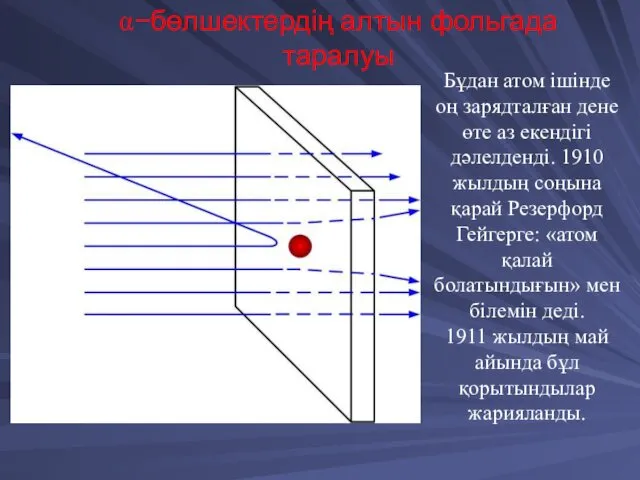
- 23. α−бөлшектердің алтын фольгада таралуы Бұдан атом ішінде оң зарядталған дене өте аз екендігі дәлелденді. 1910 жылдың
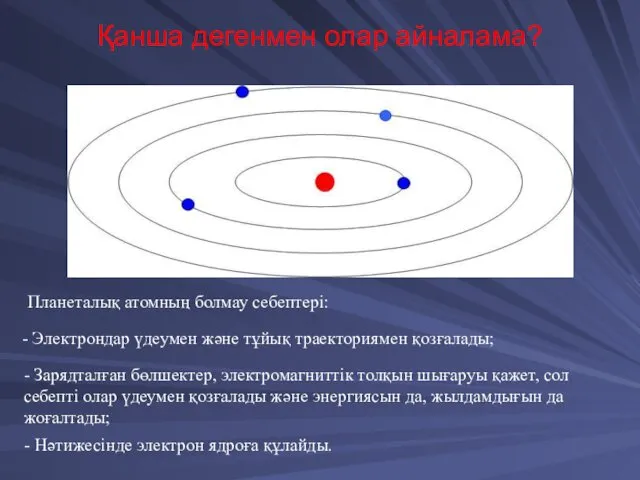
- 24. Қанша дегенмен олар айналама? Планеталық атомның болмау себептері: - Электрондар үдеумен және тұйық траекториямен қозғалады; -
- 25. Бор-Зоммерфельдтің квантталу туралы ережелері 9.4.
- 26. Атом және квантың ұқсастығы неде? 1. Резерфордтың планеталық атомының бар екендігін дәлелдеу үшін, Бор квант қасиеттерін,
- 27. Бор – Зоммерфельдтың квантталу ережелері Планкқа сәйкес жарықтың сәулеленуі порция порциямен, яғни квантпен шығады және энергия
- 28. Бордың сутегі атомы жайлы теориясы 6.5.
- 29. Бордың сутегі ұқсас атомдарының теориясы Электрон ядроны айнала дөңгелек орбита бойымен қозғалады. Оған ядро жағынан кулондық
- 30. мұндағы V - электронның жылдамдығы, R – орбита радиусы мұнда Z - ядро заряды. Ньютонның екінші
- 31. Бордың ұсынысына сүйене отырып, классикалық механикадағы барлық мүмкін болатын электрондардың тек орбиталық импульс моменті бар электрондар
- 32. Бордың сутегі ұқсас атомдарының теориясы Сонда, сутегі ұқсас атомдардың электрондарының энергиясы көптеген дискретті мәндер алуы мүмкін
- 33. Орбита радиуысының n кез келген мәндегі күйін Бордың бірінші орбита күйі арқылы өрнектеген ыңғайлы: Бордың сутегі
- 34. Сутегі атомның энергетикалық теңдеуінің кестесі
- 35. Бордың постулаттары 1.Атом кейбір дискретті энергия мәндерде ғана тұрақты дискретті күйде бола алады. Тұрақты күйде атом
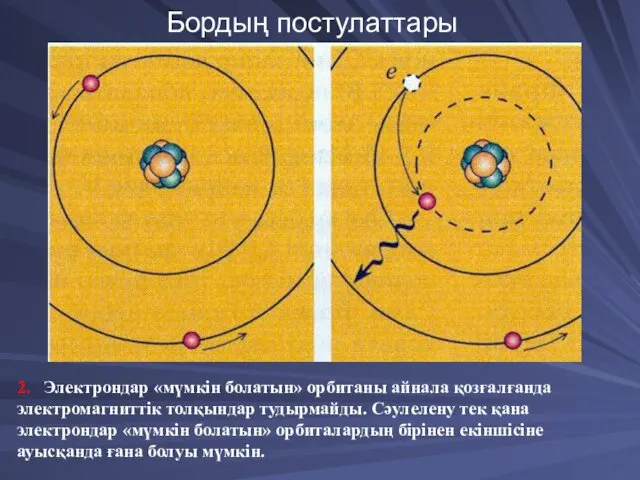
- 36. Бордың постулаттары 2. Электрондар «мүмкін болатын» орбитаны айнала қозғалғанда электромагниттік толқындар тудырмайды. Сәулелену тек қана электрондар
- 37. Бордың постулаттары 3. Сонымен, атом энергияларының шашырауы және жұтылуы порция порция болып шығады, сонымен бірге (энергия
- 38. Атом электрондары жұтылғанда олар сыртқы орбитадан ішкі ядродан алыс орналасқан орбитаға өтеді. Ал олар кері қарай
- 39. Сутегі атомына Бордың тәжірибелік дәлдемелері. 6.6.
- 40. Оптикалық спектр атомдармен шығарылады
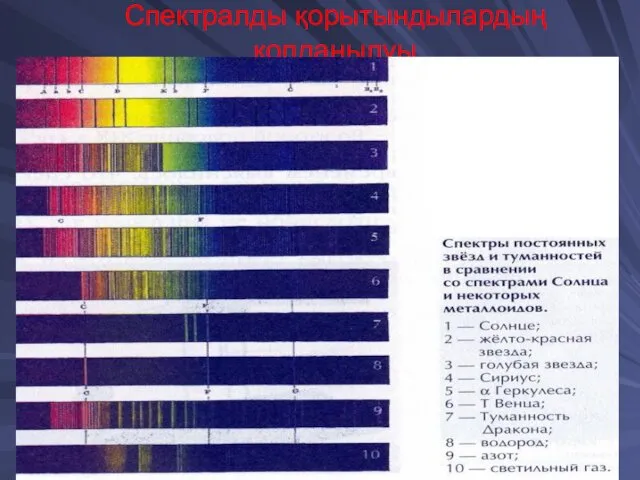
- 41. Спектралды қорытындылардың қолданылуы
- 42. Қалай тексеру қажет? Бальмер формуласын толықтырған Ридбергтің формуласы: Бордың теориясына сәйкес Сутегі үшін s = 1,
- 43. Франк және Герц тәжірибелері. Дж. Франк және Г. Герц, 1913 ж. Шыны колба сынаппен толтырылған. К
- 45. Скачать презентацию
































 Фотоэффект құбылысы
Фотоэффект құбылысы Our knowledge in the field of fundamental physics
Our knowledge in the field of fundamental physics лабораторная работа №1 10 класс
лабораторная работа №1 10 класс Цепная реакция деления ядер. Ядерный реактор
Цепная реакция деления ядер. Ядерный реактор Электрический ток в жидкостях
Электрический ток в жидкостях Облаштування бульдозерів і визначення їх продуктивності
Облаштування бульдозерів і визначення їх продуктивності Датчик числа оборотов G28
Датчик числа оборотов G28 Экзотические и перспективные виды электростанций
Экзотические и перспективные виды электростанций Электромагнитная совместимость. Электромагнитные помехи. (Занятие 2)
Электромагнитная совместимость. Электромагнитные помехи. (Занятие 2) Основы технической термодинамики
Основы технической термодинамики Нанотехнологии: фантазии или реальность?
Нанотехнологии: фантазии или реальность? Магниторазведка. Магнитометры
Магниторазведка. Магнитометры Құрамында галогендер бар мономерлер. Винилхлорид пен винилфторидті алу жолдары. Поливинилхлоридты өндіру
Құрамында галогендер бар мономерлер. Винилхлорид пен винилфторидті алу жолдары. Поливинилхлоридты өндіру Термоядерная реакция
Термоядерная реакция Метрологія, як наука про вимірювання. Державні метрологічні організації. Фізичні величини та їх одиниці
Метрологія, як наука про вимірювання. Державні метрологічні організації. Фізичні величини та їх одиниці Презентация по теме Излучения и спектры 11 класс
Презентация по теме Излучения и спектры 11 класс Кинематика передач
Кинематика передач Кристаллооптика
Кристаллооптика Термодинамика екінші бастамасы
Термодинамика екінші бастамасы Основы технической механики. Связи и их реакции. Тема 2
Основы технической механики. Связи и их реакции. Тема 2 Термодинамические циклы двигателей внутреннего сгорания (ДВС) и газотурбинных установок (ГТУ)
Термодинамические циклы двигателей внутреннего сгорания (ДВС) и газотурбинных установок (ГТУ) Basics of thermodynamics & kinetics
Basics of thermodynamics & kinetics Робототехника. Робот-дворник
Робототехника. Робот-дворник Регуляторы швейной машины
Регуляторы швейной машины Теория симметричного вибратора
Теория симметричного вибратора Солнечная батарея и ее использование в физике
Солнечная батарея и ее использование в физике Линзы. Оптические приборы
Линзы. Оптические приборы Electrical Charges
Electrical Charges