Слайд 2

1. Описание эффекта
Эффе́ктом Джо́уля — То́мсона называют изменение температуры газа или жидкости при стационарном адиабатическом дросселировании — медленном протекании газа
под действием постоянного перепада давлений сквозь дроссель (пористую перегородку). Назван в честь открывших его Джеймса Джоуля и Уильяма Томсона. Данный эффект является одним из методов получения низких температур.
Слайд 3
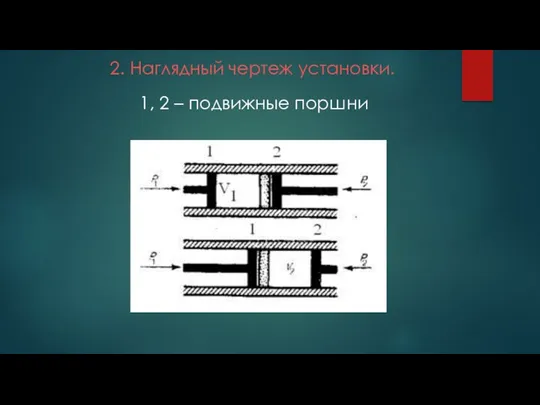
2. Наглядный чертеж установки. 1, 2 – подвижные поршни
Слайд 4

3. Термодинамика в эффекте.
Термодинамика процесса Джоуля-Томсона
1) Интегральный и дифф.
Эффекты
Запишем для левой и правой части газа уравнение Бернулли
i₁+U²₁/2=i₂+U²₂/2 , где величины
U²₁<= i₁ и U²₂<=i₂=>I₁=I₂ (1)
Имеем равенство энтальпий:
* I₁= U₁+p₁V₁= Cv*T₁- (a/T₁)+p₁V₁ (2)
- тут подразумевается, что в левой части цилиндра – газ Ван-Дер-Ваальса
I₂=U₂+p₂V₂= Cv*T ₂+RT₂= Cp*T₂ (3)
Воспользуемся равенством (1) и выражениями (2) и (3)=> =>(R + Cv)T= CpT₂= CvT₁- (a/T₁)+p₁V₁ , где (p₁+(a/V²₁))(V-b)= RT, тогда запишется след. Т₂ -Т₁= ((Rb/V₁-b)*T₁- (2a/V₁))* (1/R+Cv)
Обозначим за величину Tинв= (2a/ Rb) * ( V₁-b/ V₁), тогда
Т ₁< Tинв – охлаждение. Т ₁>Tинв – нагрев
Слайд 5

Некоторые промежуточные выкладки
а) Вывод уравнения внутренней энергии газа Ван-Дер-Ваальса




 Инфрақызыл и раман спектроскопия
Инфрақызыл и раман спектроскопия Потенциал и работа электростатического поля. Связь напряженности с потенциалом
Потенциал и работа электростатического поля. Связь напряженности с потенциалом ТО и ТР заднего моста
ТО и ТР заднего моста Естественное и искусственное освещение. Лекция 5
Естественное и искусственное освещение. Лекция 5 Изменение агрегатных состояний вещества
Изменение агрегатных состояний вещества Гидродинамика. Введение в гидродинамику. Виды движения
Гидродинамика. Введение в гидродинамику. Виды движения Двигатели внутреннего сгорания. Конструкция
Двигатели внутреннего сгорания. Конструкция Огляд конструкцій плугів спец. призначення. Огляд конструкцій фрезерних машин, ямокопачів, площадкоутворювачів. Лекція 4 (ч. 1)
Огляд конструкцій плугів спец. призначення. Огляд конструкцій фрезерних машин, ямокопачів, площадкоутворювачів. Лекція 4 (ч. 1) Механическая КПП
Механическая КПП Психикалық статустың жазылуымен науқастың психикалық жағдайын бағалау әдістері
Психикалық статустың жазылуымен науқастың психикалық жағдайын бағалау әдістері Избранные главы неорганического материаловедения. (Лекция 2)
Избранные главы неорганического материаловедения. (Лекция 2) Расчет временных характеристик линейных электрических цепей
Расчет временных характеристик линейных электрических цепей Презентации к некоторым лабораторным работам по учебнику А.В.Перышкина Физика 7
Презентации к некоторым лабораторным работам по учебнику А.В.Перышкина Физика 7 Свет. Источники света
Свет. Источники света Chapter 20 Thermodynamics
Chapter 20 Thermodynamics Масса. Объем. Плотность
Масса. Объем. Плотность Источники звука и звуковые колебания
Источники звука и звуковые колебания Углеродные нанотрубки. Свойства. Методы получения. Применение
Углеродные нанотрубки. Свойства. Методы получения. Применение Кинематический анализ рычажных механизмов
Кинематический анализ рычажных механизмов Атом Резерфорда - Бора
Атом Резерфорда - Бора Полупроводниковый диод
Полупроводниковый диод Двигатель внутреннего сгорания
Двигатель внутреннего сгорания Физика и познание мира
Физика и познание мира Механическое оборудование и система вентиляции
Механическое оборудование и система вентиляции Презентация к уроку по теме Простые механизмы.
Презентация к уроку по теме Простые механизмы. История о часах
История о часах Излучение. Тепловое излучение
Излучение. Тепловое излучение Электрические цепи постоянного тока. Элементы электрической цепи
Электрические цепи постоянного тока. Элементы электрической цепи