Слайд 2
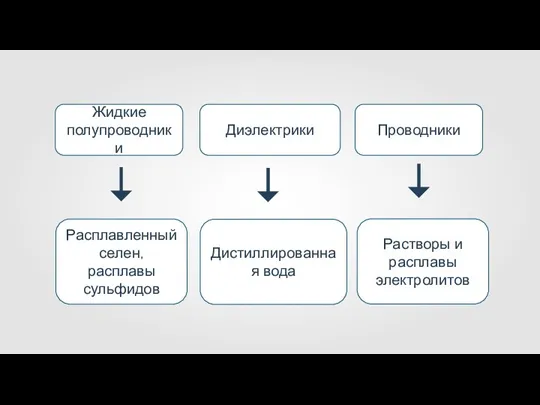
Жидкие полупроводники
Диэлектрики
Проводники
Слайд 3
Электролиты — это водные растворы солей, кислот, щелочей, обладающие ионной проводимостью.
Слайд 4
Электролитами также называют и проводящие среды, в которых протекание электрического тока
происходит в результате переноса вещества.
Слайд 5
+
‒
+
‒
+
‒
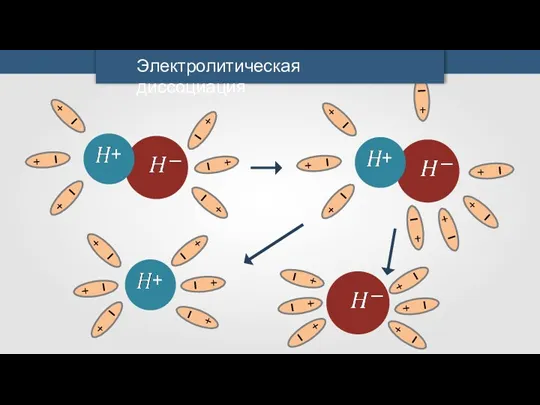
Электролитическая диссоциация
Слайд 6

Степень диссоциации зависит от:
Температуры
Концентрации раствора
Электрических свойств вещества
Слайд 7

Слайд 8
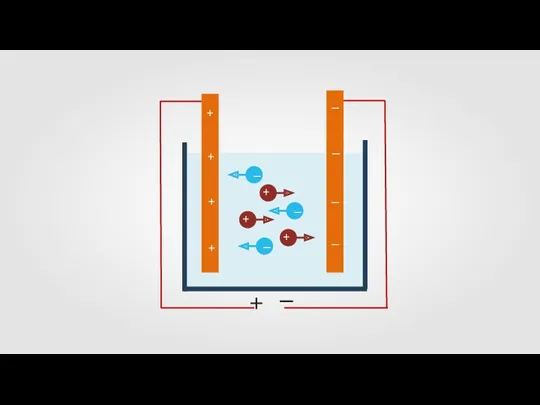
Слайд 9
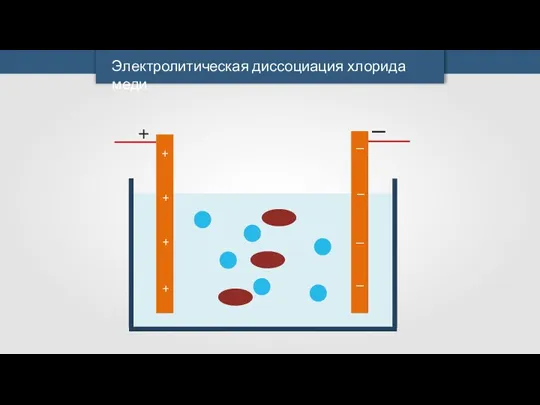
Электролитическая диссоциация хлорида меди
Слайд 10
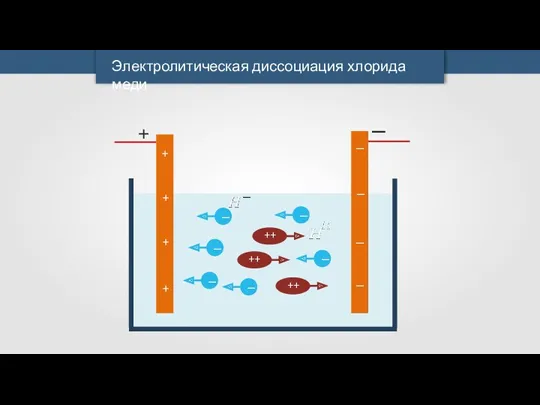
Электролитическая диссоциация хлорида меди
Слайд 11

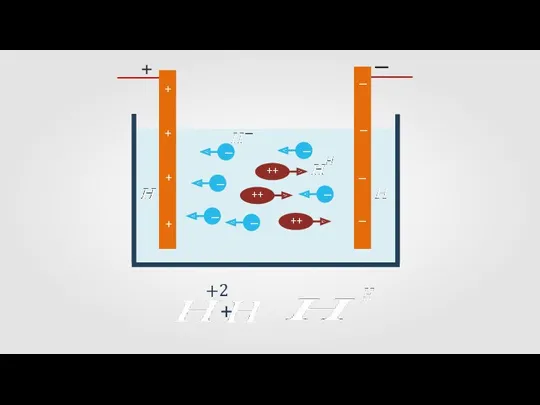
Электрический ток в электролитах представляет собой упорядоченное движение положительных
и отрицательных
ионов.
Слайд 12
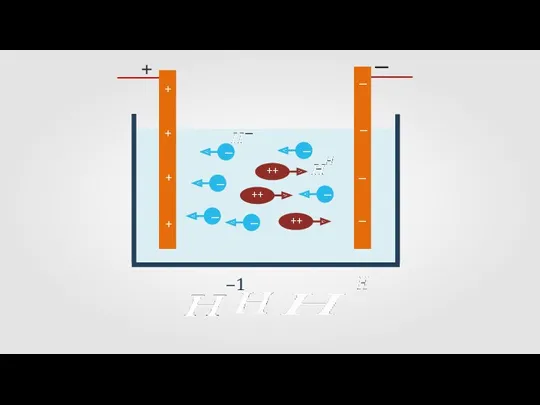
Слайд 13
Слайд 14
+
+
+
+
‒
‒
‒
‒
‒
+
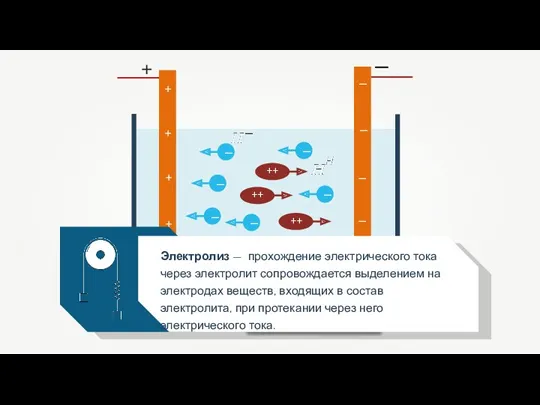
Электролиз — прохождение электрического тока через электролит сопровождается выделением на электродах
веществ, входящих в состав электролита, при протекании через него электрического тока.
Слайд 15
У. Нильсон
1753–1815 гг.
В 1800 открыли явление электролиза.
А. Карлейн
1768–1840
гг.
Слайд 16

М. Фарадей
1791–1867 гг.
В 1833 г. открыл закон для электролиза.
Слайд 17

Слайд 18

Слайд 19

Слайд 20

Закон Фарадея для электролиза
Слайд 21

Слайд 22
+
+
+
+
‒
‒
‒
‒
‒
+
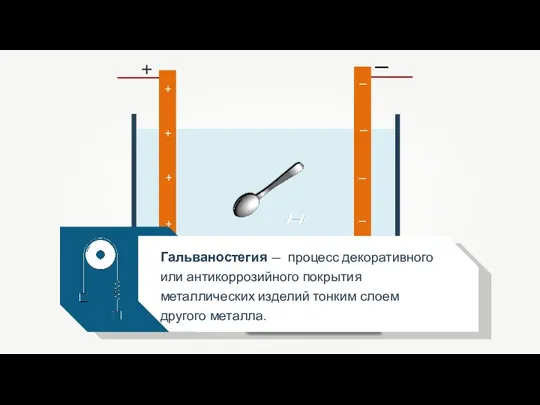
Гальваностегия — процесс декоративного или антикоррозийного покрытия металлических изделий тонким слоем
Слайд 23

Слайд 24

Слайд 25

Гальванопластика — это электролитическое изготовление металлических копий рельефных предметов.
Слайд 26

Б.С. Якоби
1801–1874 гг.
В 1836 г. открыл процесс получения
отслаиваемых покрытий.
Слайд 27

+
‒
Электрометаллургия — это получение чистых металлов (Al, Na, Mg, Be) при электролизе
расплавленных руд.


























 Линзы. Оптические приборы
Линзы. Оптические приборы Облаштування бульдозерів і визначення їх продуктивності
Облаштування бульдозерів і визначення їх продуктивності Истечение газов и паров
Истечение газов и паров Oscillatory motion
Oscillatory motion Ремонт КШМ двигателя Д-240
Ремонт КШМ двигателя Д-240 Презентация Мощность.Единицы мощности
Презентация Мощность.Единицы мощности Задачи на смеси, сплавы и растворы
Задачи на смеси, сплавы и растворы Молекулярно-кинетическая теория газов. (Лекция 2)
Молекулярно-кинетическая теория газов. (Лекция 2) Задачи по статике. (10 класс)
Задачи по статике. (10 класс) Мир в магнитах. При поддержке туристической компании Колесница
Мир в магнитах. При поддержке туристической компании Колесница Нитрид индия – новый материал для оптоэлектроники
Нитрид индия – новый материал для оптоэлектроники Методы измерения газопроницаемости
Методы измерения газопроницаемости Презентация-отчет по учебной практике
Презентация-отчет по учебной практике Свободные электромагнитные колебания. Колебательный контур
Свободные электромагнитные колебания. Колебательный контур Элементы машиноведения. Составные части машин
Элементы машиноведения. Составные части машин Механические свойства твердых тел
Механические свойства твердых тел Машиноведение. История создания швейной машины
Машиноведение. История создания швейной машины Презентация:Каты җисемнәрдә, сыеклыкларда һәм газларда басым.
Презентация:Каты җисемнәрдә, сыеклыкларда һәм газларда басым. Постоянный ток. Лекция №6
Постоянный ток. Лекция №6 Электрический ток в металлах
Электрический ток в металлах Закон Ома для полной цепи
Закон Ома для полной цепи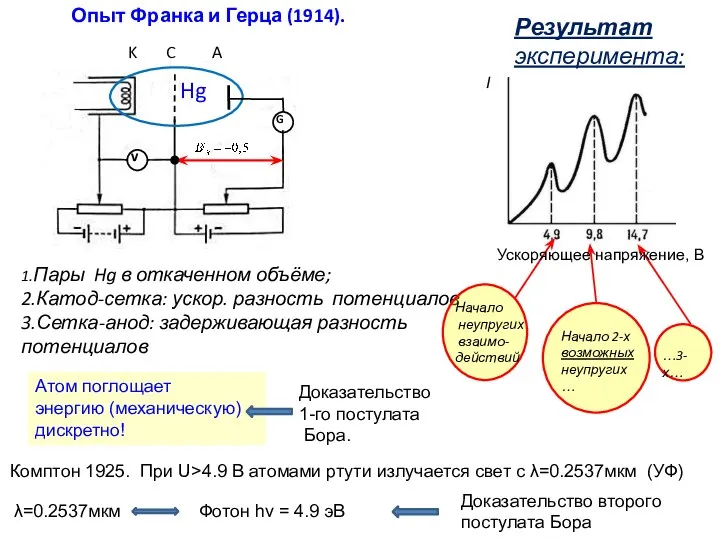 Опыт Франка и Герца (1914)
Опыт Франка и Герца (1914) Техника безопасности при работе с электрическим током. Проблемы энергосбережения
Техника безопасности при работе с электрическим током. Проблемы энергосбережения Паровая машина. Паровой двигатель Уатта
Паровая машина. Паровой двигатель Уатта Презентация к уроку в 11 классе Лазеры
Презентация к уроку в 11 классе Лазеры Пример использования метода преобразования сложнозамкнутых электрических сетей
Пример использования метода преобразования сложнозамкнутых электрических сетей Традиційна енергетика. Централізовані системи електропостачання
Традиційна енергетика. Централізовані системи електропостачання Основные законы электростатики
Основные законы электростатики