Содержание
- 2. УЧЕНЫЕ ДРЕВНОСТИ О СТРОЕНИИ ВЕЩЕСТВА Древнегреческий ученый Демокрит 2500 лет назад считал, что любое вещество состоит
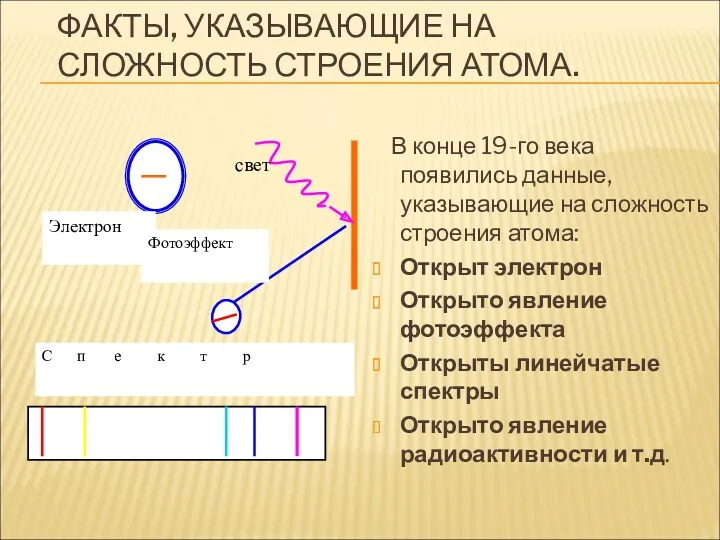
- 3. ФАКТЫ, УКАЗЫВАЮЩИЕ НА СЛОЖНОСТЬ СТРОЕНИЯ АТОМА. В конце 19-го века появились данные, указывающие на сложность строения
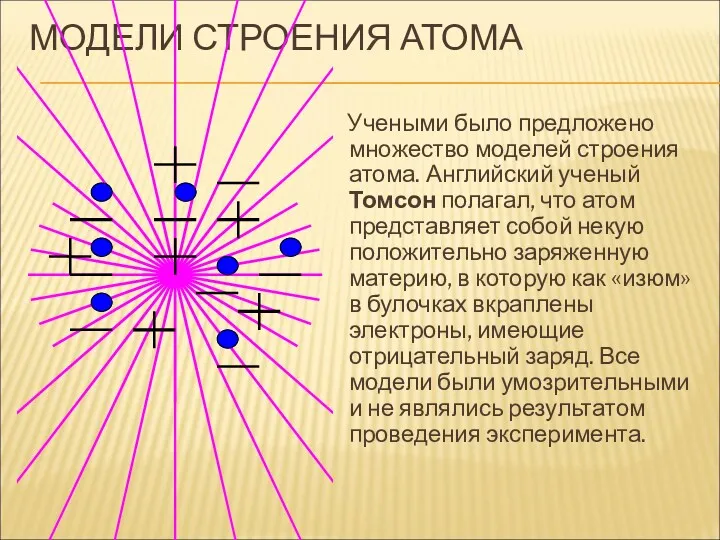
- 4. МОДЕЛИ СТРОЕНИЯ АТОМА Учеными было предложено множество моделей строения атома. Английский ученый Томсон полагал, что атом
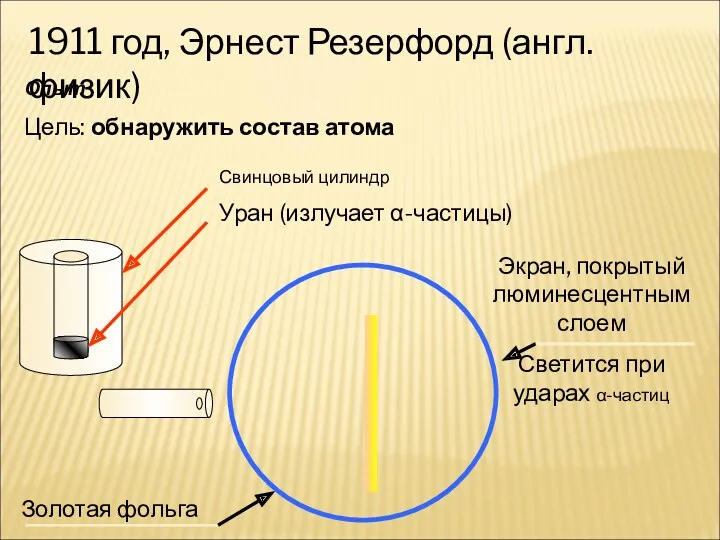
- 5. 1911 год, Эрнест Резерфорд (англ.физик) Опыт Цель: обнаружить состав атома Свинцовый цилиндр Уран (излучает α-частицы) Золотая
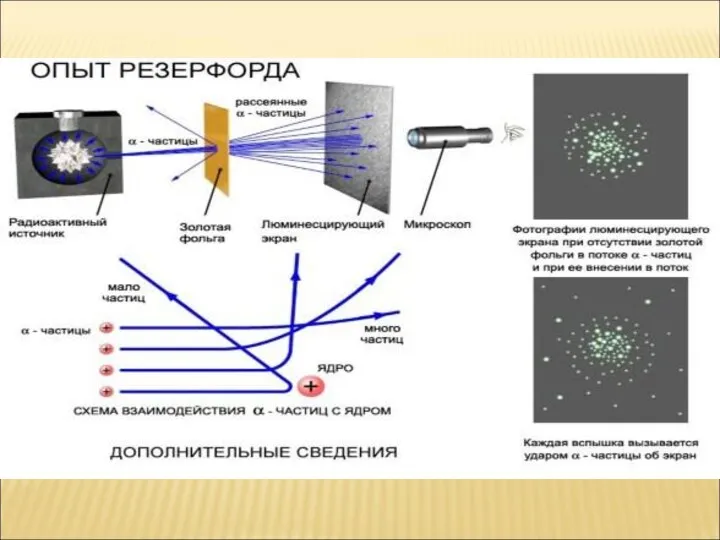
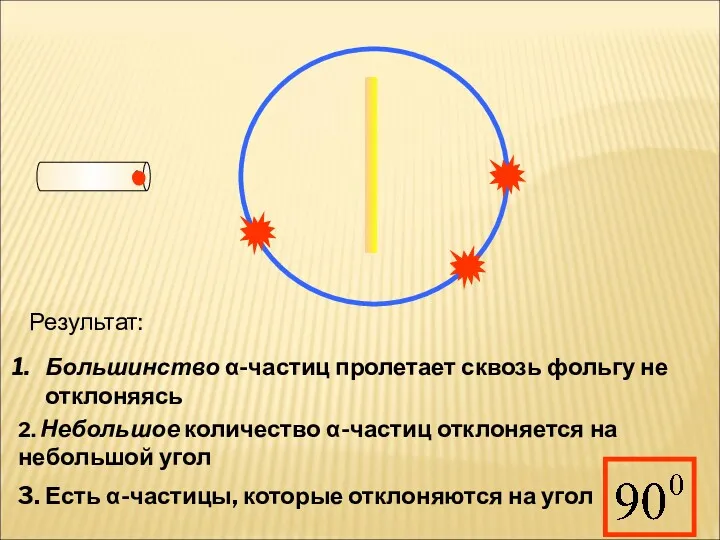
- 7. Результат: Большинство α-частиц пролетает сквозь фольгу не отклоняясь 2. Небольшое количество α-частиц отклоняется на небольшой угол
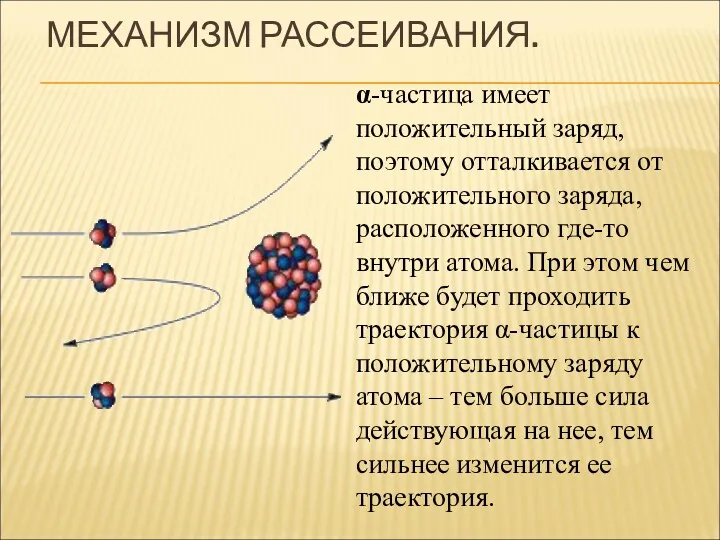
- 8. МЕХАНИЗМ РАССЕИВАНИЯ. α-частица имеет положительный заряд, поэтому отталкивается от положительного заряда, расположенного где-то внутри атома. При
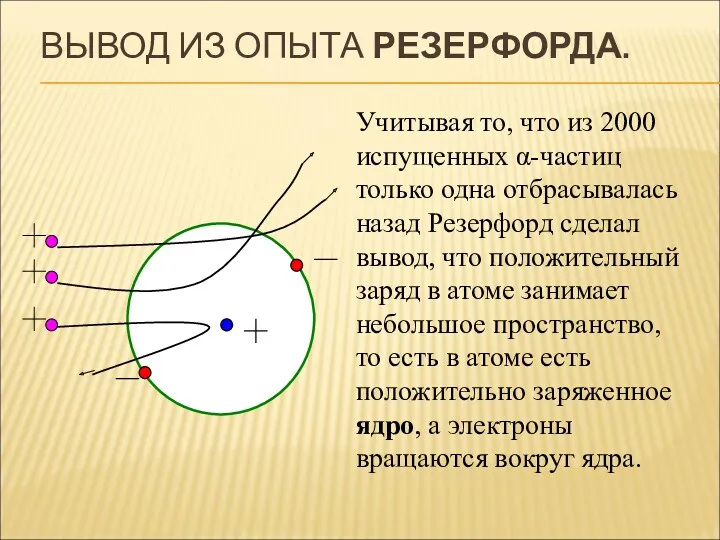
- 9. ВЫВОД ИЗ ОПЫТА РЕЗЕРФОРДА. Учитывая то, что из 2000 испущенных α-частиц только одна отбрасывалась назад Резерфорд
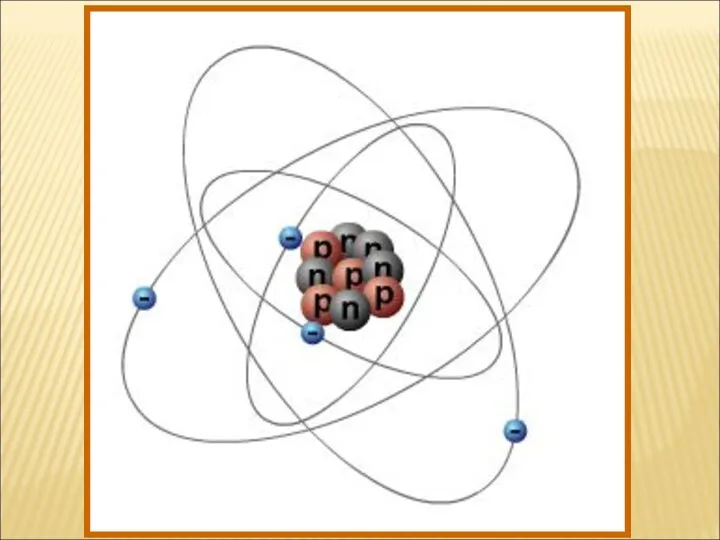
- 10. СТРОЕНИЕ АТОМА Из опыта Резерфорда следует, что атом устроен следующим образом: в центре атома расположено положительно
- 12. ЯДРО Ядро представляет собой центральную часть атома. В нем сосредоточены положительный электрический заряд и основная часть
- 13. ИСТОРИЯ ОТКРЫТИЯ СТРОЕНИЯ АТОМНОГО ЯДРА Ядра большинства атомов оказались не только очень малы – на них
- 14. ОТКРЫТИЕ СТРОЕНИЯ ЯДРА Открытие изотопов не прояснило вопрос о строении ядра. К этому времени были известны
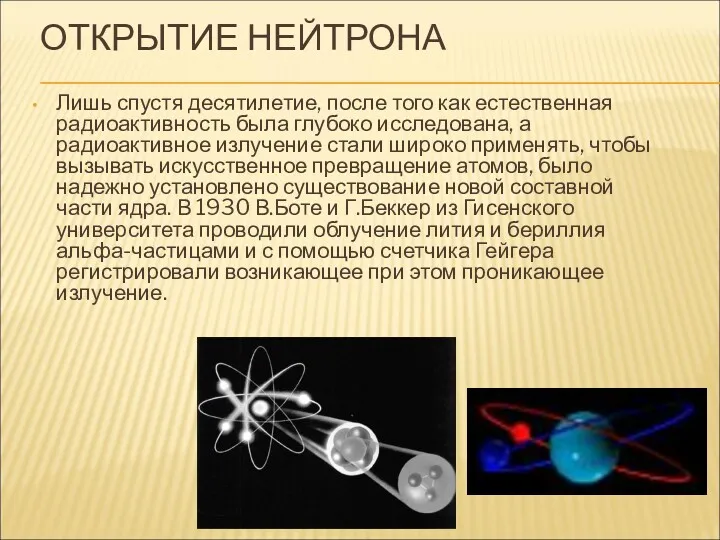
- 15. ОТКРЫТИЕ НЕЙТРОНА Лишь спустя десятилетие, после того как естественная радиоактивность была глубоко исследована, а радиоактивное излучение
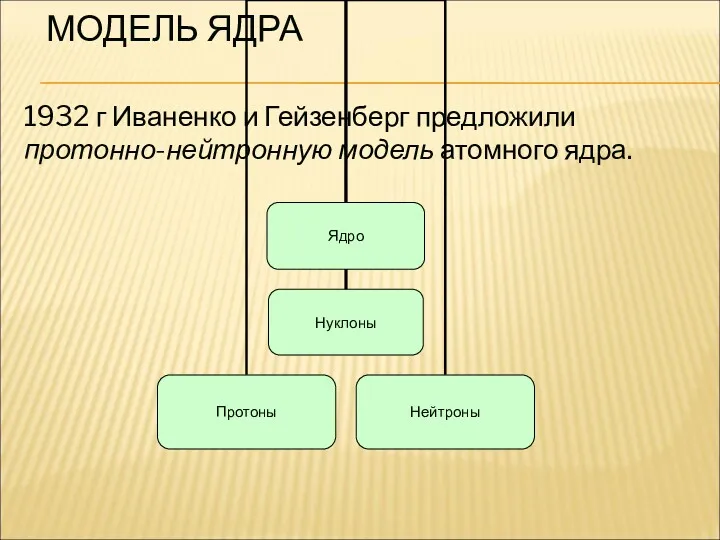
- 16. МОДЕЛЬ ЯДРА 1932 г Иваненко и Гейзенберг предложили протонно-нейтронную модель атомного ядра.
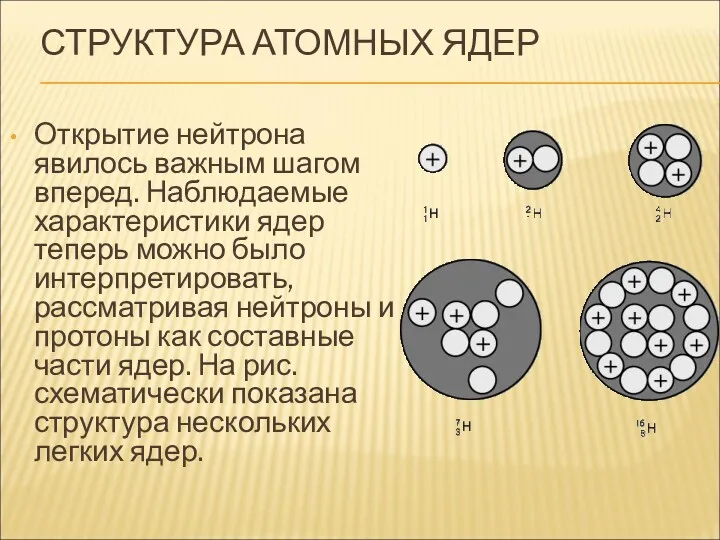
- 18. СТРУКТУРА АТОМНЫХ ЯДЕР Открытие нейтрона явилось важным шагом вперед. Наблюдаемые характеристики ядер теперь можно было интерпретировать,
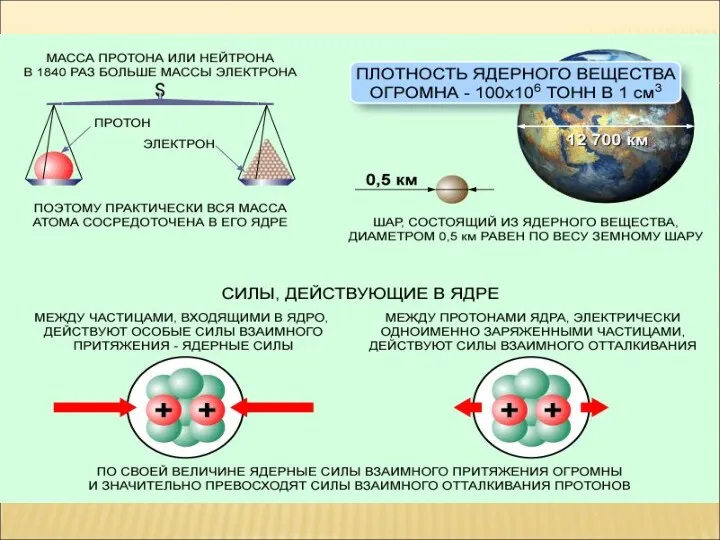
- 19. ЯДЕРНЫЕ СИЛЫ Малый радиус действия ядерных сил впервые отчетливо обнаружился уже в опытах по рассеянию Резерфорда.
- 21. Скачать презентацию






 Образовательная среда кабинета физики как условие формирования и развития УУД обучающихся
Образовательная среда кабинета физики как условие формирования и развития УУД обучающихся Электромагнитные колебания и волны
Электромагнитные колебания и волны Негативные факторы в системе Человек – среда обитания (вводное занятие Химические и физико-энергетические опасные факторы)
Негативные факторы в системе Человек – среда обитания (вводное занятие Химические и физико-энергетические опасные факторы) Қайтымды реакциялар
Қайтымды реакциялар Презентация к уроку по физике (7 класс) Сила трения
Презентация к уроку по физике (7 класс) Сила трения Физика и методы научного познания
Физика и методы научного познания Основные понятия кинематики. Кинематика точки
Основные понятия кинематики. Кинематика точки Fuel supply system DC9 EDC MS5
Fuel supply system DC9 EDC MS5 Основы генерирования и формирования сигналов. Лекция 2
Основы генерирования и формирования сигналов. Лекция 2 Импульс, закон сохранения импульса
Импульс, закон сохранения импульса Магнитное поле в веществе
Магнитное поле в веществе Урок в 7 классе По следам одной катастрофы
Урок в 7 классе По следам одной катастрофы Электрический ток в жидкостях
Электрический ток в жидкостях Элементы механики жидкости. Давление в жидкости и газе
Элементы механики жидкости. Давление в жидкости и газе Розміщення електрообладнання БМП-2 в машині
Розміщення електрообладнання БМП-2 в машині Спектральные методы исследования веществ. Масс-спектрометрический метод анализа
Спектральные методы исследования веществ. Масс-спектрометрический метод анализа Технологическое оборудование для предприятий технического сервиса (Лекция № 6 )
Технологическое оборудование для предприятий технического сервиса (Лекция № 6 ) Вращательные передачи
Вращательные передачи Тұрақты жүктемелі үздіксіз қозғалыс механизмі
Тұрақты жүктемелі үздіксіз қозғалыс механизмі Методическая разработка урока Плотность вещества
Методическая разработка урока Плотность вещества Материалдардың созылуын және сығылуын эксперимент арқылы зерттеу
Материалдардың созылуын және сығылуын эксперимент арқылы зерттеу Жидкие кристаллы
Жидкие кристаллы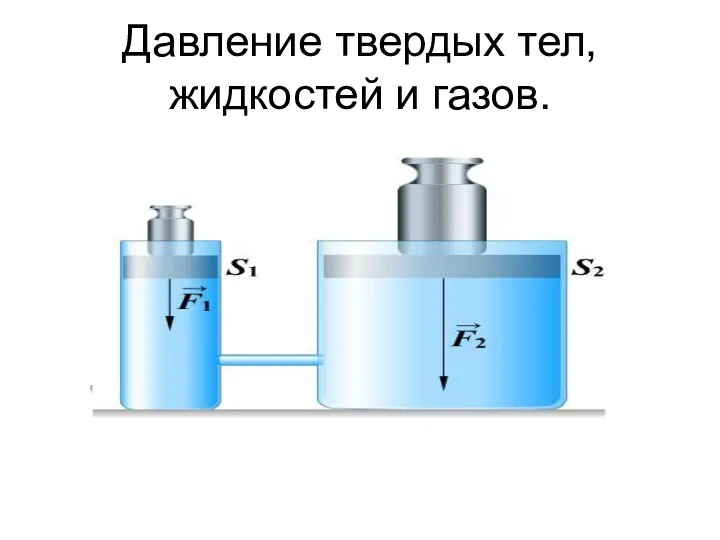 Давление твердых тел, жидкостей и газов
Давление твердых тел, жидкостей и газов Основные понятия и определения планарной технологии ИС (интегральная схема). Практическое занятие №1
Основные понятия и определения планарной технологии ИС (интегральная схема). Практическое занятие №1 Презентация по теме Электрическое поле и его свойства
Презентация по теме Электрическое поле и его свойства Сила Архимеда. Подготовка к ЕГЭ
Сила Архимеда. Подготовка к ЕГЭ работа и энергия
работа и энергия Дизельна електростанція
Дизельна електростанція