Содержание
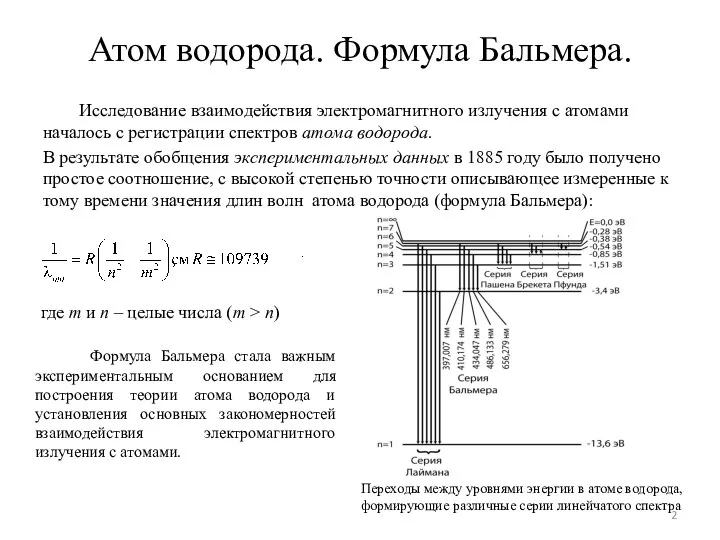
- 2. Атом водорода. Формула Бальмера. Исследование взаимодействия электромагнитного излучения с атомами началось с регистрации спектров атома водорода.
- 3. Полуклассическая теория атома Н. Бора. Постулаты Бора. 1. Электроны в атомах находятся в особых, стационарных состояниях
- 4. Уравнения Бора и атомные единицы.
- 5. Дискретный спектр энергии водородоподобного атома Целое неотрицательное число n, фигурирующее в этом равенстве, отвечает главному квантовому
- 6. Принцип соответствия между классической и квантовой механикой Вышеизложенная теория Бора является не только теорией атома водорода,
- 7. Мощность излучения атомного перехода Итак, использование формулы классической электродинамики и замен дипольного момента и собственной частоты
- 8. Спектроскопический принцип соответствия Принцип соответствия между классической и квантовой физикой, конкретизированный для случая излучательных переходов в
- 9. Сила осциллятора Вклад осцилляторов переходов в отклик атома на электромагнитное воздействие пропорционален безразмерной величине, называемой силой
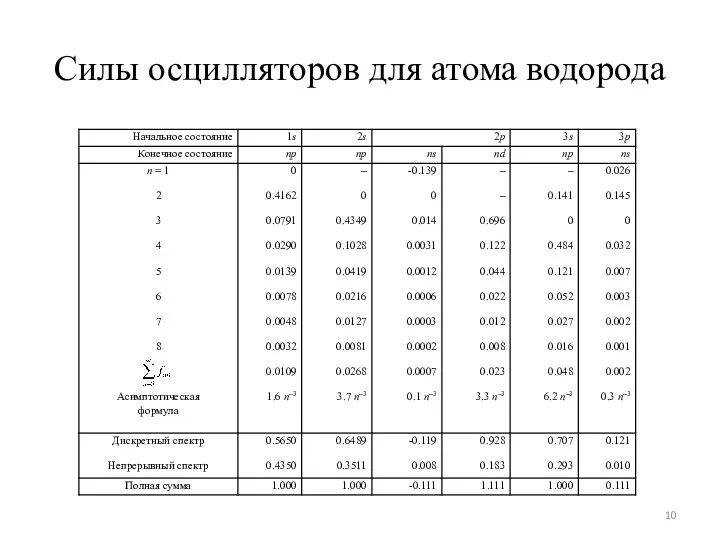
- 10. Силы осцилляторов для атома водорода
- 11. Взаимодействие электромагнитного поля с осциллятором перехода в атоме
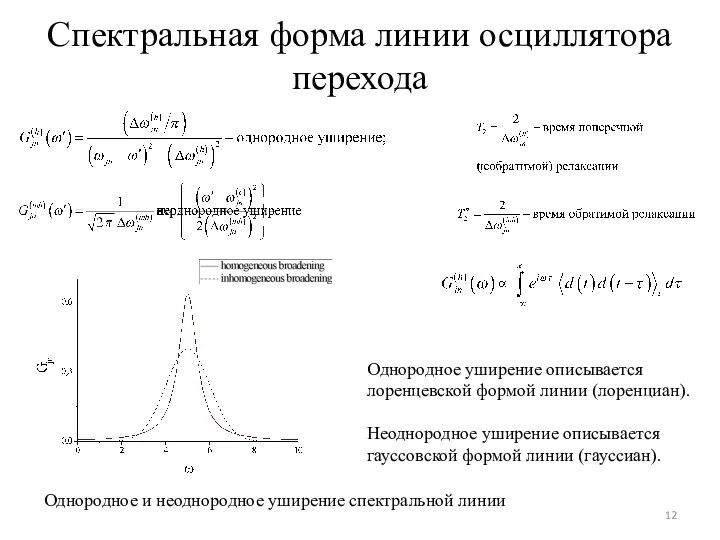
- 12. Спектральная форма линии осциллятора перехода Однородное и неоднородное уширение спектральной линии Однородное уширение описывается лоренцевской формой
- 13. Сечение радиационного перехода
- 14. Динамическая поляризуемость атома
- 15. Предельные случаи атомной поляризуемости
- 16. Общие соотношения для динамической поляризуемости
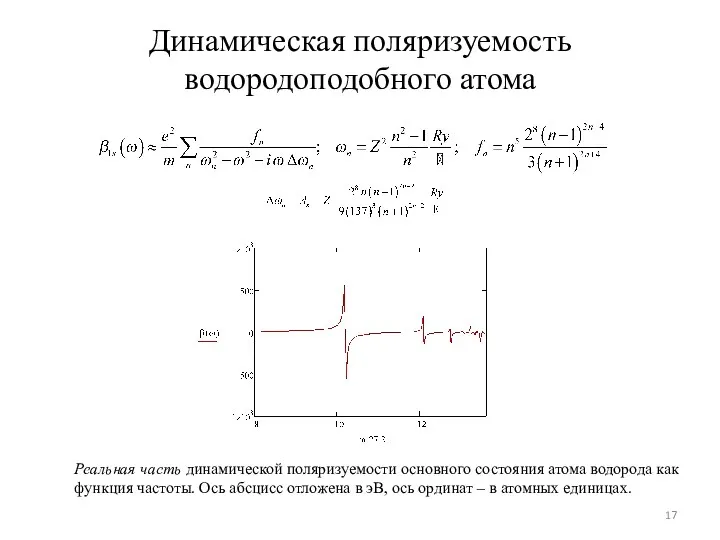
- 17. Динамическая поляризуемость водородоподобного атома Реальная часть динамической поляризуемости основного состояния атома водорода как функция частоты. Ось
- 18. Фотоионизация атомной оболочки Как правило, в сечение фотоионизации дает основной вклад переход с увеличением квантового числа
- 19. Водородоподобное приближение для фотоионизации (формула Зоммерфельда)
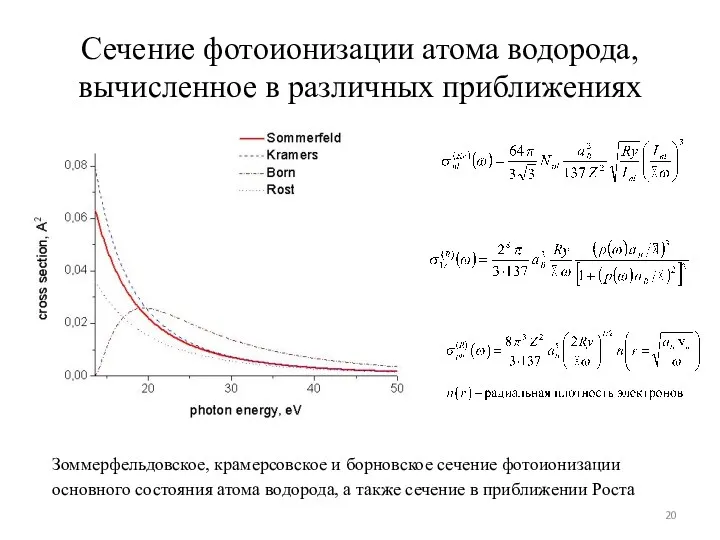
- 20. Сечение фотоионизации атома водорода, вычисленное в различных приближениях Зоммерфельдовское, крамерсовское и борновское сечение фотоионизации основного состояния
- 21. Рассеяние фотона на свободном электроне Рассеяние фотона на покоящемся электроне, pe – импульс отдачи электрона
- 22. Рэлеевское рассеяние излучения на атоме, интегральное по углу рассеяния
- 24. Скачать презентацию
















 Презентация Звук
Презентация Звук Электронная проводимость металлов. Электрический ток и его характеристики
Электронная проводимость металлов. Электрический ток и его характеристики Теплообменные аппараты
Теплообменные аппараты Генератор незатухающих колебаний
Генератор незатухающих колебаний Электрические тали
Электрические тали Презентация к уроку физики в 8 классе на тему Звуковые волны в различных средах
Презентация к уроку физики в 8 классе на тему Звуковые волны в различных средах Окружающий мир как иерархическая система
Окружающий мир как иерархическая система Вертолет Ми-8МТВ. Несущий винт
Вертолет Ми-8МТВ. Несущий винт Подготовка к ГИА по физике 2013
Подготовка к ГИА по физике 2013 Механическая работа и мощность 7 класс, презентация
Механическая работа и мощность 7 класс, презентация Механическая работа
Механическая работа Ручное изготовление кольца с использованием традиционных материалов
Ручное изготовление кольца с использованием традиционных материалов Механические характеристики электродвигателей постоянного тока
Механические характеристики электродвигателей постоянного тока Механические передачи. Ременные передачи
Механические передачи. Ременные передачи NW Rapid Site Installation
NW Rapid Site Installation Основные понятия теории механизмов и машин
Основные понятия теории механизмов и машин Основы измерения основных параметров зубчатого колеса с эвольвентным профилем
Основы измерения основных параметров зубчатого колеса с эвольвентным профилем Презентация Дисперсия. Дифракция и интерференция света
Презентация Дисперсия. Дифракция и интерференция света Вечный двигатель
Вечный двигатель Урок по физике в 8 классе по теме: Испарение
Урок по физике в 8 классе по теме: Испарение Презентация к уроку Сила. Явления тяготения. Сила тяжести.
Презентация к уроку Сила. Явления тяготения. Сила тяжести. Путь и время движения.
Путь и время движения. разработка технологического процесса на механическую обработку детали фланец
разработка технологического процесса на механическую обработку детали фланец Сборка модели электролизера для получения водорода
Сборка модели электролизера для получения водорода Тепловые двигатели и охрана окружающей среды
Тепловые двигатели и охрана окружающей среды Применение компьютера в демонстрационном эксперименте
Применение компьютера в демонстрационном эксперименте электрическое поле. напряжонность
электрическое поле. напряжонность Теория информационных процессов и систем. Элементы теории приема и обработки информации. (Тема 4)
Теория информационных процессов и систем. Элементы теории приема и обработки информации. (Тема 4)