Первый закон электролиза Фарадея: масса вещества, осаждённого на электроде при
электролизе, прямо пропорциональна количеству электричества, переданного на этот электрод. Под количеством электричества имеется в виду электрический заряд, измеряемый, как правило, в кулонах :
m = k*q = k*I*Δt , где:
q – электрический заряд(в кулонах), I – сила тока, Δt – промежуток времени,
k - электрохимический эквивалент.
Второй закон электролиза Фарадея: электрохимический эквивалент прямо пропорционален молярной массе выделяемого вещества и обратно пропорционален его валентности:
k= M/(F*z), где:
M – молярная масса образовавшегося на электроде вещества , F= 96485 Кл/моль – Постоянная Фарадея , z – валентность вещества.
Отсюда общая формула равна:
m = (q/F)*(M/z)
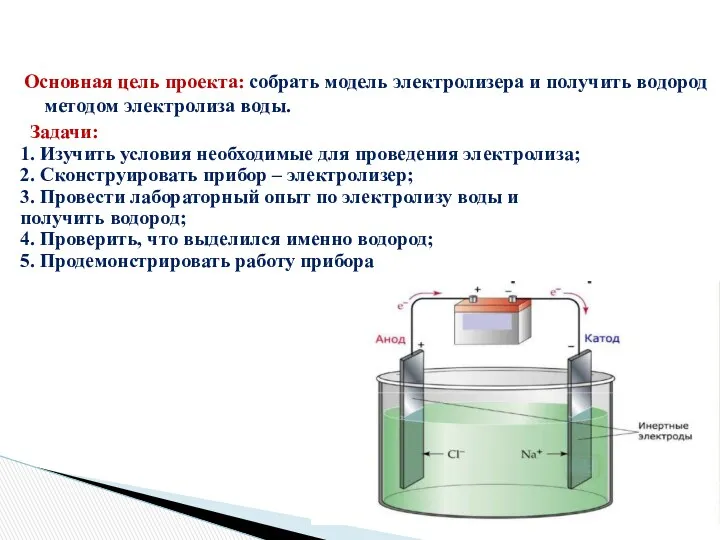
Основные законы электролиза





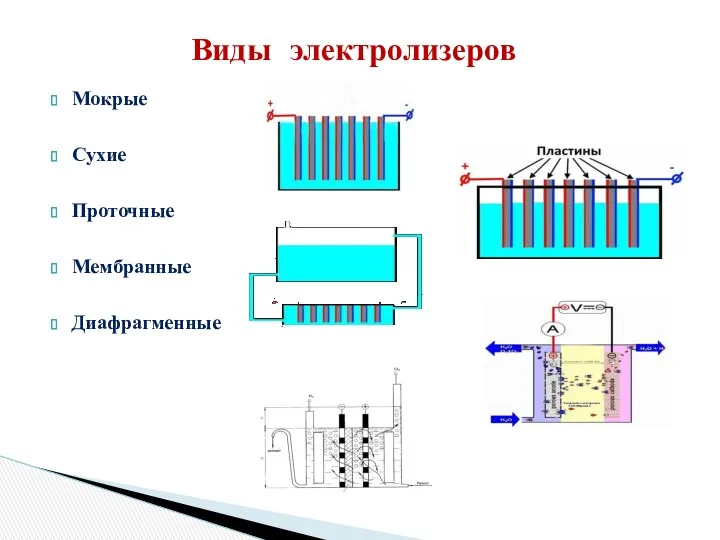





 Двигатели FSI. Потенциометры дроссельной заслонки
Двигатели FSI. Потенциометры дроссельной заслонки Ядерные реакции
Ядерные реакции Трёхфазные цепи
Трёхфазные цепи Техническое обслуживание и ремонт автомобильных кранов
Техническое обслуживание и ремонт автомобильных кранов Дисперсия света
Дисперсия света Конденсатори
Конденсатори Биомеханика двигательных действий: составные движения в биокинематических цепях
Биомеханика двигательных действий: составные движения в биокинематических цепях Istoria electricitatii
Istoria electricitatii Непрерывно-детерминированные модели (D-схемы)
Непрерывно-детерминированные модели (D-схемы) Взаимодействие тел. Масса тела
Взаимодействие тел. Масса тела Сборка электромагнита и испытание его действия. Лабораторная работа
Сборка электромагнита и испытание его действия. Лабораторная работа Закон сохранения энергии. Работа и кинетическая энергия
Закон сохранения энергии. Работа и кинетическая энергия Второй закон Ньютона
Второй закон Ньютона Ремонт КШМ двигателя Д-240
Ремонт КШМ двигателя Д-240 Три состояния вещества
Три состояния вещества Обеспечение безопасности полётов и авиационной безопасности. Тема 1.1
Обеспечение безопасности полётов и авиационной безопасности. Тема 1.1 Дослідження режимів роботи рентгенівських апаратів
Дослідження режимів роботи рентгенівських апаратів Электрический ток в газах. Урок изучения нового материала. 10 класс
Электрический ток в газах. Урок изучения нового материала. 10 класс Фотометрия. Энергетические характеристики света
Фотометрия. Энергетические характеристики света Методическая разработка урока физики 8 класс. Лабораторная работа № 13 Исследование зависимости угла преломления от угла падения света.
Методическая разработка урока физики 8 класс. Лабораторная работа № 13 Исследование зависимости угла преломления от угла падения света. Презентация к уроку физики в 9 классе по теме Искусственные спутники Земли. Первая космическая скорость
Презентация к уроку физики в 9 классе по теме Искусственные спутники Земли. Первая космическая скорость Условные графические обозначения на принципиальных электрических схемах
Условные графические обозначения на принципиальных электрических схемах Физико–химические свойства нефти, нефтепродуктов. Качество нефти и нефтепродуктов. Методы их анализа
Физико–химические свойства нефти, нефтепродуктов. Качество нефти и нефтепродуктов. Методы их анализа Научные фокусы. Электрические тени
Научные фокусы. Электрические тени Вода. Физические и химические свойства воды. 8 класс
Вода. Физические и химические свойства воды. 8 класс Общие сведения об устройствах получения информации о процессе
Общие сведения об устройствах получения информации о процессе Фізичні основи механіки. Лекція №1
Фізичні основи механіки. Лекція №1 Заболевания молочных желёз. Взгляд гинеколога
Заболевания молочных желёз. Взгляд гинеколога