Содержание
- 2. Содержание Вода в природе Применение и значение воды Рефлексия Круговорот воды Физические св-ва воды Химические св-ва
- 3. I.Вода в природе Большая часть поверхности Земли покрыта морями и океанами - 71% Морская вода –
- 4. 1.Вода́ (оксид водорода) —Н2O. Mr (H2O)= M (H2O)= Связь между атомами водорода и кислорода возникает за
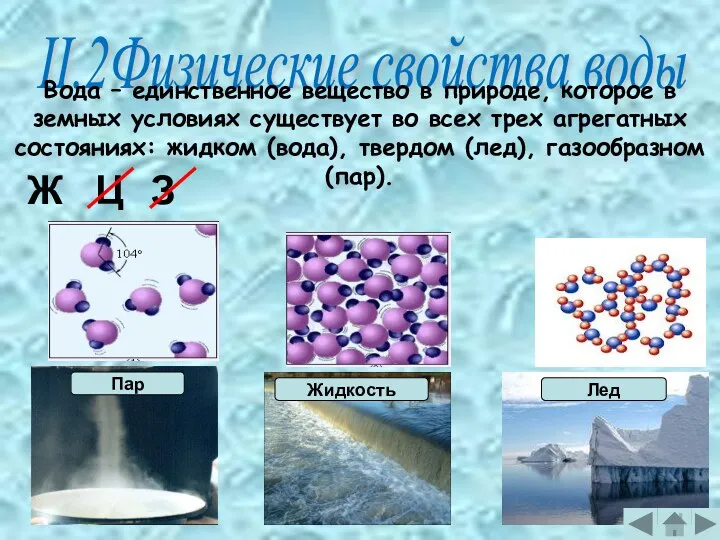
- 5. II.2Физические свойства воды Вода – единственное вещество в природе, которое в земных условиях существует во всех
- 6. Вода в организме человека Кровь человека на 90% состоит из воды Мышцы на 75% Кости на
- 7. Вода в организме человека Обезвоживание организма на 12 – 15 % приводит к нарушению обмена веществ,
- 8. III.Химические свойства воды
- 10. б) металлы средней активности взаимодействуют с водой при нагревании, образуя оксид металла и H2: Zn +
- 11. III.2 Взаимодействие с неметаллами Получающиеся продукты взаимодействия очень разнообразны: C + H2О = H2 + CO
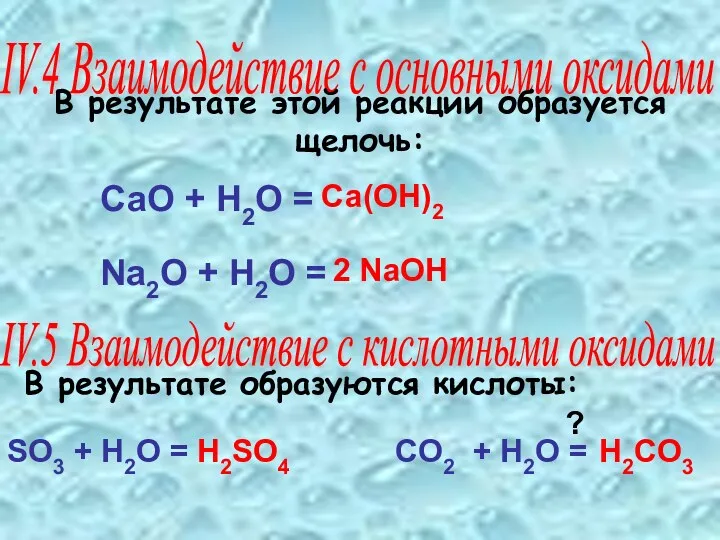
- 12. В результате образуются кислоты: IV.4 Взаимодействие с основными оксидами IV.5 Взаимодействие с кислотными оксидами В результате
- 14. IV.Круговорот воды в природе Вода постоянно испаряется с поверхности наземных водоемов, листьев растений Так возникает водяной
- 15. Вода необходима всем живым организмам: растениям, животным и человеку. Без воды нет жизни. Вода – одно
- 16. Закончите уравнения реакций, расставьте коэффициенты: а) Li2O + H2O → б) Mg + H2O → в)
- 18. Скачать презентацию













 Презентация по физике 9 класс Неравномерное движение
Презентация по физике 9 класс Неравномерное движение Сила трения. Трение в природе и технике
Сила трения. Трение в природе и технике Механические колебания. Волны. Акустика. Ультразвук. Лекция №4
Механические колебания. Волны. Акустика. Ультразвук. Лекция №4 Электротехника и электроника
Электротехника и электроника Схемы соединения потребителей трехфазного тока
Схемы соединения потребителей трехфазного тока Тепловозные дизели
Тепловозные дизели Высота всасывания насоса. Условия бескавитационной работы насоса. (Лекция 8)
Высота всасывания насоса. Условия бескавитационной работы насоса. (Лекция 8) Теплопроводность. Нестационарная теплопроводность. (Тема 4. Лекции 16,17)
Теплопроводность. Нестационарная теплопроводность. (Тема 4. Лекции 16,17) Физика туралы ғылым
Физика туралы ғылым Смешанное соединение элементов в цепи постоянного тока
Смешанное соединение элементов в цепи постоянного тока Электр өрісі
Электр өрісі Автомеханік
Автомеханік Электрический ток в металлах и электролитах. Законы Фарадея
Электрический ток в металлах и электролитах. Законы Фарадея NW Rapid Site Installation
NW Rapid Site Installation Механические волны
Механические волны Повторение формул по физике, 7 класс
Повторение формул по физике, 7 класс Теплообмен при кипении и конденсации
Теплообмен при кипении и конденсации Давление в жидкости и газе. Расчет давления жидкости на дно и стенки сосуда
Давление в жидкости и газе. Расчет давления жидкости на дно и стенки сосуда Формула Мора. Правило Верещагина
Формула Мора. Правило Верещагина Подшипники качения
Подшипники качения Своя игра по физике - 7
Своя игра по физике - 7 Силовые линии электрического поля (линии напряженности)
Силовые линии электрического поля (линии напряженности) Требования к видимости на дорогах. Торможение автомобиля
Требования к видимости на дорогах. Торможение автомобиля Цепная реакция деления ядер. Ядерный реактор
Цепная реакция деления ядер. Ядерный реактор Общая физика
Общая физика Применение сообщающихся сосудов
Применение сообщающихся сосудов Механічна енергія
Механічна енергія Молекулярная физика и термодинамика
Молекулярная физика и термодинамика