Содержание
- 2. Предшественники: никель-кадмиевый и никель-железный аккумуляторы Ni-Cd; Ni - Fe Вальдемар Юнгнер (Швеция, 1899 г.) Ni -
- 3. Компоненты НК- и НЖ-аккумуляторов Положительный электрод – NiOOH с добавкой графита Отрицательный электрод – Cd или
- 4. Электрохимические процессы Электродные реакции: на положительном оксидно-никелевом электроде: Ni(OH)2 + OH- → NiOOH + H2O +
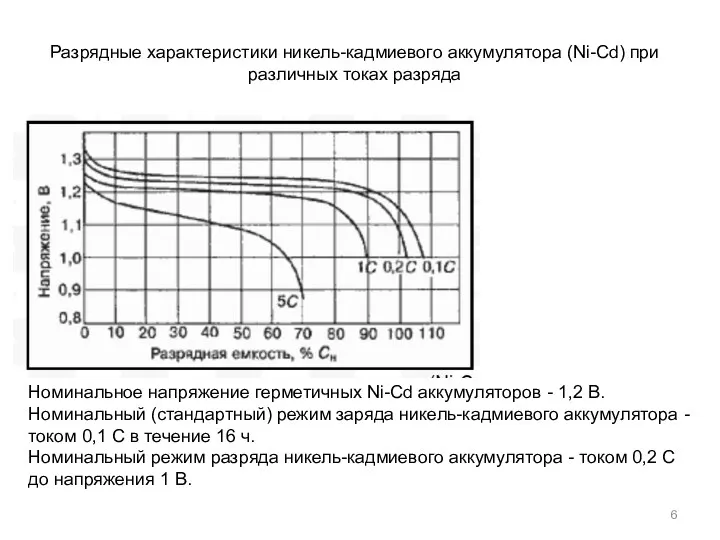
- 6. Разрядные характеристики никель-кадмиевого аккумулятора (Ni-Cd) при различных токах разряда Номинальное напряжение герметичных Ni-Cd аккумуляторов - 1,2
- 7. Применение НК-аккумуляторов: первые компактные компьютеры Предок нынешних сверхкомпактных персональных компьютеров – Epson HX-20 (1981 г.)
- 8. Применение НК-аккумуляторов: первые мобильные телефоны Первый «народный» GSM-телефон Nokia 1011 (1992 г.)
- 9. Применение НЖ-аккумуляторов Первые электромобили 1915 Detroit Electric Model 61 Электровозы, электропогрузчики
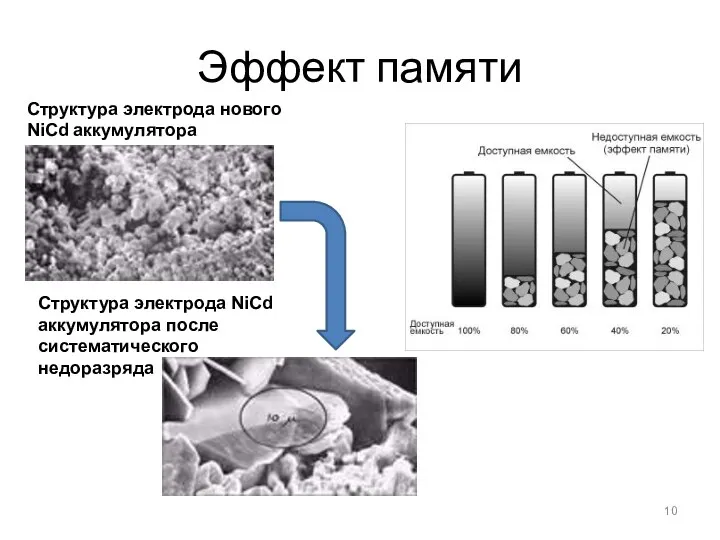
- 10. Эффект памяти Структура электрода нового NiCd аккумулятора Структура электрода NiCd аккумулятора после систематического недоразряда
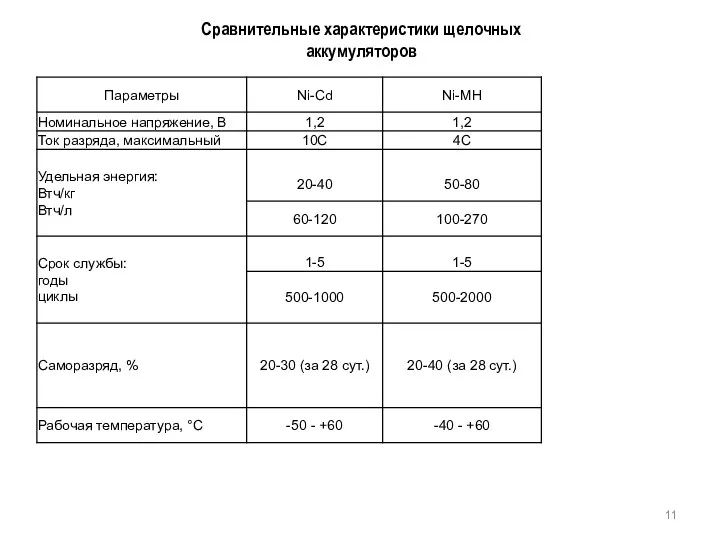
- 11. Сравнительные характеристики щелочных аккумуляторов
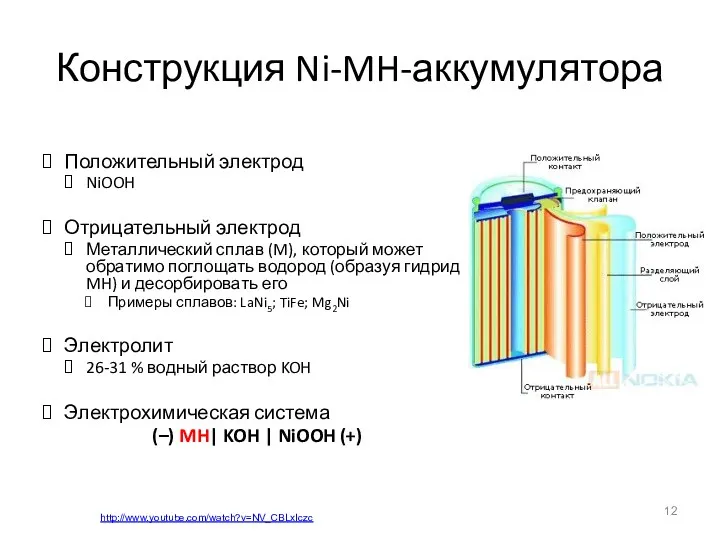
- 12. Конструкция Ni-MH-аккумулятора Положительный электрод NiOOH Отрицательный электрод Металлический сплав (M), который может обратимо поглощать водород (образуя
- 13. Электрохимические процессы Электродные реакции На положительном оксидно-никелевом: Ni(OH)2 + OH- → NiOOH + H2O + e-
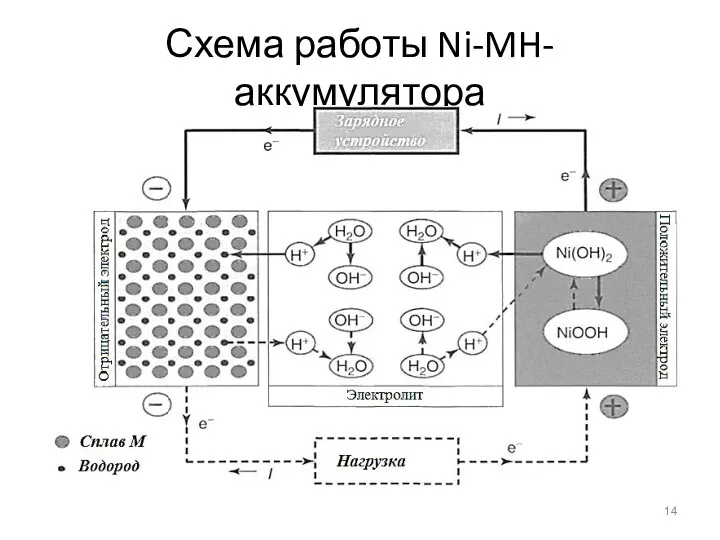
- 14. Схема работы Ni-MH-аккумулятора
- 15. Побочные процессы: перезаряд аккумулятора реакция на положительном электроде: следствие: повышается внутреннее давление, рабочая температура устройства, высыхает
- 16. Побочные процессы: глубокий разряд аккумулятора 1) Истощение материала положительного электрода NiOOH + H2O + e =
- 18. Побочные процессы: глубокий разряд аккумулятора 1) Истощение материала положительного электрода NiOOH + H2O + e =
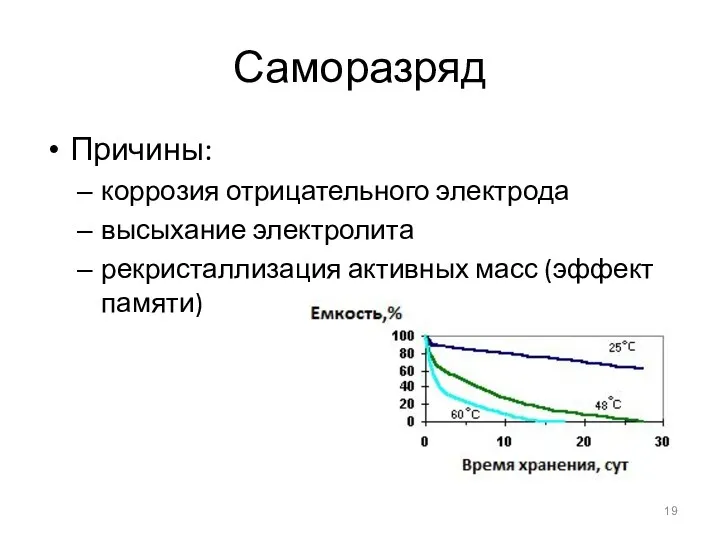
- 19. Саморазряд Причины: коррозия отрицательного электрода высыхание электролита рекристаллизация активных масс (эффект памяти)
- 20. Применение Аккумуляторы высокой емкости устройства с высоким потреблением энергии в течение короткого времени электроинструмент фотоаппарат плеер
- 22. Скачать презентацию













 Работа и мощность электрического тока
Работа и мощность электрического тока Элементы квантовой биофизики
Элементы квантовой биофизики Внутренняя энергия тела
Внутренняя энергия тела Участок отгрузки ЛПЦ-10. Контролёр в производстве черных металлов
Участок отгрузки ЛПЦ-10. Контролёр в производстве черных металлов Термодинамика ионных систем
Термодинамика ионных систем Методы измерения плотности материалов
Методы измерения плотности материалов Элементарные излучатели электромагнитного поля. Электромагнитное поле плоских излучающих раскрывов
Элементарные излучатели электромагнитного поля. Электромагнитное поле плоских излучающих раскрывов Количество теплоты
Количество теплоты Авиационный механик (авиационный техник-механик, авиамеханик)
Авиационный механик (авиационный техник-механик, авиамеханик) Презентация Электрическое поле. Напряженность и потенциал электрического поля
Презентация Электрическое поле. Напряженность и потенциал электрического поля Урок - повторение по теме: Температура тел. Шкалы и приборы измерения температуры, 10 класс.
Урок - повторение по теме: Температура тел. Шкалы и приборы измерения температуры, 10 класс. Плотность вещества
Плотность вещества Асинхронный двигатель с короткозамкнутым и фазным ротором
Асинхронный двигатель с короткозамкнутым и фазным ротором ОБРАЗОВАТЕЛЬНАЯ РОБОТОТЕХНИКА ВО ВНЕУРОЧНОЙ ДЕЯТЕЛЬНОСТИ ШКОЛЫ ОБРАЗОВАТЕЛЬНАЯ РОБОТОТЕХНИКА ВО ВНЕУРОЧНОЙ ДЕЯТЕЛЬНОСТИ ШКОЛЫ
ОБРАЗОВАТЕЛЬНАЯ РОБОТОТЕХНИКА ВО ВНЕУРОЧНОЙ ДЕЯТЕЛЬНОСТИ ШКОЛЫ ОБРАЗОВАТЕЛЬНАЯ РОБОТОТЕХНИКА ВО ВНЕУРОЧНОЙ ДЕЯТЕЛЬНОСТИ ШКОЛЫ Хроматографические методы анализа и их применение для контроля качества лекарственных средств
Хроматографические методы анализа и их применение для контроля качества лекарственных средств Знатоки физики
Знатоки физики Взаимное притяжение и отталкивание молекул
Взаимное притяжение и отталкивание молекул Реактивное движение.
Реактивное движение. Масса тела. Единицы массы. Измерение массы тела на весах. 7 класс
Масса тела. Единицы массы. Измерение массы тела на весах. 7 класс Механические свойства твердых тел и биологических тканей
Механические свойства твердых тел и биологических тканей Задачи по физике
Задачи по физике Электризация тел. Электроскоп. Проводники и диэлектрики
Электризация тел. Электроскоп. Проводники и диэлектрики Общие принципы нормирования
Общие принципы нормирования Электротехника және электроника. Трансформаторлар
Электротехника және электроника. Трансформаторлар Лучевая обработка материалов
Лучевая обработка материалов Ремонт, диагностирование и испытание оборудования после ремонта
Ремонт, диагностирование и испытание оборудования после ремонта Сетевое планирование и управление ремонтом подвижного состава
Сетевое планирование и управление ремонтом подвижного состава Принципы автоматического управления
Принципы автоматического управления