Содержание
- 2. Температура кристаллизации Температура кристаллизации (Ткр) вещества постоянна и характерна для данного вещества при определенном давлении. Она
- 3. Температура кристаллизации При температуре кристаллизации: Теплота плавления практически не зависит от давления. Температура кристаллизации Ткр зависит
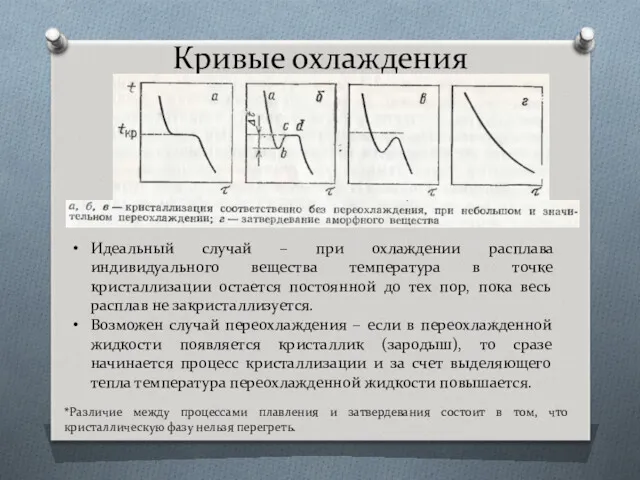
- 4. Кривые охлаждения Идеальный случай – при охлаждении расплава индивидуального вещества температура в точке кристаллизации остается постоянной
- 5. Правило фаз Гиббса Связь между числом степеней свободы, числом компонент и числом фаз при термодинамическом равновесии
- 6. Однокомпонентные системы Нонвариантное равновесие – точка А (тройная точка) Моновариантное равновесие – линии ВА (кривая возгонки),
- 7. Бинарные системы Рассмотрим конденсированные системы (в равновесии учувствуют только жидкие и твердые фазы). Парциальное давление пара
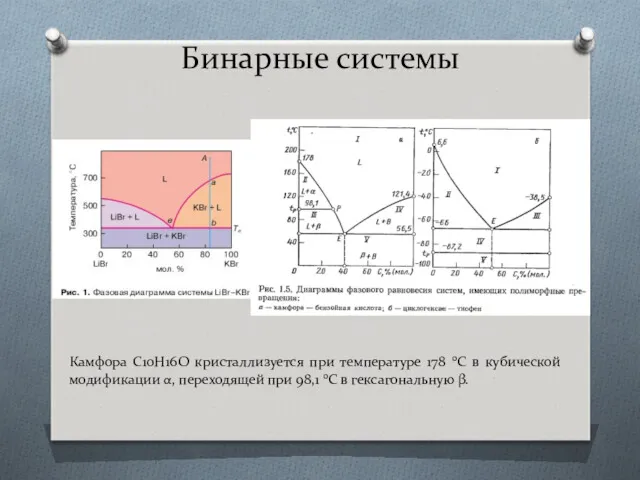
- 8. Бинарные системы Камфора C10H16O кристаллизуется при температуре 178 0С в кубической модификации α, переходящей при 98,1
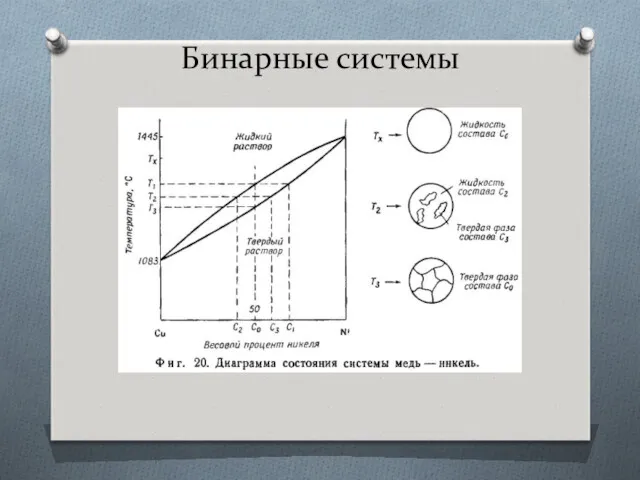
- 9. Бинарные системы Системы с неограниченной растворимостью компонентов в твердом растворе Такие системы обычно образуются веществами, близкими
- 10. Бинарные системы
- 11. Бинарные системы Системы с ограниченной растворимостью компонентов в твердом растворе При определенной температуре имеется область существования
- 12. Изоморфизм Изоморфизм – взаимное замещение атомов (или их групп) разных химических элементов в эквивалентных позициях кристаллической
- 13. Твердые растворы Твердыми растворами называют однородные системы переменного состава, состоящие из двух или более компонентов. Твердые
- 14. Твердые растворы замещения Типы замещений: Нормальное замещение а) Простое замещение (изовалетное). Например, Аl2O3 и Сг2O3 (структура
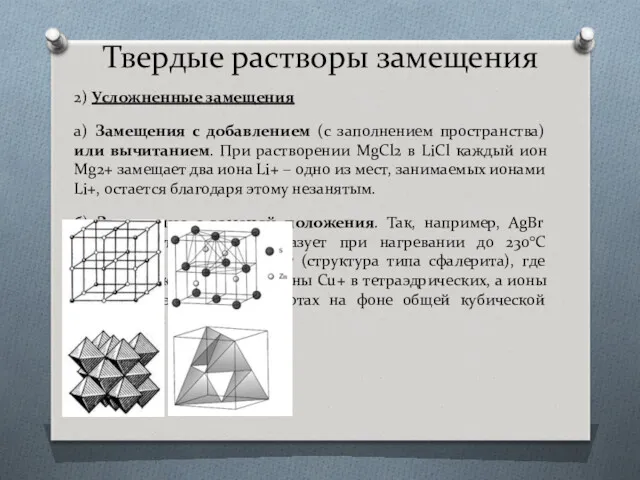
- 15. Твердые растворы замещения 2) Усложненные замещения а) Замещения с добавлением (с заполнением пространства) или вычитанием. При
- 16. Условия образования твердых растворов Образование или отсутствие твердого раствора определяется конкуренцией двух основных факторов противоположной направленности:
- 17. Эмпирические правила изоморфизма
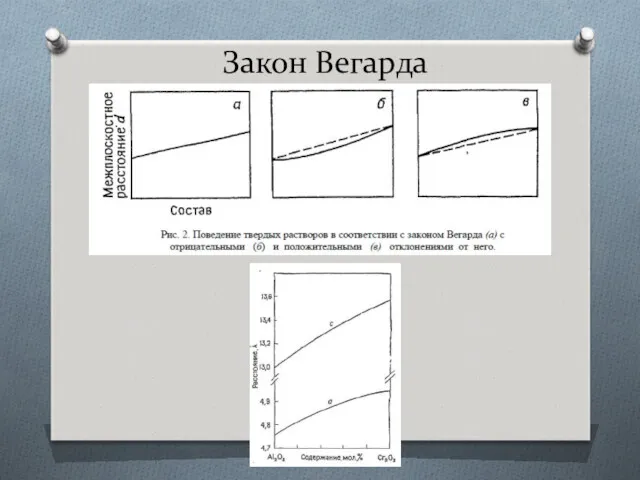
- 18. Закон Вегарда
- 19. Эмпирические правила изоморфизма
- 20. Учет электроотрицательности Электроотрицательность – величина, характеризующая способность атома к поляризации ковалентных связей. Изоморфная взаимозаместимость тем меньше,
- 21. Учет электроотрицательности Правило полярности Гольдшмидта–Ферсмана Ион с меньшим радиусом или бóльшим зарядом входит как примесь в
- 22. Учет электроотрицательности «Звезды изоморфизма». Правило кристаллохимической компенсации. Если Ва2+ замещается на Ln3+, то лучшей компенсацией избыточной
- 23. Кинетика кристаллизации возникновение зародыша новой фазы его дальнейший рост Зарождение кристалла Гомогенное зарождение кристаллов Самопроизвольное образование
- 24. Гомогенное зарождение Кристаллизация возможна при понижении энергии Гиббса все системы. Объемный эффект: Поверхностный эффект:
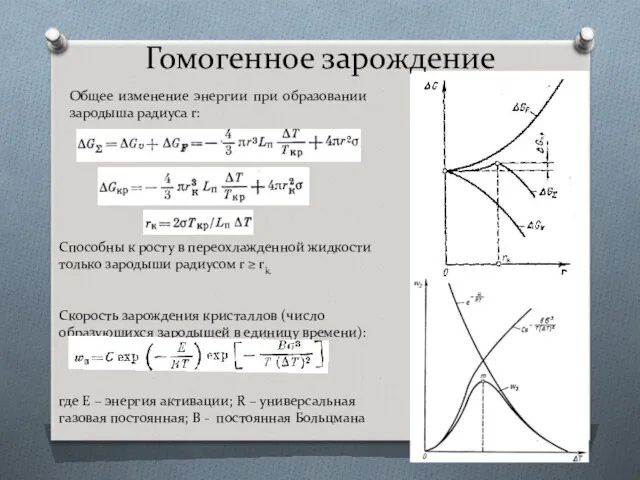
- 25. Гомогенное зарождение Общее изменение энергии при образовании зародыша радиуса r: Способны к росту в переохлажденной жидкости
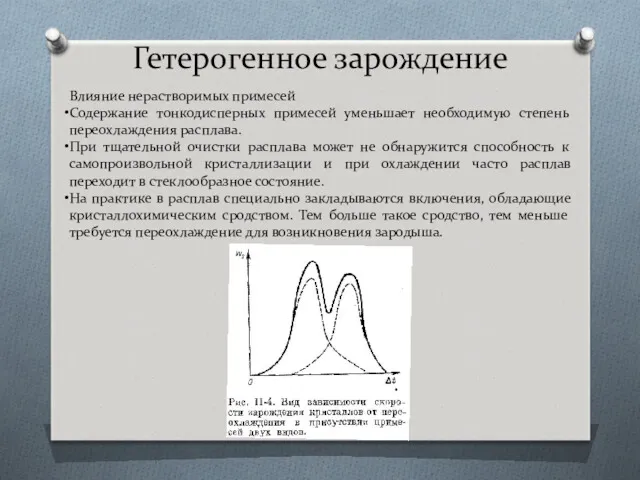
- 26. Гетерогенное зарождение Влияние нерастворимых примесей Содержание тонкодисперных примесей уменьшает необходимую степень переохлаждения расплава. При тщательной очистки
- 27. Гетерогенное зарождение Влияние растворимых примесей Если примеси растворимы в жидкой фазе и нерастворимы в кристаллической, то
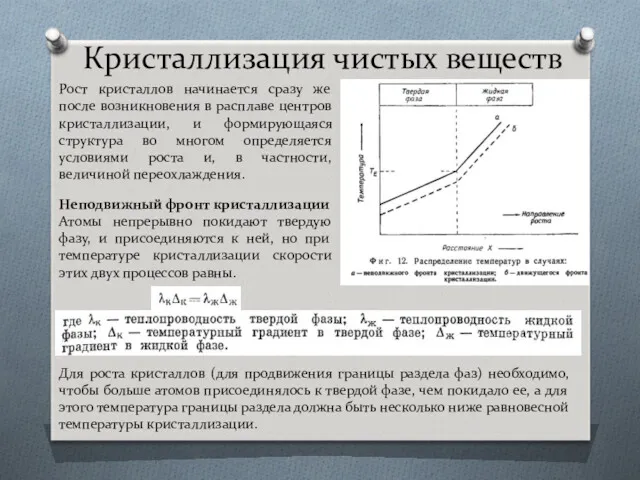
- 28. Кристаллизация чистых веществ Рост кристаллов начинается сразу же после возникновения в расплаве центров кристаллизации, и формирующаяся
- 29. Кристаллизация чистых веществ Рост кристаллов при положительном температурном градиенте в жидкости В процессе затвердевания выделяется теплота
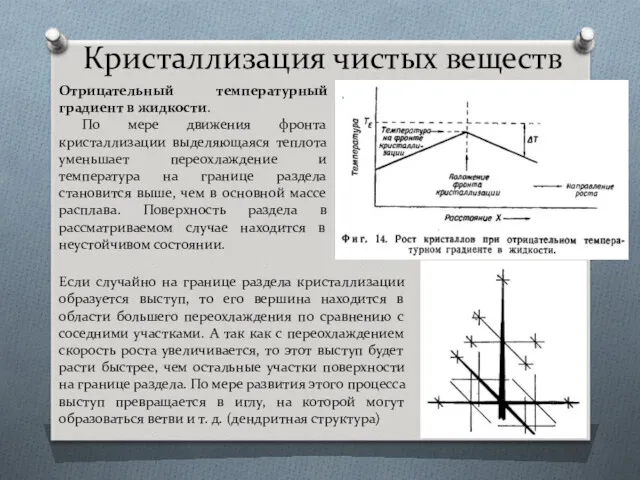
- 30. Кристаллизация чистых веществ Отрицательный температурный градиент в жидкости. По мере движения фронта кристаллизации выделяющаяся теплота уменьшает
- 31. Кристаллизация бинарных расплавов Концентрационное переохлаждение В чистых веществах возникает только термическое переохлаждение расплава, в сплавах же
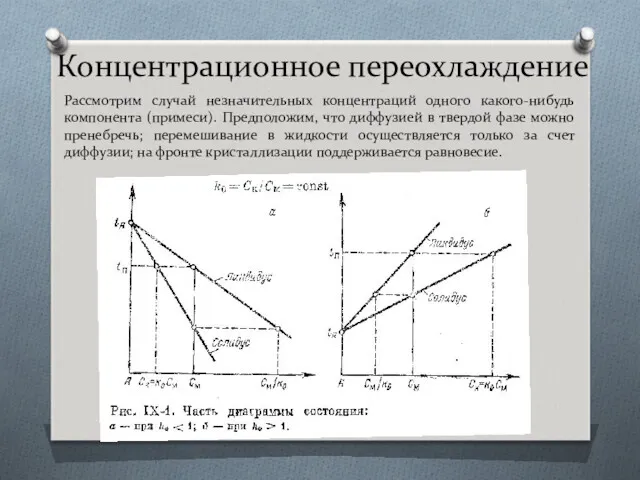
- 32. Концентрационное переохлаждение Рассмотрим случай незначительных концентраций одного какого-нибудь компонента (примеси). Предположим, что диффузией в твердой фазе
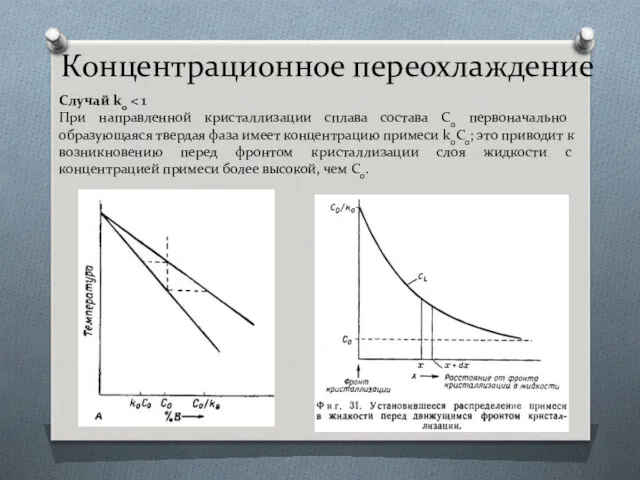
- 33. Концентрационное переохлаждение Случай k0 При направленной кристаллизации сплава состава Со первоначально образующаяся твердая фаза имеет концентрацию
- 34. Концентрационное переохлаждение Случай k0
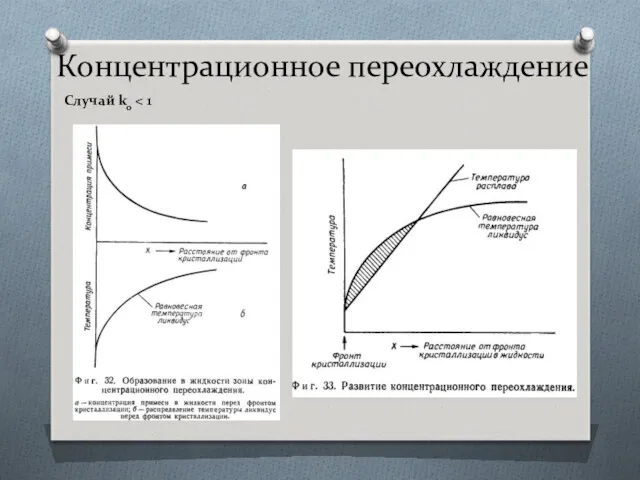
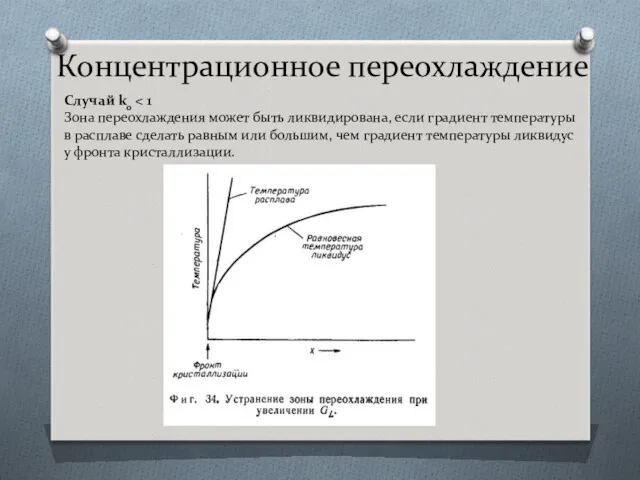
- 35. Концентрационное переохлаждение Случай k0 Зона переохлаждения может быть ликвидирована, если градиент температуры в расплаве сделать равным
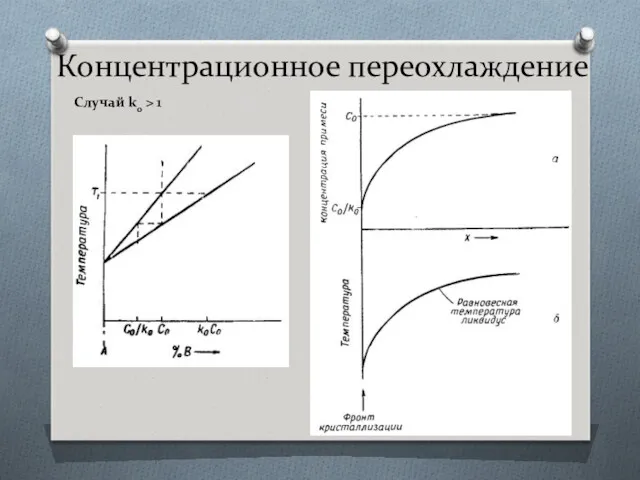
- 36. Концентрационное переохлаждение Случай k0 > 1
- 37. Структура поверхности раздела При наличии концентрационного переохлаждения поверхность раздела неустойчива. При k0 При k0 > 1
- 38. Направленная кристаллизация Охлаждение образца в процессе направленной кристаллизации обычно производят так, что фронт кристаллизации постепенно передвигается
- 39. Распределение примеси При полном перемешивании жидкой фазы Уравнение материального баланса: Vп – полный объем образца CF
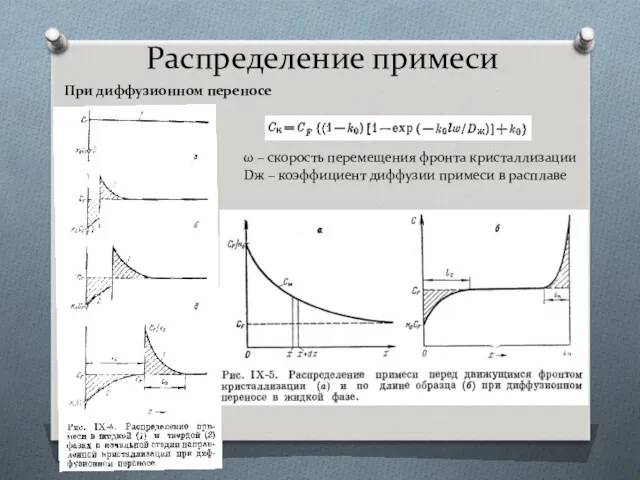
- 40. Распределение примеси При диффузионном переносе ω – скорость перемещения фронта кристаллизации Dж – коэффициент диффузии примеси
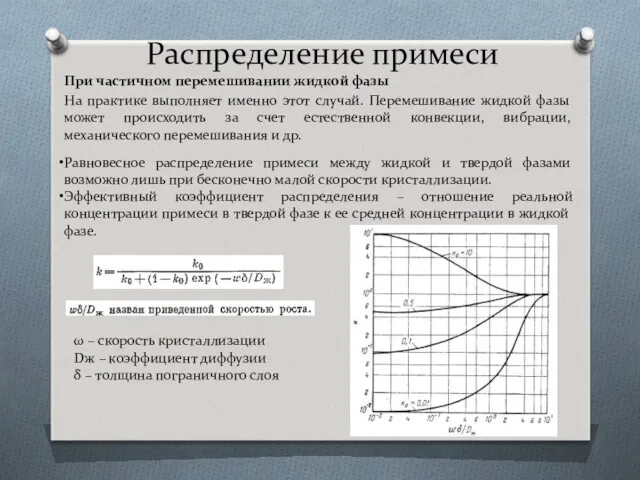
- 41. Распределение примеси При частичном перемешивании жидкой фазы На практике выполняет именно этот случай. Перемешивание жидкой фазы
- 42. Зонная плавка В основном зонная плавка используется для очистки образцов от примеси. При зонной плавке образуются
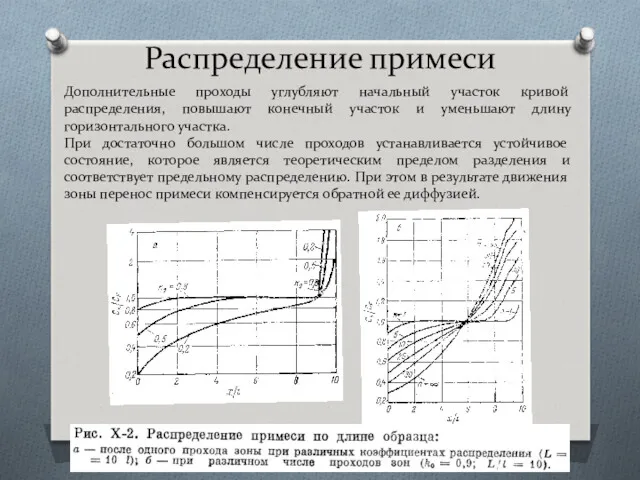
- 43. Распределение примеси Дополнительные проходы углубляют начальный участок кривой распределения, повышают конечный участок и уменьшают длину горизонтального
- 44. Дефекты. Сегрегация примесей. Различают линейные и поверхностные дефекты. Линейные дефекты – дислокации. Механизмы образования дислокаций: Механические
- 45. Залечивание несплошностей Различают линейные и поверхностные дефекты. Линейные дефекты – дислокации. Механизмы образования дислокаций: Механические деформации,
- 46. Техника кристаллизации расплавов Основная задача – обеспечение монокристаллического роста. Кристаллизация из расплава сопровождается рядом физических и
- 47. Состояние расплава Кристаллизацию проводят в вакууме или при нормальном давлении. Подбирают максимально допустимую температуру перегрева расплава
- 48. Материал контейнера Химические силы связи материала контейнера должны резко отличаться по своей природе от химических сил
- 49. Материал контейнера
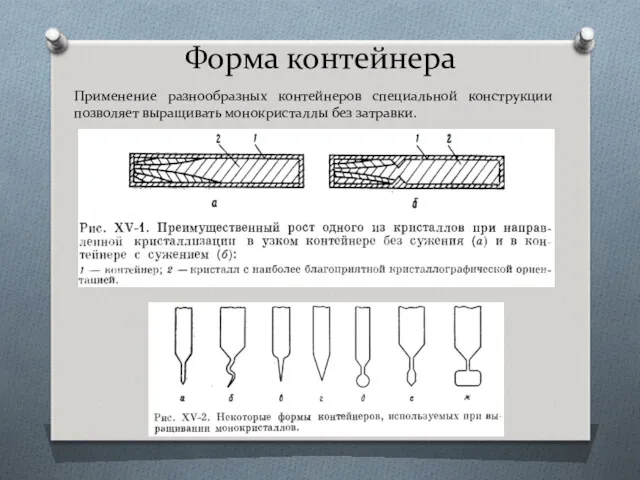
- 50. Форма контейнера Применение разнообразных контейнеров специальной конструкции позволяет выращивать монокристаллы без затравки.
- 51. Атмосфера кристаллизации Роль атмосферы кристаллизации может быть пассивной и активной; в последнем случае атмосфера взаимодействует с
- 52. Основные методы Методы с большим объёмом расплава (методы Киропулоса, Чохральского, Стокбаргера, Бриджмена) Методы с малым объемом
- 53. Метод Обреимова-Шубникова Охлаждение производится только через нижний конец трубки и температура расплава над фронтом кристаллизации все
- 54. Метод Бриджмана 1) Передвижение фронта кристаллизации путем медленного опускания контейнера с расплавов в неподвижной печи (от
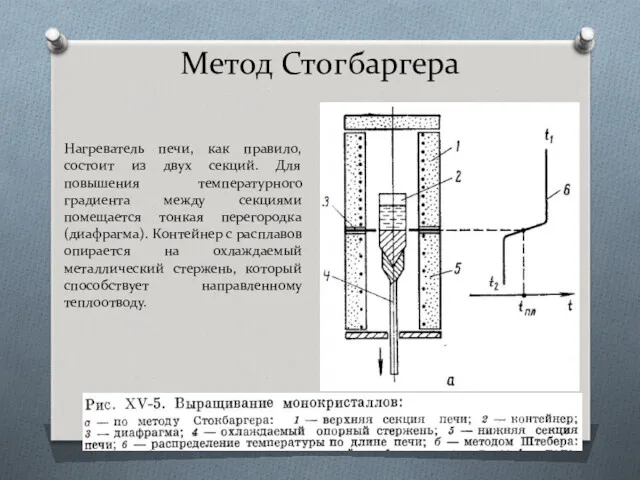
- 55. Метод Стогбаргера Нагреватель печи, как правило, состоит из двух секций. Для повышения температурного градиента между секциями
- 56. Метод Киропулоса Температура расплава в тигле поддерживается несколько выше точки плавления данного вещества. Охлаждение расплава производится
- 57. Метод Чохральского Особенность – одновременно с медленным вытягиванием из расплава монокристалл вращается около его вертикальной оси.
- 58. Метод Чохральского Y3Al5O12, LiNdO3, Si. Существенный недостаток метода состоит в наличии разогреваемого контейнера, который может явиться
- 59. Метод Вернейля Метод Вернейля (методом плавления в пламени) заключается в том, что вещество в виде порошка
- 60. Метод Вернейля Преимущества: отсутствие контейнера, в результате чего снимаются проблемы физико-химического взаимодействия расплава с материалом контейнера,
- 61. Метод зонной плавки Заключается в последовательном проплавлении слитка исходного вещества. Преимущество метода зонной плавки заключается в
- 62. Кристаллизация из раствора Под кристаллизацией из растворов подразумевается рост кристалла, химический состав которого заметно отличается от
- 63. Кристаллизация из раствора По принципу создания пересыщений способы кристаллизации из растворов разделяются на несколько групп. Кристаллизация
- 64. Кристаллизация из газовой фазы Преимущества: практически для любого вещества может быть подобран процесс роста монокристалла малая
- 66. Скачать презентацию












































 Проектирование и расчет механизмов передвижения
Проектирование и расчет механизмов передвижения Strings, Gauge Fields and Duality
Strings, Gauge Fields and Duality Строение вещества.
Строение вещества. Модель строения твердых тел
Модель строения твердых тел Физико-технические основы электроэнергетики
Физико-технические основы электроэнергетики Взаимодействие тел. Инерция. Масса тела. Сила
Взаимодействие тел. Инерция. Масса тела. Сила Сопротивление проводника
Сопротивление проводника Жидкое состояние вещества
Жидкое состояние вещества Теоретическая механика. Динамика. (Лекции 1-6)
Теоретическая механика. Динамика. (Лекции 1-6) Подготовка к ОГЭ по физике на уроке. Решение задач по физике различного типа и уровня сложности
Подготовка к ОГЭ по физике на уроке. Решение задач по физике различного типа и уровня сложности презентация к уроку в 7 классе по темеплавание тел
презентация к уроку в 7 классе по темеплавание тел Силовой анализ механизмов
Силовой анализ механизмов Решение задач по темам Архимедова сила, Условия плавания тел. 7 класс
Решение задач по темам Архимедова сила, Условия плавания тел. 7 класс ПРЕЗЕНТАЦИЯ ТЕСТ ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ
ПРЕЗЕНТАЦИЯ ТЕСТ ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ Плазма
Плазма Напряженность магнитного поля
Напряженность магнитного поля Компания Volat
Компания Volat Презентация для урока по теме Изопроцессы в газах
Презентация для урока по теме Изопроцессы в газах Электромагнитное излучение, его влияние на человека и способы защиты от электромагнитного излучения
Электромагнитное излучение, его влияние на человека и способы защиты от электромагнитного излучения Назначение и устройство КМ 394
Назначение и устройство КМ 394 Электрический ток
Электрический ток Разработка урока на тему : Плотность вещества
Разработка урока на тему : Плотность вещества Предмет фізики
Предмет фізики Разнообразие форм домашней работы учащихся по физике.
Разнообразие форм домашней работы учащихся по физике. Стоячие волны. Колебания и волны 14
Стоячие волны. Колебания и волны 14 Режущий инструмент. Основные функции. Основы теории режущих инструментов
Режущий инструмент. Основные функции. Основы теории режущих инструментов Решение задач на расчет массы и объёма тела по его плотности
Решение задач на расчет массы и объёма тела по его плотности Influence of supply voltage on torque–speed curve
Influence of supply voltage on torque–speed curve