Первый закон термодинамики. Применение первого закона термодинамики к различным процессам презентация
Содержание
- 3. Энергия в природе не возникает из ничего и не исчезает: количество энергии неизменно, она только переходит
- 4. Закон сохранения энергии является фундаментальным законом природы. Он выполняется всегда и везде, применительно к любым явлениям
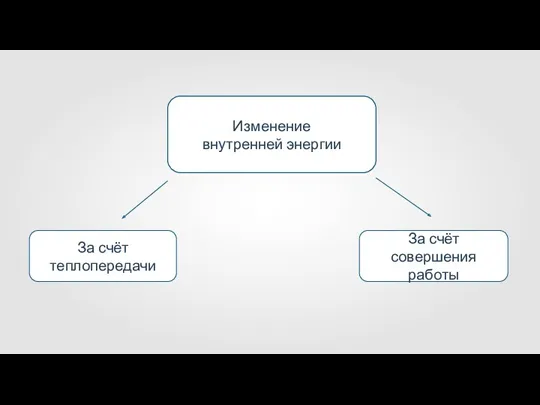
- 6. Изменение внутренней энергии
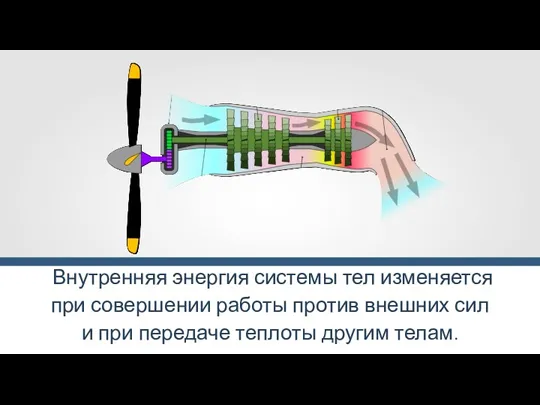
- 8. Изменение внутренней энергии системы при переходе её из одного состояния в другое равно сумме работы внешних
- 9. Можно рассмотреть работу системы над внешними силами. Первый закон термодинамики
- 10. Количество теплоты, переданное системе, идёт на совершение системой работы против внешних сил и на увеличение её
- 11. Если система является изолированной, то внешние тела не взаимодействуют с системой, а, значит, работа внешних сил
- 13. Из первого закона термодинамики следует, что создание вечного двигателя невозможно. Если к системе не поступает энергия,
- 15. Первый закон термодинамики позволяет делать важные выводы о характере протекающих процессов.
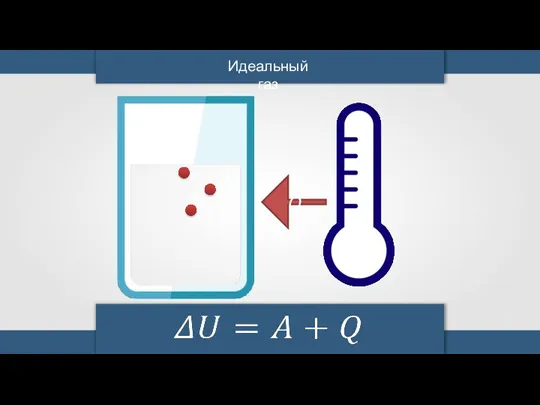
- 16. Идеальный газ При изохорном процессе объём газа не меняется, и поэтому работа газа равна нолю.
- 17. Идеальный газ Q
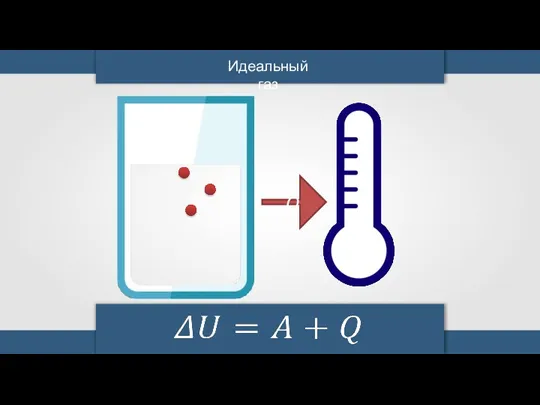
- 18. Идеальный газ Q
- 19. Идеальный газ При изотермическом процессе температура газа не изменяется, значит, не меняется внутренняя энергия идеального газа.
- 20. Согласно первому закону термодинамики, всё переданное газу количество теплоты идёт на совершение работы газа против внешних
- 21. При изобарном процессе согласно первому закону термодинамики, передаваемое газу количество теплоты идёт на изменение его внутренней
- 22. При адиабатном процессе по первому закону термодинамики изменение внутренней энергии происходит только за счёт совершения работы.
- 23. Если внешние тела совершают над газом положительную работу, его внутренняя энергия увеличивается, температура газа повышается.
- 24. Если внешние тела совершают над газом положительную работу, его внутренняя энергия увеличивается, температура газа повышается. И
- 27. Уровень конденсации Пар
- 28. После наступления теплового равновесия, по первому закону термодинамики, увеличение внутренней энергии ложки в стакане будет равно
- 29. В изолированной системе суммарная внутренняя энергия не меняется. А, значит, и сумма количеств теплоты, полученных и
- 30. Уравнение теплового баланса
- 32. Скачать презентацию
























 Электромагнитная индукция 11 класс
Электромагнитная индукция 11 класс Ця важка робота
Ця важка робота Проектирование и производство изделий интегральной электроники. Нанесение тонких плёнок
Проектирование и производство изделий интегральной электроники. Нанесение тонких плёнок Теория многофазной фильтрации. (Лекция 3)
Теория многофазной фильтрации. (Лекция 3) Inverzná kinematika – aprox. metóda
Inverzná kinematika – aprox. metóda Электрические явления. 8 класс
Электрические явления. 8 класс 61f4bb8105f047b8922e06e3e916ed53
61f4bb8105f047b8922e06e3e916ed53 Поршеньді компрессорларды жөндеу
Поршеньді компрессорларды жөндеу Общая физика. (Лекция 1) Классическая механика
Общая физика. (Лекция 1) Классическая механика Буландыру. Буландыру әдістері
Буландыру. Буландыру әдістері Тест по физике 8 класс по теме Внутренняя энергия.Виды теплопередачи
Тест по физике 8 класс по теме Внутренняя энергия.Виды теплопередачи Детали машин
Детали машин Оптичні ілюзії
Оптичні ілюзії Презентация к уроку физики 10 класс Движение по окружности
Презентация к уроку физики 10 класс Движение по окружности Лекция 1. Общие принципы построения электропривода
Лекция 1. Общие принципы построения электропривода Рентгеновские методы спектрального анализа
Рентгеновские методы спектрального анализа Поляризация света
Поляризация света ЭСПРИ. Электронный справочник инженера
ЭСПРИ. Электронный справочник инженера Магнітне поле
Магнітне поле Физика и музыка
Физика и музыка Мастер класс Реализация компетентностного подхода в преподавании физики через организацию самостоятельных исследований при решении физических задач
Мастер класс Реализация компетентностного подхода в преподавании физики через организацию самостоятельных исследований при решении физических задач Відновлення деталей електролітичними способами. Зміцнення поверхонь
Відновлення деталей електролітичними способами. Зміцнення поверхонь Генерирование электрической энергии. Трансформаторы
Генерирование электрической энергии. Трансформаторы Проблемно-задачный подход обучения физике
Проблемно-задачный подход обучения физике Закон Паскаля, объясняющий процесс передачи давления жидкостями и газами
Закон Паскаля, объясняющий процесс передачи давления жидкостями и газами Сила упругости
Сила упругости Давление. Единицы давления. 7 класс
Давление. Единицы давления. 7 класс Экзамен по дисциплинам Электропривод
Экзамен по дисциплинам Электропривод