Содержание
- 2. Содержание Внутренняя энергия Работа в термодинамике Количество теплоты _________ Определение: Термодинамика – теория тепловых процессов, в
- 3. Внутренняя энергия Определение: Внутренняя энергия тела – это сумма кинетической энергии хаотического теплового движения частиц (атомов
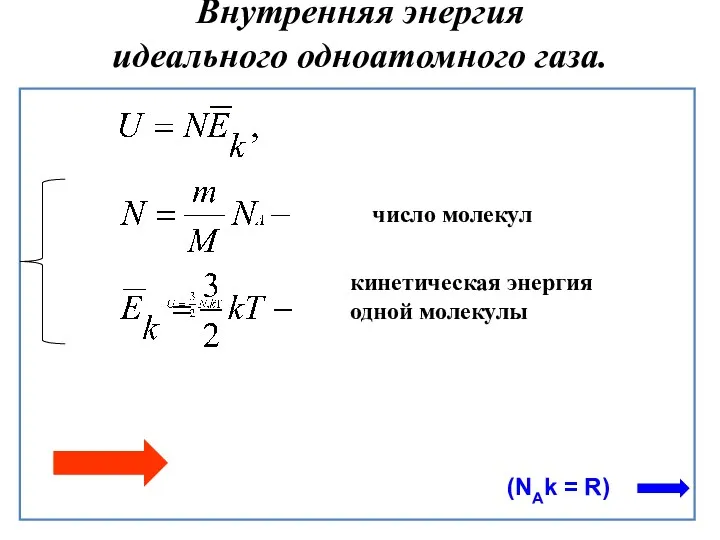
- 4. Внутренняя энергия идеального одноатомного газа. число молекул кинетическая энергия одной молекулы (NAk = R)
- 5. Внутренняя энергия идеального одноатомного газа
- 6. Так как - уравнение Клапейрона – Менделеева, то внутренняя энергия: - для одноатомного газа - для
- 7. В общем виде: где i – число степеней свободы молекул газа (i = 3 для одноатомного
- 8. Изменение внутренней энергии:
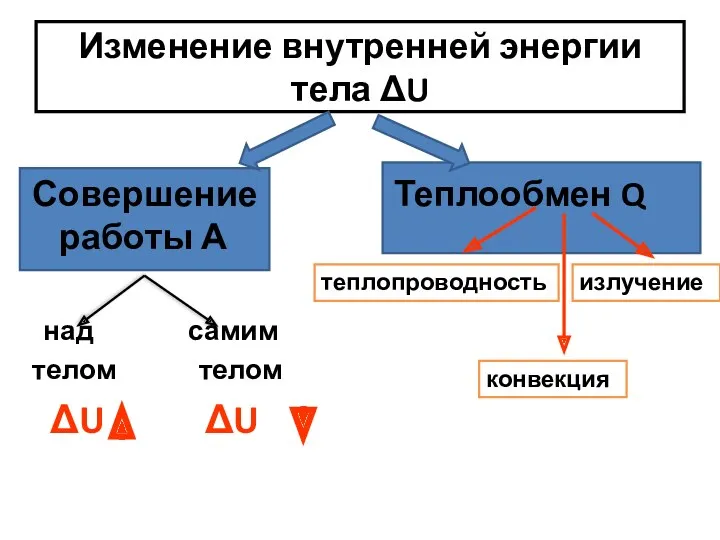
- 10. Изменение внутренней энергии тела ΔU Совершение работы А над самим телом телом ΔU ΔU Теплообмен Q
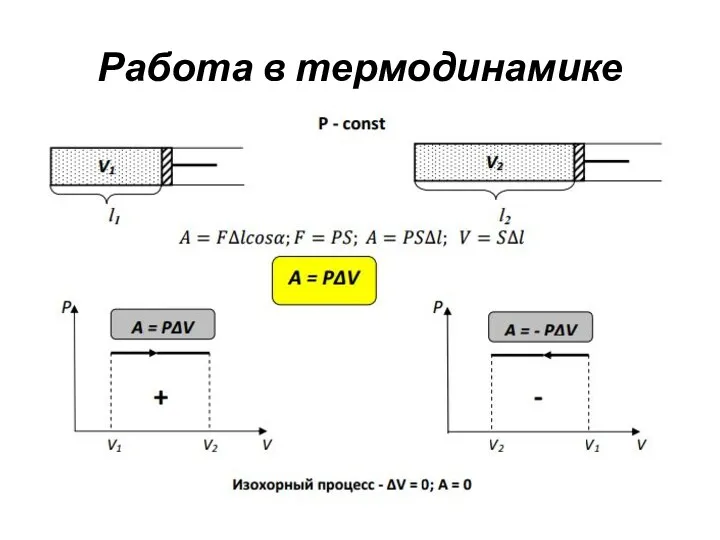
- 11. Работа в термодинамике
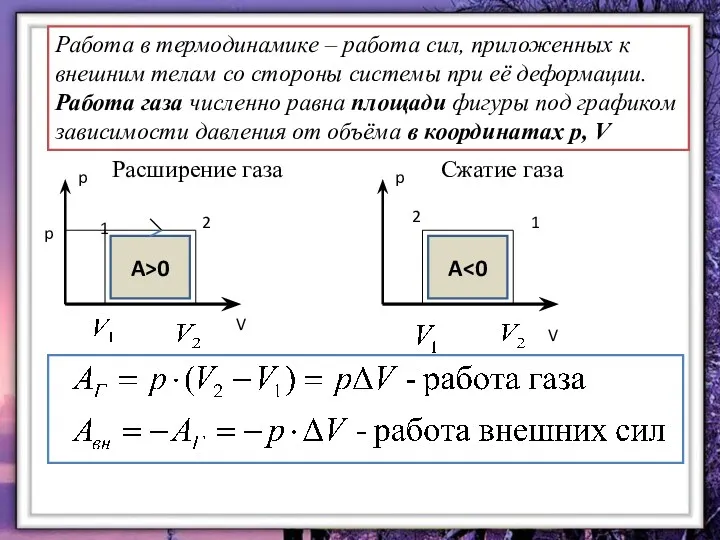
- 12. Работа в термодинамике – работа сил, приложенных к внешним телам со стороны системы при её деформации.
- 13. Работа в термодинамике Работа газа: Работа внешних сил: Работа А, совершаемая внешними телами над газом, отличается
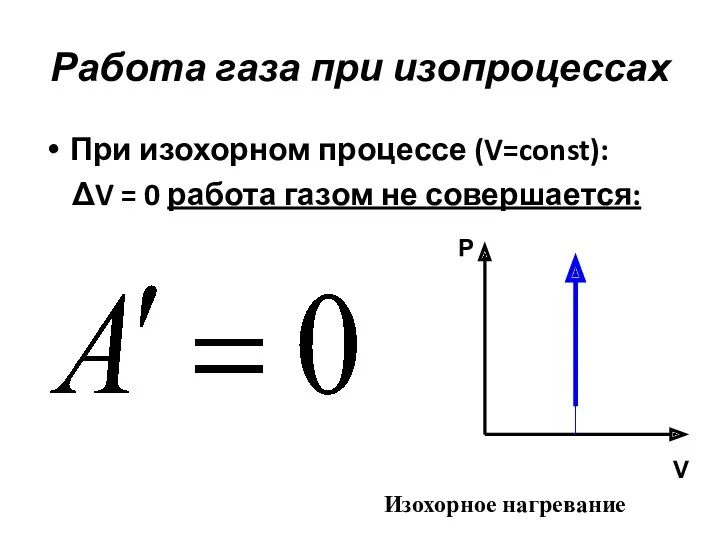
- 14. Работа газа при изопроцессах При изохорном процессе (V=const): ΔV = 0 работа газом не совершается: P
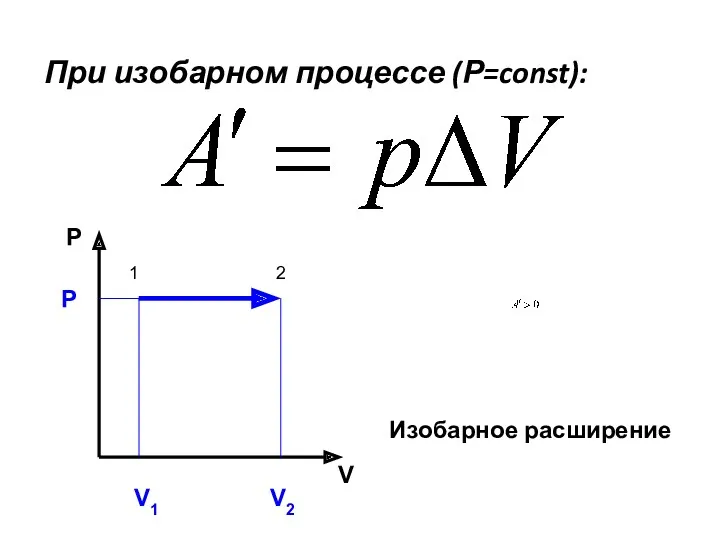
- 15. При изобарном процессе (Р=const): P V V1 V2 P Изобарное расширение 1 2
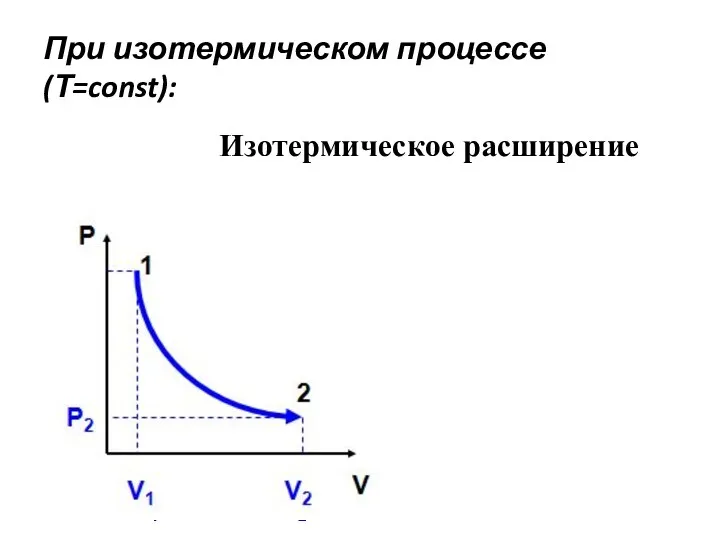
- 16. При изотермическом процессе (Т=const): P V Изотермическое расширение Р2 1 2 V1 V2
- 19. Количество теплоты – часть внутренней энергии, которую тело получает или теряет при теплопередаче
- 22. Уравнение теплового баланса:
- 23. Первое начало термодинамики.
- 25. Тема: Коэффициент полезного действия (КПД) тепловых двигателей
- 26. Развитие техники зависит от умения использовать громадные запасы внутренней энергии. Использовать эту энергию - это значит
- 27. Тепловой двигатель - устройство, преобразующее внутреннюю энергию топлива в механическую энергию
- 28. Вся ли тепловая энергия превращается в тепловых двигателях в механическую энергию? Любой тепловой двигатель превращает в
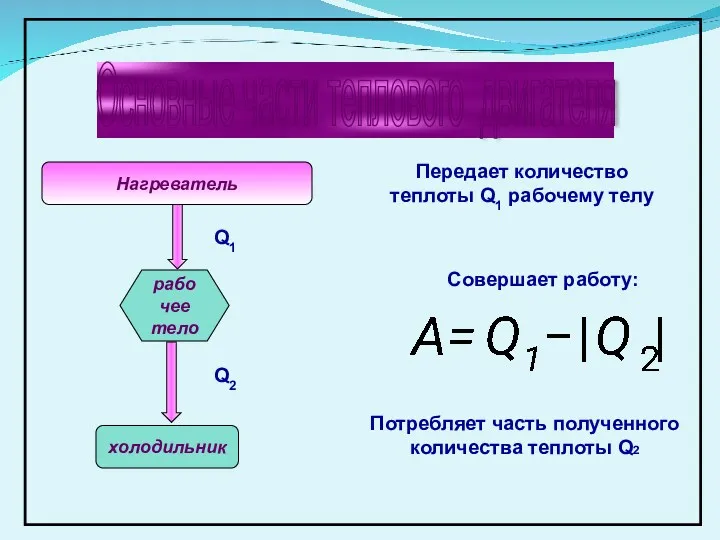
- 29. Основные части теплового двигателя Нагреватель рабочее тело холодильник Передает количество теплоты Q1 рабочему телу Q1 Q2
- 30. КПД замкнутого цикла Q1 – количество теплоты полученное от нагревания Q1>Q2 Q2 - количество теплоты отданное
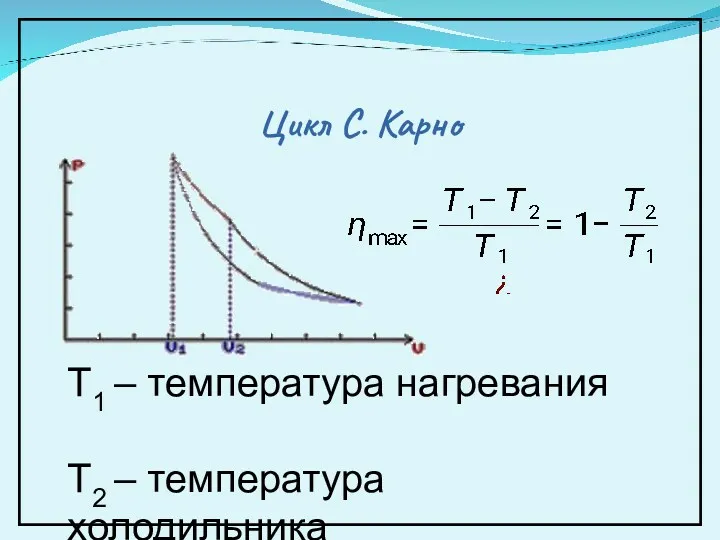
- 32. Цикл C. Карно T1 – температура нагревания Т2 – температура холодильника
- 33. Паровой двигатель Паровая турбина Двигатель внутреннего сгорания Дизельный двигатель Газовая турбина Реактивный двигатель Виды тепловых двигателей
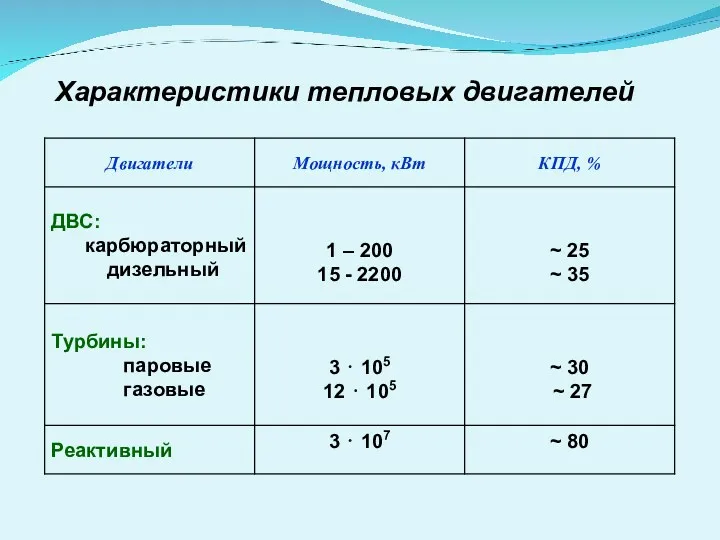
- 34. Характеристики тепловых двигателей
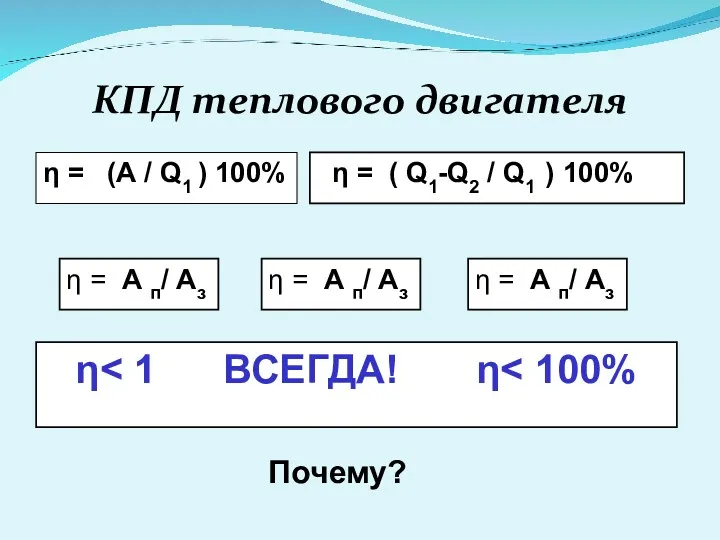
- 35. КПД теплового двигателя η = (А / Q1 ) 100% η = А п/ Аз η
- 36. Один из учеников при решении получил ответ, что КПД теплового двигателя равен 200%. Правильно ли решил
- 38. Скачать презентацию























 Исаак Ньютон
Исаак Ньютон Пара сил. Момент
Пара сил. Момент Конвекция. Конвекция как способ теплопередачи. Конвекция в жидкостях и газах
Конвекция. Конвекция как способ теплопередачи. Конвекция в жидкостях и газах Сила трения
Сила трения Современные попытки создания вечного двигателя
Современные попытки создания вечного двигателя Презентация по физике 7 класс. Тема: Плотность вещества
Презентация по физике 7 класс. Тема: Плотность вещества Модальный метод синтеза непрерывных систем
Модальный метод синтеза непрерывных систем Физические свойства
Физические свойства Постоянные магниты. Магнитное поле Земли
Постоянные магниты. Магнитное поле Земли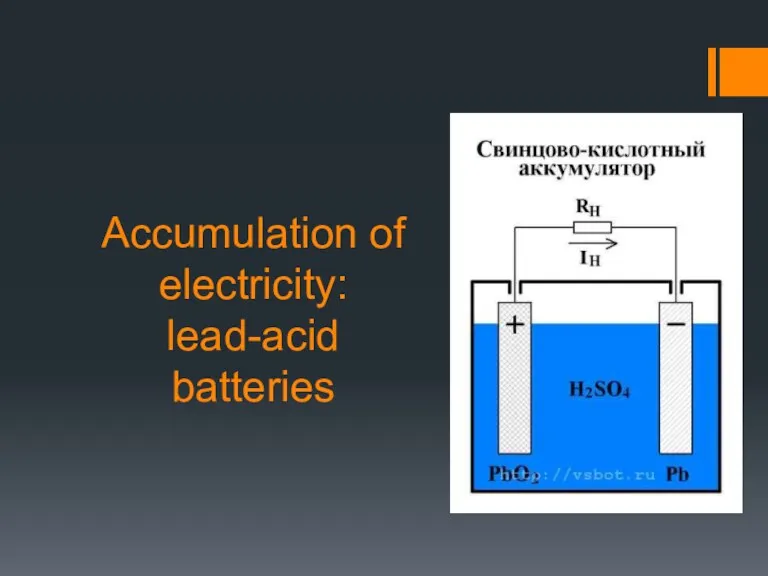 Accumulation of electricity. Leadacid batteries
Accumulation of electricity. Leadacid batteries Тест по физике (10 класс)
Тест по физике (10 класс) Электромагнитная индукция. Опыты Фарадея
Электромагнитная индукция. Опыты Фарадея Естествознание. Почему дует ветер?
Естествознание. Почему дует ветер? Звук. Источники звука
Звук. Источники звука Электростатика. Первоначальная энергия электрона
Электростатика. Первоначальная энергия электрона Сила упругости
Сила упругости Интегрированный урок (физика – экология) в 8 классе по теме: Тепловые двигатели и охрана окружающей среды
Интегрированный урок (физика – экология) в 8 классе по теме: Тепловые двигатели и охрана окружающей среды Принципы радиосвязи
Принципы радиосвязи Построение изображений, даваемых линзой (9 класс)
Построение изображений, даваемых линзой (9 класс) Термометры и их виды
Термометры и их виды Дисперсия света. Цвета тел. Типы оптических спектров
Дисперсия света. Цвета тел. Типы оптических спектров Подшипники качения
Подшипники качения Конструирование и управление БПА
Конструирование и управление БПА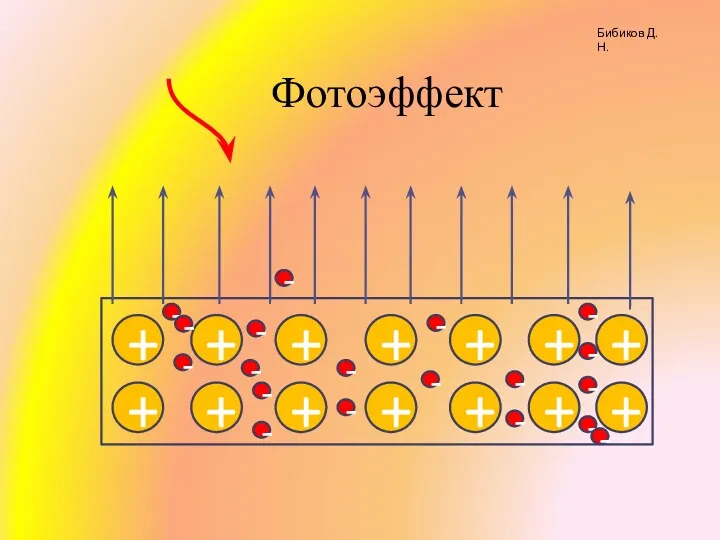 Фотоэффект
Фотоэффект Галерея автомобилей
Галерея автомобилей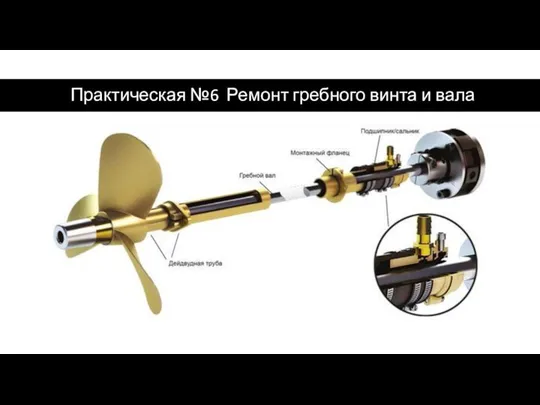 Ремонт гребного винта и вала
Ремонт гребного винта и вала Устройство круиз-контроль на автомобиле
Устройство круиз-контроль на автомобиле Ядерные реакции. Радиоактивность
Ядерные реакции. Радиоактивность