Содержание
- 2. Алкены (этиленовые углеводороды, олефины) - непредельные алифатические углеводороды, молекулы которых содержат двойную связь. Общая формула ряда
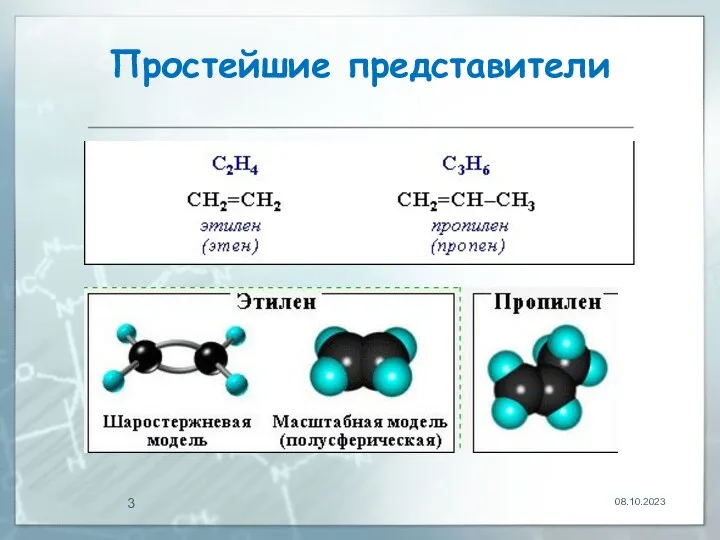
- 3. Простейшие представители 08.10.2023
- 4. Алкены В отличие от предельных углеводородов, алкены содержат двойную связь С=С, которая осуществляется 4-мя общими электронами:
- 5. Строение С=С связи Каждый из атомов имеет по три 2sp2-гибридных орбитали, направленных друг к другу под
- 6. Строение С=С связи Двойная связь является сочетанием σ- и π-связей (хотя она изображается двумя одинаковыми черточками,
- 7. Строение С=С связи Образование связей в молекуле этилена можно изобразить следующей схемой: 08.10.2023
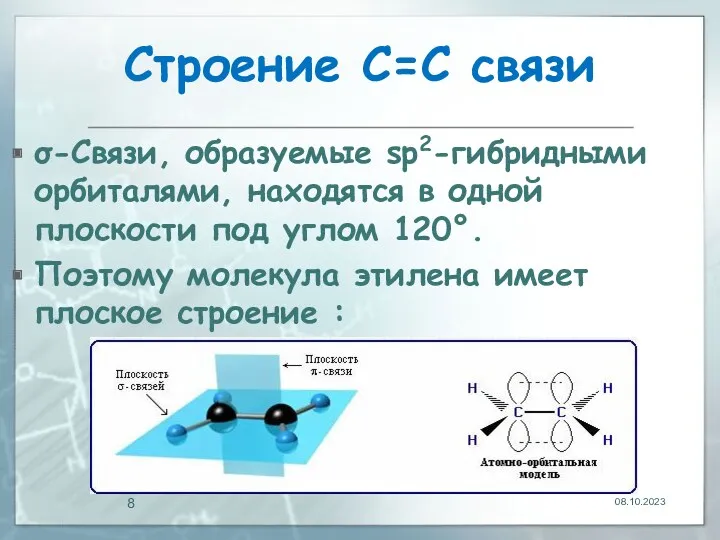
- 8. Строение С=С связи σ-Связи, образуемые sp2-гибридными орбиталями, находятся в одной плоскости под углом 120°. Поэтому молекула
- 9. Номенклатура алкенов названия алкенов производят от названий соответствующих алканов (путем замены суффикса –ан на –ен: 2
- 10. Номенклатура алкенов названия алкенов производят от названий соответствующих алканов (путем замены суффикса –ан на –ен: 2
- 11. Номенклатура алкенов Нумерацию углеродных атомов начинают с ближнего к двойной связи конца цепи. Цифра, обозначающая положение
- 12. Номенклатура алкенов В номенклатуре различных классов органических соединений наиболее часто используются следующие одновалентные радикалы алкенов: 08.10.2023
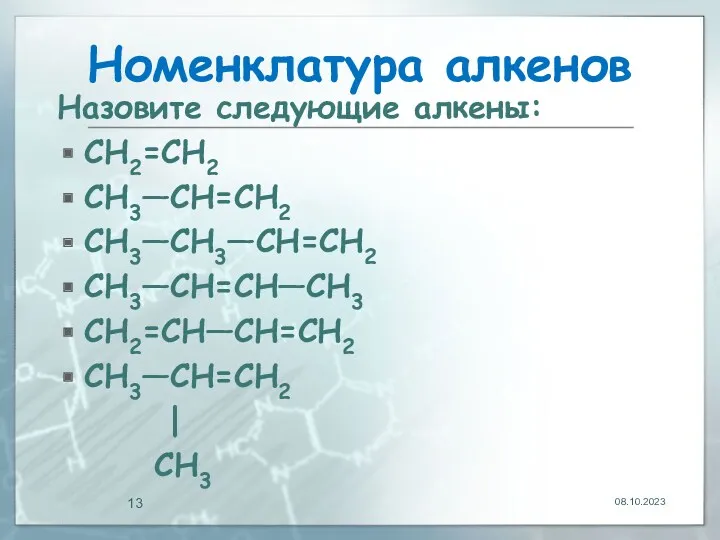
- 13. Номенклатура алкенов Назовите следующие алкены: CH2=CH2 CH3—CH=CH2 CH3—CH3—CH=CH2 CH3—CH=CH—CH3 CH2=CH—CH=CH2 CH3—CH=CH2 | CH3 08.10.2023
- 14. Структурная изомерия алкенов 08.10.2023 1. Изомерия углеродного скелета (начиная с С4Н8):
- 15. Структурная изомерия алкенов 08.10.2023 2. Изомерия положения двойной связи (начиная с С4Н8) :
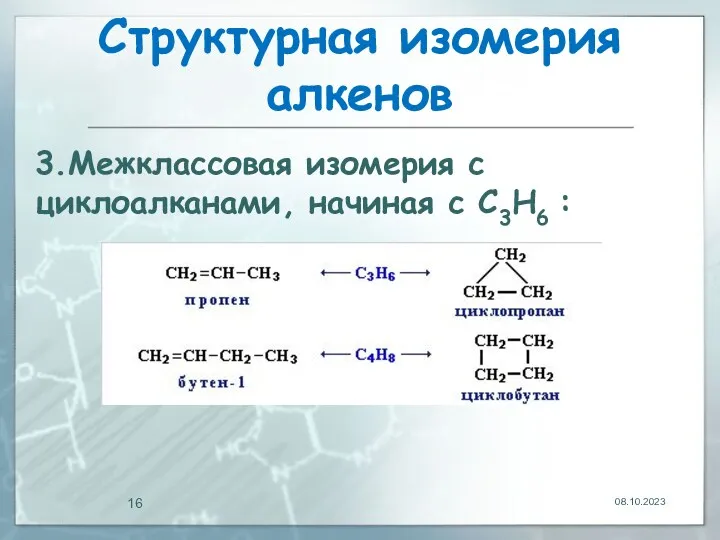
- 16. Структурная изомерия алкенов 08.10.2023 3.Межклассовая изомерия с циклоалканами, начиная с С3Н6 :
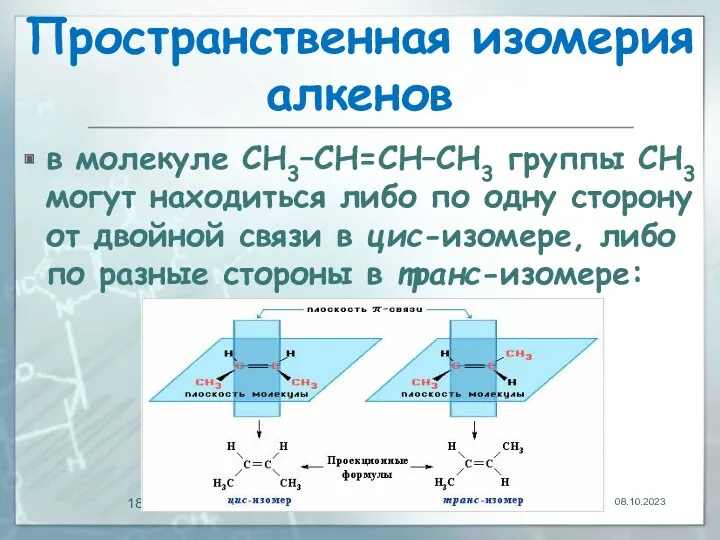
- 17. Пространственная изомерия алкенов Вследствие жесткой закрепленности атомов поворотная изомерия относительно двойной связи не проявляется. Но становится
- 18. Пространственная изомерия алкенов в молекуле СН3–СН=СН–СН3 группы СН3 могут находиться либо по одну сторону от двойной
- 19. Свойства алкенов Физические свойства алкенов изменяются в гомологическом ряду: от С2Н4 до С4Н8 – газы, начиная
- 20. Свойства алкенов Химические свойства алкенов определяются строением и свойствами двойной связи С=С, которая значительно активнее других
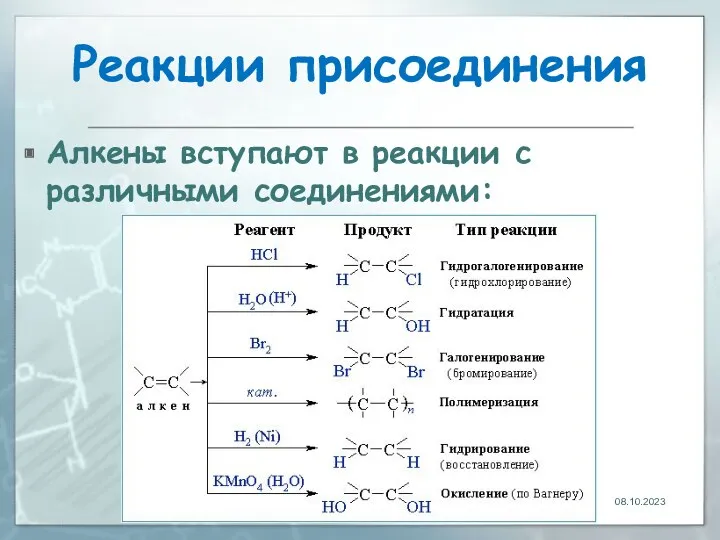
- 21. Реакции присоединения Алкены вступают в реакции с различными соединениями: 08.10.2023
- 22. Гидрирование (присоединение водорода) Алкены взаимодействуют с водородом при нагревании в присутствии металлов Pt, Pd или Ni:
- 23. Гидрирование (присоединение водорода) Присоединение водорода к атомам углерода в алкенах приводит к понижению степени их окисления:
- 24. Гидрирование (присоединение водорода) Эта реакция используется в промышленности для получения высокооктанового топлива: 08.10.2023
- 25. Галогенирование (присоединение галогенов) Присоединение галогенов по двойной связи С=С происходит легко в обычных условиях (при комнатной
- 26. Гидрогалогенирование (присоединение галогеноводородов) Реакция идет по механизму электрофильного присоединения с гетеролитическим разрывом связей. Электрофилом является протон
- 27. Гидратация (присоединение воды) Гидратация происходит в присутствии минеральных кислот по механизму электрофильного присоединения: 08.10.2023
- 28. Гидратация (присоединение воды) Реакция происходит в присутствии минеральных кислот (донора Н+) по механизму электрофильного присоединения: 08.10.2023
- 29. Полимеризация алкенов 1. Полимеризация – реакция образования высокомолекулярного соединения (полимера) путем последовательного присоединения молекул низкомолекулярного вещества
- 30. Полимеризация алкенов Число n называется степенью полимеризации. Реакции полимеризации алкенов идут в результате присоединения по кратным
- 31. Полимеризация алкенов 2. Димеризация алкенов – образование димера в результате реакции присоединения. В присутствии минеральной кислоты
- 32. Получение алкенов I. Крекинг алканов: например: 08.10.2023
- 33. Получение алкенов II. Отщепление (элиминирование) двух атомов или групп атомов от соседних атомов углерода с образованием
- 34. Получение алкенов II. Отщепление : дегидратация (при температуре менее 150°C в присутствии водоотнимающих реагентов ) 08.10.2023
- 35. Получение алкенов II. Отщепление : Дегидрогалогенирование (Дегидрогалогенирование моногалогеналканов при действии спиртового раствора щелочи) 08.10.2023
- 36. Применение алкенов Алкены применяются в качестве исходных продуктов в производстве полимерных материалов (пластмасс, каучуков, пленок) и
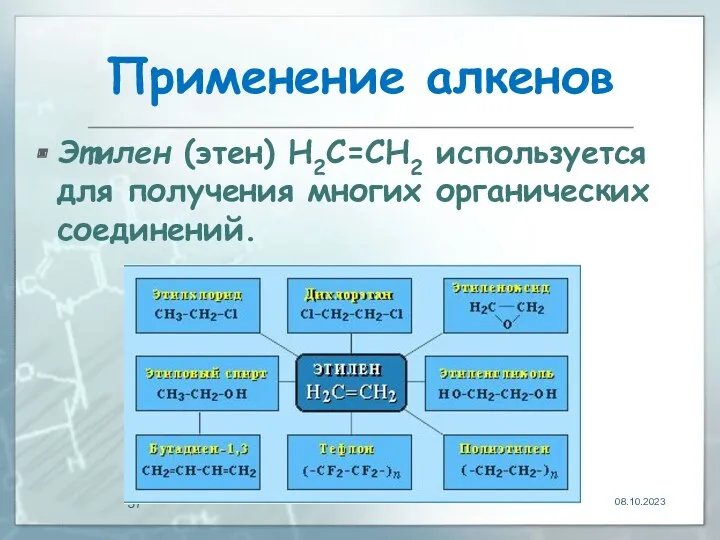
- 37. Применение алкенов Этилен (этен) Н2С=СН2 используется для получения многих органических соединений. 08.10.2023
- 38. Применение алкенов Пропилен (пропен) Н2С=СН2–СН3 и бутилены (бутен-1 и бутен-2) используются для получения спиртов и полимеров.
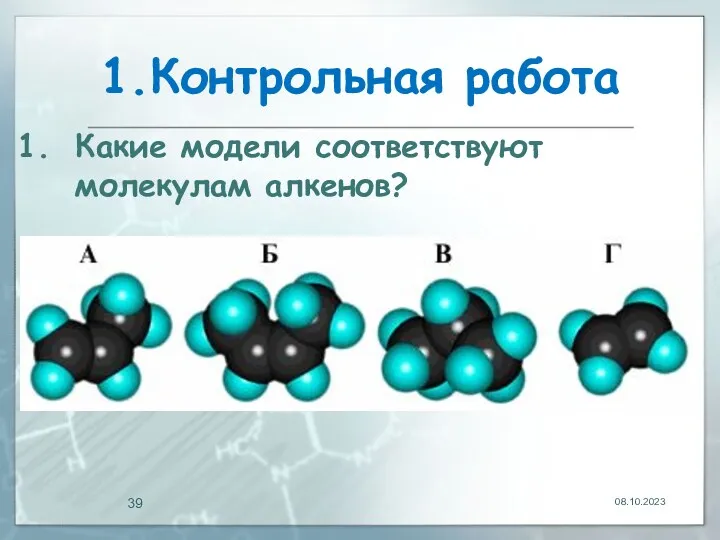
- 39. 1.Контрольная работа 08.10.2023 Какие модели соответствуют молекулам алкенов?
- 40. 2. Контрольная работа 08.10.2023 Дайте названия следующих алкенов, полученных из алканов: - пропан - декан -
- 41. 3.Контрольная работа 08.10.2023 Назовите соединение: Ответ 1: 3-метил-4-этилпентен-2 Ответ 2: 3-метил-2-этилпентен-3 Ответ 3: 3,4-диметилгексен-2 Ответ 4:
- 42. 4. Контрольная работа 08.10.2023 Сколько изомерных алкенов соответствует формуле С4Н8 ? Ответ 1: изомеров нет Ответ
- 43. 5. Контрольная работа 08.10.2023 Двойная связь является сочетанием . . . Ответ 1: двух σ-связей Ответ
- 44. 6. Контрольная работа 08.10.2023 Какова гибридизация атомов углерода в молекуле алкена: Ответ 1: 1 и 4
- 46. Скачать презентацию



































 Химия в жизни общества
Химия в жизни общества Organic molecules
Organic molecules Первичная переработка нефти
Первичная переработка нефти Состав газированной воды
Состав газированной воды Железо. Характеристика химического элемента железа по его положению в ПСХЭ и строению атома
Железо. Характеристика химического элемента железа по его положению в ПСХЭ и строению атома Галогены (солеобразующие)
Галогены (солеобразующие) Склад та властивості основних класів неорганічних сполук
Склад та властивості основних класів неорганічних сполук Научно-исследовательская работа Вся правда о продуктах с сахарозаменителями
Научно-исследовательская работа Вся правда о продуктах с сахарозаменителями Катионы 1, 2 аналитических групп
Катионы 1, 2 аналитических групп Углекислый газ
Углекислый газ Неон. Получение
Неон. Получение Периодическая система Д. И. Менделеева
Периодическая система Д. И. Менделеева Тема 1. Обработка вооружения, техники и обмундирования. Дегазирующие, дезактивирующие и дезинфицирующие вещества и растворы
Тема 1. Обработка вооружения, техники и обмундирования. Дегазирующие, дезактивирующие и дезинфицирующие вещества и растворы
 Химическая связь
Химическая связь Углеводы Cn(H2O)m
Углеводы Cn(H2O)m Генетическая связь между классами органических веществ
Генетическая связь между классами органических веществ Типы химических реакций в органической химии
Типы химических реакций в органической химии СПЛАВЫ. КОРРОЗИЯ МЕТАЛЛОВ
СПЛАВЫ. КОРРОЗИЯ МЕТАЛЛОВ Карбоновые кислоты и их функциональные производные
Карбоновые кислоты и их функциональные производные Хімічні сполуки у побуті
Хімічні сполуки у побуті Основные классы неорганических веществ
Основные классы неорганических веществ Мир первозданной красоты. Природные уникумы Урала
Мир первозданной красоты. Природные уникумы Урала Химический элемент и вещество
Химический элемент и вещество Тема 1. Металлы и сплавы
Тема 1. Металлы и сплавы Влияние спирта на здоровье человека
Влияние спирта на здоровье человека Превращения веществ. Роль химии в жизни человека
Превращения веществ. Роль химии в жизни человека Топливо. Виды топлива. Химический состав топлива. Основные характеристики топлива. Марки топлива
Топливо. Виды топлива. Химический состав топлива. Основные характеристики топлива. Марки топлива