Содержание
- 2. КАТАЛИТИЧЕСКИЙ КРЕКИНГ РИФОРМИНГ ГИДРОКРЕКИНГ РЕАКЦИИ АЛКИЛИРОВАНИЯ СТУПЕНЧАТАЯ ПОЛИМЕРИЗАЦИЯ ИЗОМЕРИЗАЦИЯ Эти превращения протекают в условиях гомогенного и
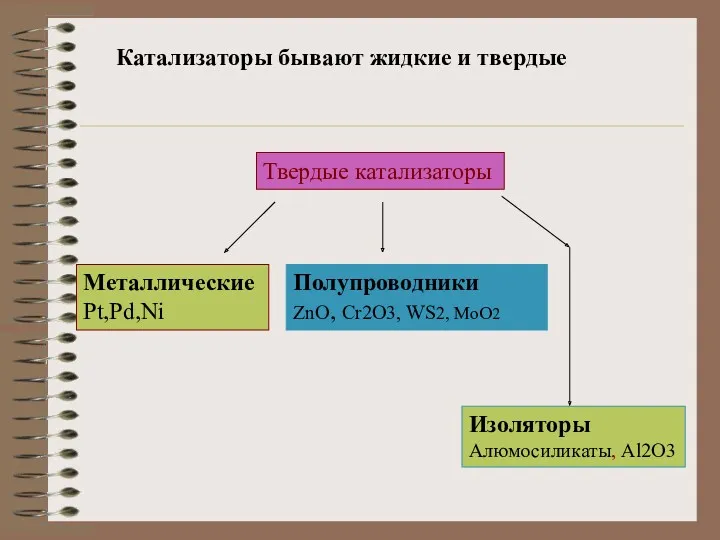
- 3. Катализаторы бывают жидкие и твердые Твердые катализаторы Металлические Pt,Pd,Ni Полупроводники ZnO, Cr2O3, WS2, MoO2 Изоляторы Алюмосиликаты,
- 4. Стадии гетерогенно-каталитических реакций над твердыми катализаторами 1.Диффузия реагентов к поверхности Cat 2. Активированная адсорбция 3. Химическое
- 5. Скорость реакции определяется скоростью наиболее медленной (лимитирующей) стадии 1 Пример: Лимитирующая стадия- диффузия Процесс протекает в
- 6. 2 Пример Лимитирующая стадия - химическая реакция Процесс находится в кинетической области Скорость процесса зависит от
- 7. Продолжительность пребывания молекулы на поверхности кат. выражается: Механизм активированной адсорбции Молекула удерживается на поверхности валентными связями
- 8. Молекула перемещается с одного адсорбционного центра на другой Время жизни на адсорбционном центре τ’=τ’0e Q’/RT Q’-
- 9. КАТАЛИТИЧЕСКИЙ КРЕКИНГ Густавсон (Россия) AlBr3, AlCl3 Создание кат. Крекинга обусловлено Необходимостью : 1. снижения Т и
- 10. Алюмосиликатные катализаторы ( аморфные и кристаллические) Менее активны , чем AlCl3 , но лишены его недостатков
- 11. Условия крекинга на Ал-сил кат: Паровая фаза, 400-500оС, Р- близко к атмосферному Сырье: вакуумные газойли с
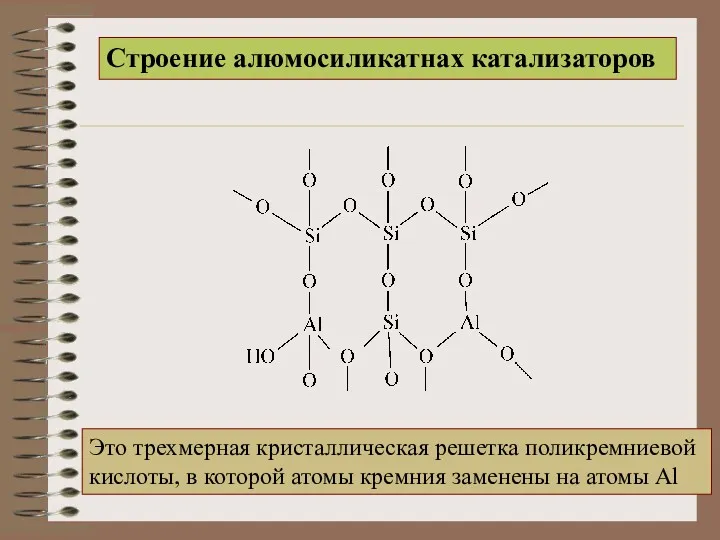
- 12. Строение алюмосиликатнах катализаторов Это трехмерная кристаллическая решетка поликремниевой кислоты, в которой атомы кремния заменены на атомы
- 13. Промышленный синтез Алюмосиликатного катализатора (ААК) Взаимодействие водных растворов силиката натрия [Na2SiO3] и сульфата алюминия [Al2(SO4)3] Образовавшийся
- 14. nAl2O3 X mSiO2 Примечание: Al2O3 и SiO2 в отдельности не являются катализаторами К. Механические смеси Al2O3
- 15. Алюмосиликатные катализаторы содержат воду А) адсорбирована (снижает активность кат.) Удаляют прокаливанием при 500-600оС Б) связана химически
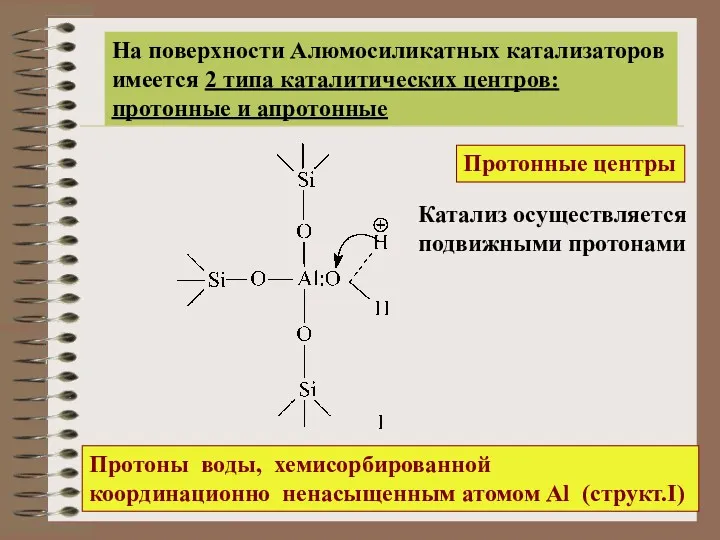
- 16. На поверхности Алюмосиликатных катализаторов имеется 2 типа каталитических центров: протонные и апротонные Протонные центры Катализ осуществляется
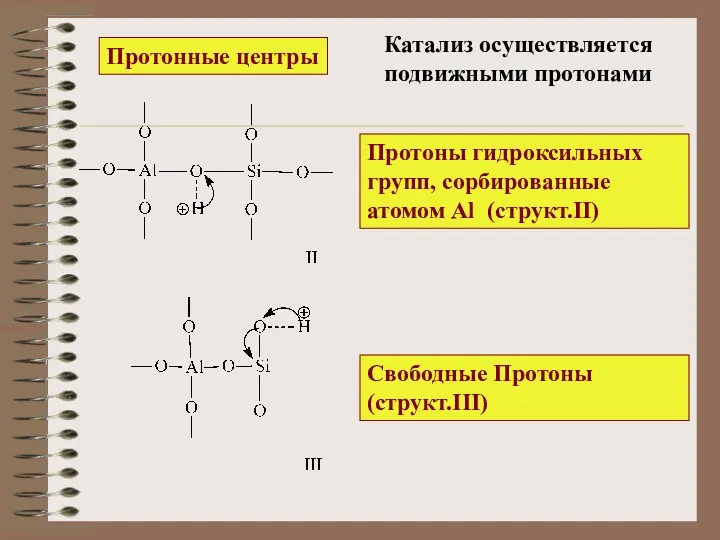
- 17. Протоны гидроксильных групп, сорбированные атомом Al (структ.II) Свободные Протоны (структ.III) Катализ осуществляется подвижными протонами Протонные центры
- 19. Скачать презентацию












 Металлы. Общая характеристика
Металлы. Общая характеристика Повышение эффективности производства изопропилбензола за счёт нового катализатора, производительность по кумолу 100500 т/год
Повышение эффективности производства изопропилбензола за счёт нового катализатора, производительность по кумолу 100500 т/год Химический состав водоотталкивающих средств
Химический состав водоотталкивающих средств Спектральные методы: инфракрасная спектроскопия. Люминесцентный анализ
Спектральные методы: инфракрасная спектроскопия. Люминесцентный анализ Атмосфера. Химия стратосферы
Атмосфера. Химия стратосферы Будова та властивості твердих тіл. Анізотропія кристалів. Рідкі кристали
Будова та властивості твердих тіл. Анізотропія кристалів. Рідкі кристали Азотсодержащие соединения
Азотсодержащие соединения Общая теория протолитических равновесий и процессов. Буферные системы
Общая теория протолитических равновесий и процессов. Буферные системы Водород. Химические свойства
Водород. Химические свойства Знакомство с образцами химических средств санитарии и гигиены
Знакомство с образцами химических средств санитарии и гигиены Эксплуатационные материалы
Эксплуатационные материалы Поширення та колообіг оксигену в природі
Поширення та колообіг оксигену в природі Катионы IV аналитической группы
Катионы IV аналитической группы Основания. Определите степени окисления элементов
Основания. Определите степени окисления элементов Исследование снега
Исследование снега Кислород. Распространение кислорода в природе (8 класс)
Кислород. Распространение кислорода в природе (8 класс) Каучук. Получение натурального каучука
Каучук. Получение натурального каучука Nucleic acids
Nucleic acids Історія відкриття періодичної системи хімічних елементів
Історія відкриття періодичної системи хімічних елементів Кремний, его физические и химические свойства
Кремний, его физические и химические свойства Поверхностно-активные вещества (ПАВ)
Поверхностно-активные вещества (ПАВ) Химия в повседневной жизни человека
Химия в повседневной жизни человека Полимеры. Мономер
Полимеры. Мономер Вычисление массовой доли растворенного вещества. 8 класс
Вычисление массовой доли растворенного вещества. 8 класс Распространенность химических элементов на земле и в космосе
Распространенность химических элементов на земле и в космосе Превращение веществ
Превращение веществ Металл серебро
Металл серебро Бутадиеновые каучуки
Бутадиеновые каучуки