Слайд 2

Цели урока:
- рассмотреть положение кремния в периодической системе Д.И.Менделеева и строении
его атома;
- рассмотреть нахождение кремния в природе;
- обратить внимание на физические свойства кремния;
- рассмотреть химические свойства кремния и способы его получения.
Слайд 3
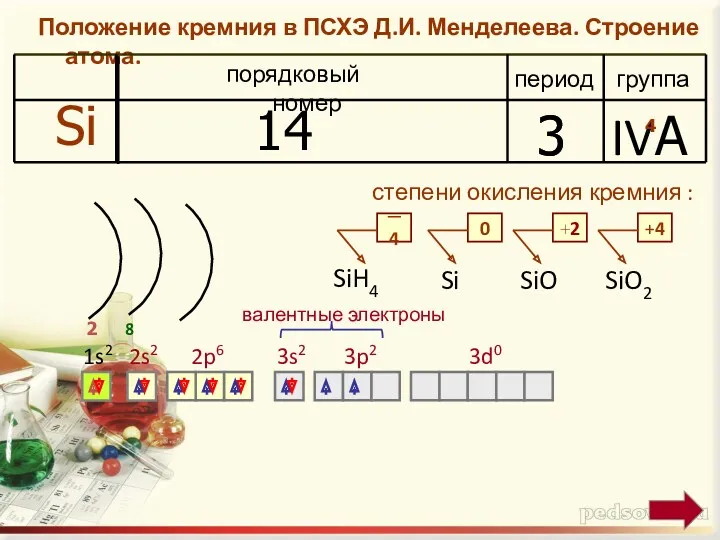
Положение кремния в ПСХЭ Д.И. Менделеева. Строение атома.
период
группа
порядковый номер
Si
14
3
IVA
3
2
4
степени окисления кремния
:
─ 4
0
+4
1s2
2s2
2p6
+2
валентные электроны
SiH4
Si
SiO
SiO2
8
3s2
3p2
3d0
Слайд 4

Слайд 5

Способы получения
Лабораторный способ получения:
Si+4O2 + 2Mg0 → 2Mg+2O + Si0
Промышленный способ
получения:
19000C
Si+4O2 + 2C0 ―――→ 2C+2O + Si0
Слайд 6

Физические свойства кремния
ρ = 2,33 г/см3
tплавления = 1415 0С
tкипения = 3500
0С
Слайд 7

Химические свойства
1) Кремний – восстановитель
Все реакции протекают при нагревании.
а) взаимодействие с
кислородом
Si0 + O20 = Si+4O2–2
Si0 -4e → Si+4 │4│1-восстановитель
O20 + 4e → 2O –2 │4│1-окислитель
б) взаимодействие с хлором
Si0 + 2Cl20 = Si+4Cl4-1
Si0 -4e → Si+4 │4 │1-восстановитель
Cl20 +2e → 2Cl- │2 │ 2-окислитель
Слайд 8

в) взаимодействие с серой
Si0 + 2S0 → Si+4S2-2
Si0 -4ē → Si+4
│2│1-восстановитель
S0 +2ē → S-2 │4│2-окислитель
г) взаимодействие с углеродом
20000С
Si0 + С0 ―――→ Si+4С-4 (карборунд)
Si0 -4e → Si + 4 │4│ 1-восстановитель
С0 +4e → С -4 │4│ 1-окислитель
Слайд 9

д) взаимодействие с водяным паром
Si0 + H2+1O (пар) → Si+4O2 +
H20↑
Si0 -4e → Si + 4│2│1-восстановитель
2H+ +2e → H20│4│2-окислитель
е) взаимодействие со щелочью
Si0 + 2NaOH + H+2O → Na2Si+4O3 + 2H20↑
Si0 -4e → Si+4 │4│1-восстановитель
2H+ +2e → H20 │2│2-окислитель
Слайд 10

2) Кремний – окислитель
Взаимодействие с металлами
Si0 + 2Mg0 = Mg2+2Si–4 (силицид
магния)
Si0 +4e → Si – 4 │2 │1-окислитель
Mg0 -2e → Mg +2│4 │2-восстановитель
Кремний напрямую не соединяется с водородом.
Силан получают косвенно, действуя на силициды металлов водой или кислотами
Mg2Si + 4H2O = 2Mg(OH)2↓ + SiH4↑









 Соли серной кислоты
Соли серной кислоты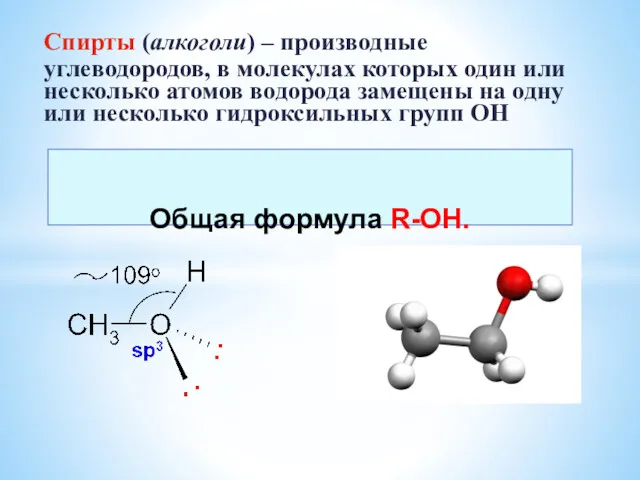 Спирты. Многоатомные спирты
Спирты. Многоатомные спирты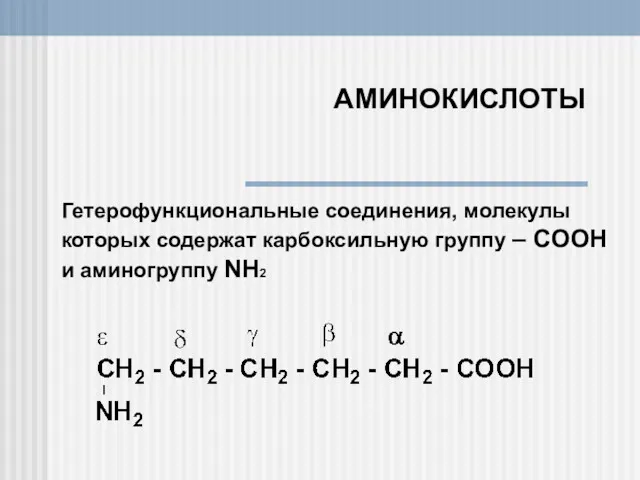 Аминокислоты. Гетерофункциональные соединения, молекулы
Аминокислоты. Гетерофункциональные соединения, молекулы Электродные системы
Электродные системы Химическая кинетика
Химическая кинетика Оценка химической обстановки при авариях на химически опасных объектах
Оценка химической обстановки при авариях на химически опасных объектах Вред Coca-Cola на организм человека
Вред Coca-Cola на организм человека Эквивалент. Закон эквивалентов
Эквивалент. Закон эквивалентов Удобрения. 9 класс
Удобрения. 9 класс Кислотно-основное титрование в неводных средах
Кислотно-основное титрование в неводных средах Растворы ВМС
Растворы ВМС Неорганические соединения галогенов
Неорганические соединения галогенов Комплекс заходів з ліквідації наслідків радіаційне небезпечної надзвичайної ситуації
Комплекс заходів з ліквідації наслідків радіаційне небезпечної надзвичайної ситуації Катализ. Факторы, влияющие на скорость реакции
Катализ. Факторы, влияющие на скорость реакции Окислительно - восстановительные реакции (ОВР) (часть 1)
Окислительно - восстановительные реакции (ОВР) (часть 1) Общая геохимия. Атомная и молекулярная масса. Представление результатов аналитических исследований
Общая геохимия. Атомная и молекулярная масса. Представление результатов аналитических исследований Итоговая контрольная работа по химии
Итоговая контрольная работа по химии Аллотропные модификации углерода ( 8класс)
Аллотропные модификации углерода ( 8класс) Почвенный раствор. Химический состав почвенных растворов. Водный режим почв. Кислотность и щелочность почвенных растворов
Почвенный раствор. Химический состав почвенных растворов. Водный режим почв. Кислотность и щелочность почвенных растворов Чистые вещества и смеси
Чистые вещества и смеси Элементы химической термодинамики и биоэнергетики
Элементы химической термодинамики и биоэнергетики Физические свойства минералов
Физические свойства минералов Реакции ионного обмена
Реакции ионного обмена Органикалық қосылыстар құрылысының теориялық негіздері және олардың реакцияға қабілеттілігін анықтаушы факторлар
Органикалық қосылыстар құрылысының теориялық негіздері және олардың реакцияға қабілеттілігін анықтаушы факторлар Судың кермектілігі. Сілтілік металдар мен сілтілікжер металдардың табиғи қосылыстарының қазақстандағы кен орындары
Судың кермектілігі. Сілтілік металдар мен сілтілікжер металдардың табиғи қосылыстарының қазақстандағы кен орындары Состояние радионуклидов в различных фазах и методы его изучения
Состояние радионуклидов в различных фазах и методы его изучения Строение и химические свойства кислот
Строение и химические свойства кислот Новые требования к оценке опасности, паспортам безопасности и маркировке химической продукции
Новые требования к оценке опасности, паспортам безопасности и маркировке химической продукции