Содержание
- 2. Катализ – это явление изменения скорости реакции под влиянием веществ, называемых катализаторами.
- 3. Катализаторы – это вещества, изменяющие скорость химической реакции, но не изменяющиеся в ходе процесса ни качественно,
- 4. Небольшие количества катализаторов способны существенно изменить скорость взаимодействия большого количества реагирующих веществ.
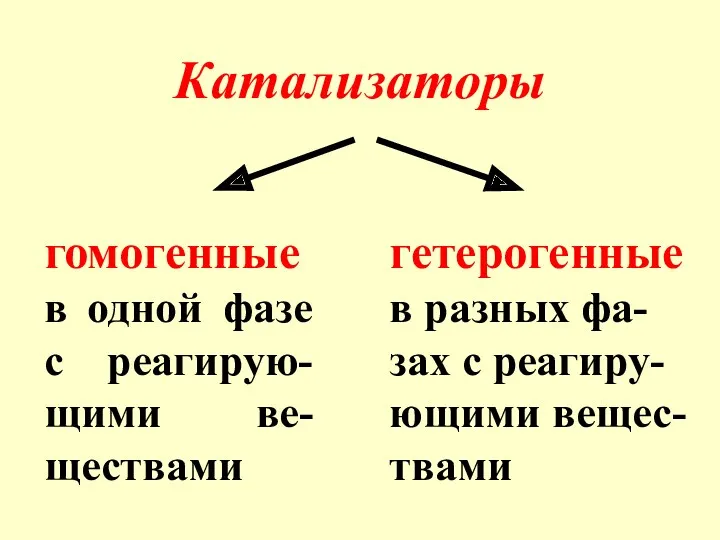
- 5. Катализаторы гомогенные в одной фазе с реагирую-щими ве-ществами гетерогенные в разных фа-зах с реагиру-ющими вещес-твами
- 6. Пример гетерогенного катализа
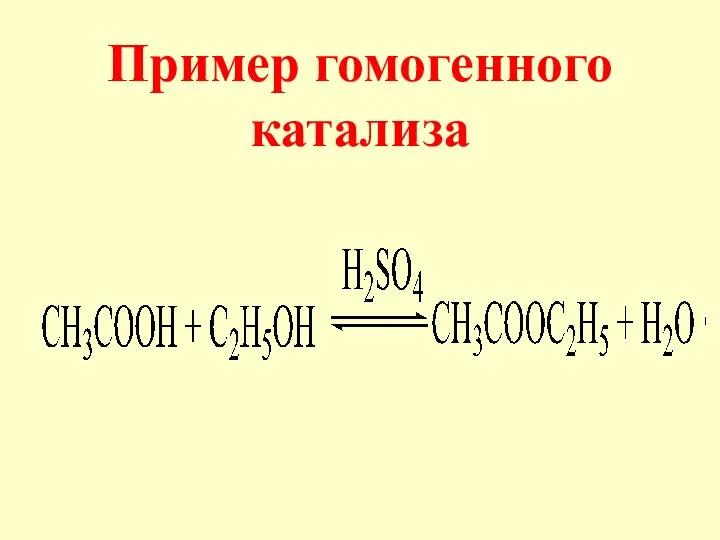
- 7. Пример гомогенного катализа
- 8. Катализаторы положительные увеличивают скорость реакции отрицательные уменьшают скорость реакции
- 9. Ингибиторы – вещества, уменьша-ющие скорость реак-ции, но расходую-щиеся при этом сами.
- 10. С точки зрения теории активного комплекса механизм действия катализаторов в том, что они изменяют высоту энергетического
- 11. Без катализатора: А + В ↔ А...В → АВ В присутствии катали-затора: А + В +
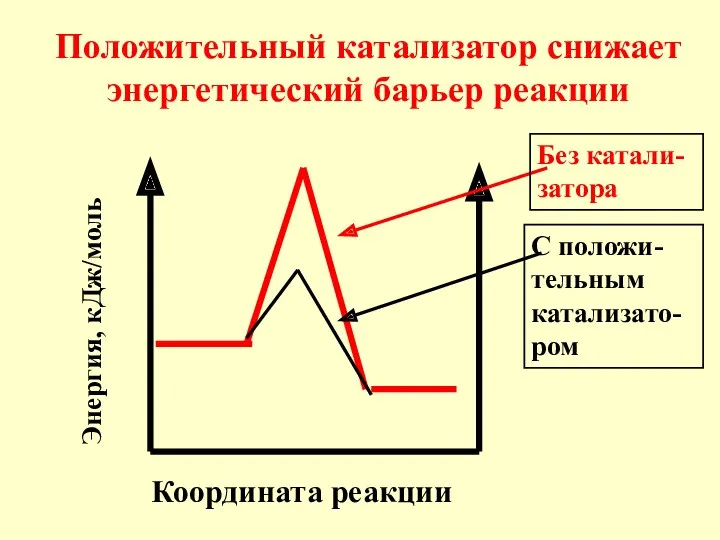
- 12. Координата реакции Положительный катализатор снижает энергетический барьер реакции Энергия, кДж/моль Без катали-затора С положи-тельным катализато-ром
- 13. Под воздействием поло-жительного катализатора в реакционной смеси возрастает доля актив-ных молекул при данной температуре. Скорость реакции
- 14. Под воздействием отри-цательного катализатора в реакционной смеси снижается доля актив-ных молекул при данной температуре. Скорость реакции
- 15. Разрушение озонового слоя Земли – пример гомогенного катализа, протекающего в атмосфере под воздействием фреонов.
- 16. Фреоны – это фторо-хлороуглеводороды (СF2Cl2), применяемые как хладаген-ты. При обычных условиях они отличаются высокой устойчивостью к
- 17. В атмосфере происходит разложение фреонов под воздействием ультрафиолето-вого излучения солнца: CF2Cl2 → CF2Cl• + Cl• Cl•
- 18. Без катализатора процесс протекает по схеме: O3 + O → 2 O2 Eак = 17,1 кДж/моль
- 19. В присутствии катализатора: O3 + Cl → ClO + O2 Eак= 2,1 кДж/моль ClO + O
- 20. Вещества, усиливаю-щие действие катализа-торов, называются про-моторами, а ослабляю-щие - каталитическими ядами.
- 21. Практически все биохимические реакции являются ферментативными. Ферменты (биокатализаторы) – это вещества белковой природы, активированные катионами металлов.
- 22. Известно около 2000 различных ферментов, ~150 из них выделены, причем некоторые используются в качестве лекарственных препа-ратов.
- 23. Трипсин и химотрипсин – лечение бронхитов и пнев-монии; пепсин – лечение гастрита; плазмин – лечение инфаркта;
- 25. Скачать презентацию


















 Омега 3
Омега 3 Химико-токсикологическое исследование кокаина
Химико-токсикологическое исследование кокаина Будова атома: ядро й електронна оболонка. Склад атомних ядер. Протонне та нуклонне число
Будова атома: ядро й електронна оболонка. Склад атомних ядер. Протонне та нуклонне число Бензол. Бензол гомологтары. Фенолдар және ароматты аминдер
Бензол. Бензол гомологтары. Фенолдар және ароматты аминдер Вода
Вода Сравнительный анализ установки изомеризации между Павлодарским НПЗ и Московским НПЗ
Сравнительный анализ установки изомеризации между Павлодарским НПЗ и Московским НПЗ Классификация химических реакций
Классификация химических реакций Минералы и их свойства
Минералы и их свойства Ароматические углеводороды
Ароматические углеводороды Минералы и их строение
Минералы и их строение Materials. Metals non-metals
Materials. Metals non-metals Водородные соединения неметаллов
Водородные соединения неметаллов Полимеры. Пластмассы. Волокна
Полимеры. Пластмассы. Волокна Спирти. Феноли. Етери
Спирти. Феноли. Етери Особливості горіння дисперсних систем
Особливості горіння дисперсних систем Чисті речовини та суміші. (7 клас)
Чисті речовини та суміші. (7 клас) Мыло. Синтетические моющие средства
Мыло. Синтетические моющие средства Спирты, фенолы, тиолы
Спирты, фенолы, тиолы Арены. Бензол
Арены. Бензол Вклад М.В. Ломоносова в развитие науки химия
Вклад М.В. Ломоносова в развитие науки химия Определение разных форм угольной кислоты
Определение разных форм угольной кислоты Металлы и Неметаллы
Металлы и Неметаллы Цинк и его соединения
Цинк и его соединения Щелочные металлы
Щелочные металлы Скорость химических реакций. Катализ. Химическое равновесие
Скорость химических реакций. Катализ. Химическое равновесие Химия p-элементов
Химия p-элементов Физическая химия дисперсных систем. Лекция 7
Физическая химия дисперсных систем. Лекция 7 Органіка. Органічні речовини
Органіка. Органічні речовини