Содержание
- 2. В історії розвитку науки відомо багато великих відкриттів. Але деякі з них можна співставити з тим,
- 3. Періодична система-шахово-клітинна таблиця, в якій елемент займає своє місце. Структура Періоди Короткі (1-3) Довгі (4-7) Групи
- 4. Загальні закономірності заповнення рівнів елементами: Починається заповнення з зовнішнього рівня атома; Кожен період закінчується 6-тьма елементами,
- 5. Металами називаються елементи, атоми яких можуть тільки віддавати електрони - s-елементи (крім Н) p, d, f.
- 6. Радіуси атомів (ефективний радіус атома) – це границя силового поля, ближче якої даний атом не підпускає
- 7. Кількісна характеристика хімічних властивостей елементів Енергія іонізації, або іонізаційний потенціал; Енергія, яка виділяється при приєднанні електрону
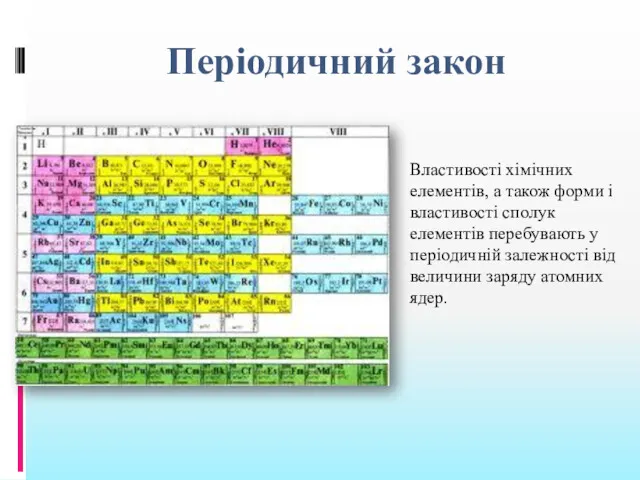
- 8. Періодичний закон Властивості хімічних елементів, а також форми і властивості сполук елементів перебувають у періодичній залежності
- 9. В даний час поширеними є три форми таблиці Менделєєва: «коротка», «довга» і «наддовга».
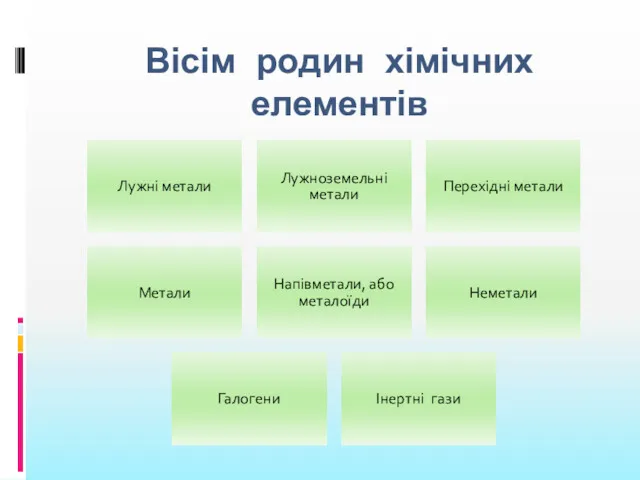
- 10. Вісім родин хімічних елементів Лужні метали Лужноземельні метали Перехідні метали Метали Напівметали, або металоїди Неметали Галогени
- 11. Принципи заповнення Таблиці періодичної системи Принцип Паулі Правило Клечковского Принцип найменшої енергії Правило Хундай
- 12. Електрон, як енергетична система, має власну кваркову структуру, тому при приєднанні до атома одночасно займає вісім
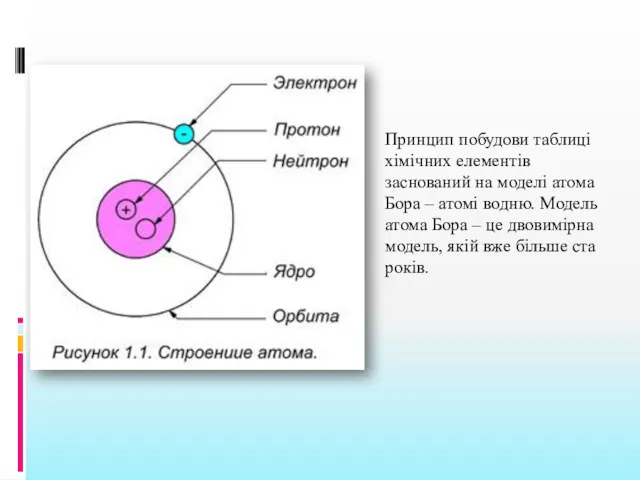
- 13. Принцип побудови таблиці хімічних елементів заснований на моделі атома Бора – атомі водню. Модель атома Бора
- 14. Найменші матеріальні частки Нейтрон Електрон Фотон
- 15. Електрон – енергетична частка, утворена з кварка простору під час первинного нуклеосинтезу. Електричний заряд електрона є
- 16. Нейтрон – енергетична частка реального навколишнього Всесвіту, утворена з 8 кварків простору вимірювання , що мають
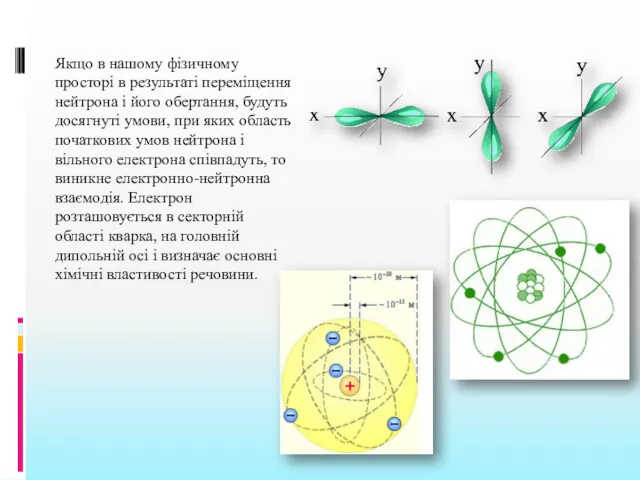
- 17. Якщо в нашому фізичному просторі в результаті переміщення нейтрона і його обертання, будуть досягнуті умови, при
- 18. Конструкція кожного наступного за номером елементу включає в себе конструкцію попереднього елементу. Останнім елементом є елемент
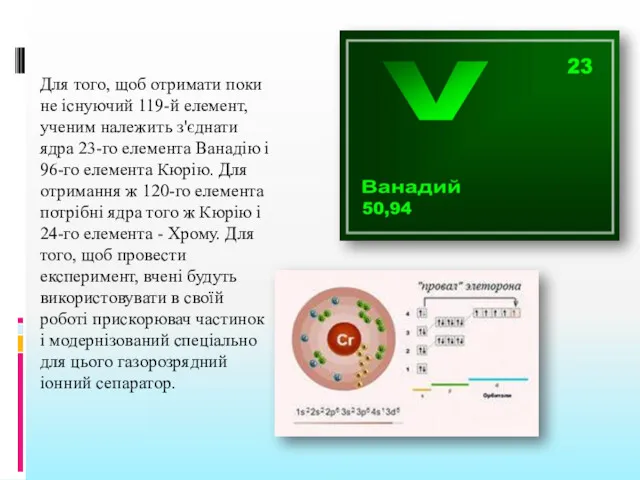
- 19. Для того, щоб отримати поки не існуючий 119-й елемент, ученим належить з'єднати ядра 23-го елемента Ванадію
- 21. Скачать презентацию













 Процессы природного минералообразования. Формы природных выделений минералов
Процессы природного минералообразования. Формы природных выделений минералов Химический элемент титан
Химический элемент титан Химическая термодинамика
Химическая термодинамика Обзор электродных процессов
Обзор электродных процессов Азотсодержащие органические соединения
Азотсодержащие органические соединения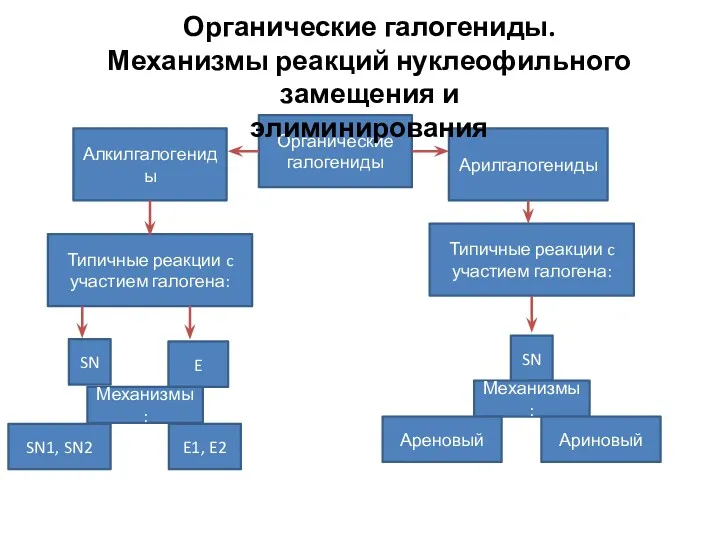
 Никель – тяжелый металл
Никель – тяжелый металл Хром. Строение атома
Хром. Строение атома ЕГЭ по химии. Решение задач 27, 28, 29
ЕГЭ по химии. Решение задач 27, 28, 29 Технология производства бутилкаучука
Технология производства бутилкаучука Катализ кислотами и основаниями. Лекция 3
Катализ кислотами и основаниями. Лекция 3 Силикатное производство
Силикатное производство серная кислота и ее соли 9 класс
серная кислота и ее соли 9 класс Химическая кинетика
Химическая кинетика Арены - ароматические соединения
Арены - ароматические соединения Электролиз растворов. Применение вытеснительного ряда металлов для прогнозирования продуктов электролиза
Электролиз растворов. Применение вытеснительного ряда металлов для прогнозирования продуктов электролиза Склад та властивості основних класів неорганічних сполук
Склад та властивості основних класів неорганічних сполук Воздух, которым мы дышим
Воздух, которым мы дышим Жуғыш заттардың адам өміріндегі маңызы
Жуғыш заттардың адам өміріндегі маңызы Строение и свойства атомов в свете квантовомеханической теории. Периодический закон – основа основ химии
Строение и свойства атомов в свете квантовомеханической теории. Периодический закон – основа основ химии Измерение и оценка химического фактора. Лекция 9
Измерение и оценка химического фактора. Лекция 9 Коррозия металлов
Коррозия металлов Неметаллы. Общая характеристика неметаллов
Неметаллы. Общая характеристика неметаллов Заходи з ліквідації наслідків хімічної небезпечної надзвичайної ситуації. Особливості ведення хімічної розвідки та контролю
Заходи з ліквідації наслідків хімічної небезпечної надзвичайної ситуації. Особливості ведення хімічної розвідки та контролю Периодическая система Д. И. Менделеева
Периодическая система Д. И. Менделеева Кислород. Открытие кислорода
Кислород. Открытие кислорода Lipid metabolism
Lipid metabolism Алканы: физические и химические свойства, получение
Алканы: физические и химические свойства, получение