Содержание
- 2. 6я группа главная подгруппа содержит элементы: О S Se Te На долю кислорода приходится 46% массы
- 3. О – второй по электроотрицательности элемент. С большинством металлов О реагирует при комнатной температуре, образую основные
- 4. Более сильным окислителем, чем кислород является озон. Его получают пропусканием электрического заряда через кислород (выход реакции
- 5. В промышленности получают: Фракционной перегонкой жидкого воздуха (разность температур конденсации) Электролизом воды В лаборатории: 2KMnO4 ->
- 6. Сера элемент встречающийся в самородном виде. Имеет три аллотропных модификации: ромбическая, моноклинная и пластическая. Сера
- 7. Часто образуется в фумаролах рядом с вулканами. Сера
- 8. При комнатной температуре сера реагирует со фтором, хлором и концентрированными кислотами-окислителями (HNO3, H2SO4): S + 3F2
- 9. Сероводород – бесцветный и очень токсичный газ с запахом тухлых яиц. Получение в лаборатории: FeS +
- 10. SO2 + H2O H2SO3 Сернистый газ можно получить при взаимодействии: Me + 2H2SO4 (конц) -> CuSO4
- 12. Скачать презентацию









 Ароматические амины
Ароматические амины Природные и химические волокна
Природные и химические волокна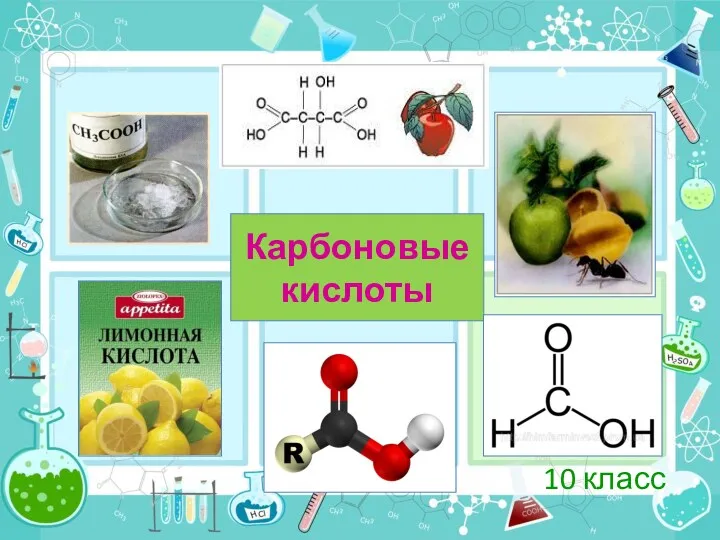 Карбоновые кислоты. 10 класс
Карбоновые кислоты. 10 класс Химические свойства алкенов
Химические свойства алкенов Диэлектрофорез: движение клеток или частиц в неоднородном переменном электрическом поле
Диэлектрофорез: движение клеток или частиц в неоднородном переменном электрическом поле Растворы электролитов. Ионизация воды и шкала рН
Растворы электролитов. Ионизация воды и шкала рН Химический элемент и вещество
Химический элемент и вещество Летучие органические соединения (ЛОС)
Летучие органические соединения (ЛОС) Вуглецьвмісна сировина для одержання вуглецевих сорбентів
Вуглецьвмісна сировина для одержання вуглецевих сорбентів Бытовая химия
Бытовая химия Кристаллические решетки. (8 класс)
Кристаллические решетки. (8 класс) Сера и её соединения
Сера и её соединения Обмен жиров
Обмен жиров Изомерия. (11 класс)
Изомерия. (11 класс) Такой разный песок
Такой разный песок Роль полимеров в нашей жизни
Роль полимеров в нашей жизни Реакции нейтрализации
Реакции нейтрализации Скорость химических реакций. Факторы, влияющие на скорость химической реакции
Скорость химических реакций. Факторы, влияющие на скорость химической реакции Кинетика и равновесие химических реакций
Кинетика и равновесие химических реакций Аминокислоты и белки
Аминокислоты и белки Синтетические моющие средства
Синтетические моющие средства Количество вещества. Единица измерения вещества моль
Количество вещества. Единица измерения вещества моль Камни и Лев
Камни и Лев Химия көшбасшысы
Химия көшбасшысы Қышқылдық-негіздік тепе-теңдік. Қышқылдар мен негіздердің протологиялық теориясы
Қышқылдық-негіздік тепе-теңдік. Қышқылдар мен негіздердің протологиялық теориясы Металдардың физикалық қасиеттерін ажырата білу
Металдардың физикалық қасиеттерін ажырата білу XXI ғасыр көшбасшысы
XXI ғасыр көшбасшысы Неметаллические материалы, используемые в машино- и приборостроении
Неметаллические материалы, используемые в машино- и приборостроении