Содержание
- 2. 4.1 Сильные и слабые электролиты 4.2. Кислотность водных растворов и биологических жидкостей. 4.3 Буферные растворы. План
- 3. 4.1. Электролиты – это вещества, диссоциирующие в растворах на ионы. К ним относятся соединения с ионным
- 4. К слабым электролитам относятся соединения, частично (обратимо) диссоциирующие в водных растворах: а) почти все органические и
- 5. Равновесие между молекулами и ионами в растворе описываются с помощью констант равновесия, называемых константами диссоциации (Кдис)
- 6. Константы диссоциации кислот называются константами кислотности Ka, а константы диссоциации оснований – константами основности Kb
- 7. Слабые электролиты подчиняются закону разбавления Оствальда: при разбавление раствора водой степень электролитической диссоциации электролита увеличивается ,
- 8. Сильные электролиты - это соединения, полностью диссоциирующие в водных растворах (α = 100%)
- 9. Из-за высокой концентрации ионов в растворе сильного электролита создается электромагнитное поле, интенсивность которого определяется величиной ионной
- 10. В растворе сильного электролита вокруг каждый ион окружен ионной атмосферой, состоящая из ионов противоположного знака: +
- 11. Во внешнем электрическом поле ион и его атмосфера приобретают разнонаправленное движение, вследствие чего происходит электрофоретическое торможение
- 12. Концентрация ионов, рассчитанная по электропроводности, меньше, чем их истинная концентрация. «Кажущаяся» концентрация называется активностью (а) а
- 13. а) удерживают воду в виде гидратов; б) создают осмотическое давление биологических жидкостей. Существование перепадов осмотического давления
- 14. в) влияют на растворимость биологически активных соединений. В разбавленных растворах наблюдается солевой эффект – увеличение растворимости
- 15. 4.2 Кислотность является важной характеристикой как водных растворов, так и биологических жидкостей. Она определяется соотношением концентраций
- 16. Для характеристики кислотности используется водородный показатель (рН) : рН = - lg[H+], а для сильных кислот
- 17. Реже для характеристики реакции среды используется гидроксильный показатель (рОН): рОН = - lg[OH-], а для щелочей
- 18. Для одного раствора рН + рОН = 14
- 19. Константа равновесия, описывающая диссоциацию воды (ионное произведение воды), КW = [H+]×[OH-] = 10-14, В нейтральном растворе
- 20. В кислой среде: [H+] > [OH-] рН 7 В щелочной среде: [H+] pH > 7, pOH
- 21. Шкала рН [Н+],M pH 1 10-5 10-7 10-9 10-14 0 5 7 9 14 Сильнокислая среда
- 22. Кислотность биологических жидкостей человека
- 23. Для биологических жидкостей характерен кислотно-основной гомеостаз (постоянство значений рН), обусловленный действием биологических буферных систем.
- 24. Нарушение кислотно-основного равновесия приводит: к ацидозу – увеличение кислотности внутренней среды организма, к алкалозу –увеличение ее
- 25. Ацидоз Респираторный Метаболический Гиповентиляция легких CO2 + H2O ⇄ H2CO3 Сахарный диабет и некоторые другие заболевания
- 26. Здоровая диета должна содержать 60% основных и 40% кислотных компонентов пищи.
- 27. Опасность изменения рН связана 1) со снижением активности ферментов и гормонов, активных в узком диапазоне рН;
- 28. 3) с изменением скорости биохимических реакций, катализируемых катионами Н+. При изменении рН крови на 0,3 единицы
- 29. 4.3 Буферными называют растворы, рН которых не изменяется при добавлении небольших количеств кислот или щелочей, а
- 30. Протолитическая теория кислот и оснований Бренстеда-Лоури (1923) объясняет механизм буферного действия. Согласно этой теории, кислота –
- 31. Различают: кислоты–молекулы (CH3COOH), кислоты-катионы (NH4+), кислоты–анионы (H2PO4-)
- 32. Каждая кислота сопряжена со своим основанием. Основание – это акцептор протонов.
- 33. Cопряженные пары кислот и оснований СH3COOH ⇄ CH3COO- + H+ Кислота Сопряженное основание
- 34. NH4+ ⇄ NH3 + H+ Кислота Сопряженное основание
- 35. Поскольку буферный раствор содержит кислоту и сопряженное с ней основание, он нейтрализует как добавленную кислоту, так
- 36. Классификация буферных растворов Ацетатный буфер: СН3СООН/СН3СООNa Механизм буферного действия НCl + CH3COONa ⇄ CH3COOH + NaCl
- 37. 2) Слабое основание/его соль Аммиачный буфер: NН3/NН4Сl Механизм буферного действия НCl + NH3 ⇄ NH4Cl Нейтрализация
- 38. 3) Две кислые соли Гидрофосфатный буфер : NаН2PO4/Nа2НPO4 Механизм буферного действия НCl + Na2HPO4 ⇄ NaH2PO4+
- 39. 4) кислая соль/средняя соль Карбонатный буфер: NаНСO3/Nа2СO3 Механизм буферного действия НCl + Na2СO3 ⇄ NaHСO3+ NaCl
- 40. Уравнение Гендерсона- Гассельбаха позволяет рассчитать рН буферного раствора: рН =рКа - lg [кислота] [сопряженное основание] _
- 41. Буферная емкость раствора (В, ммоль/л) - это количества сильных кислот или щелочей, при прибавлении которых к
- 42. Буферная емкость зависит: от концентрации: чем выше концентрация раствора, тем больше его буферная емкость; 2) от
- 43. Характеристиками биологических буферных систем являются: Bк – буферная емкость по кислоте, Bщ – буферная емкость по
- 44. Из буферных систем организма наибольшей емкостью характеризуются буферные системы крови. Они распределены между эритроцитами и плазмой.
- 45. БУФЕРНЫЕ СИСТЕМЫ КРОВИ Плазма Эритроциты гидрокарбонатный гидрофосфатный белковый (альбумины, глобулины ) гемоглобин - оксигемоглобин
- 46. Гидрокарбонатный (водокарбонатный) буфер: H2CO3/HCO3- ферм. СО2 + Н2О ⇄ Н2СО3 ⇄ НСО3-+ Н+ Механизм буферного действия:
- 47. В крови [HCO3] 40 [H2CO3] 1 избыток гидрокарбоната создает щелочной резерв крови Вк = 40 ммоль/л;
- 48. Анализируя содержание НСО3- в крови можно диагностировать наличие дыхательных и метаболических нарушений.
- 49. Буферная система гемоглобин-оксигемоглобин обеспечивает 75% буферной емкости крови.
- 50. Буферные системы организма обеспечивают кислотно-основной гомеостаз человека.
- 52. Скачать презентацию
 Периодический закон и периодическая система химических элементов Д.И. Менделеева
Периодический закон и периодическая система химических элементов Д.И. Менделеева Химия вокруг нас
Химия вокруг нас Теория химического строения органических соединений
Теория химического строения органических соединений Фазовые диаграммы и статистическая термодинамика бинарных m-h систем
Фазовые диаграммы и статистическая термодинамика бинарных m-h систем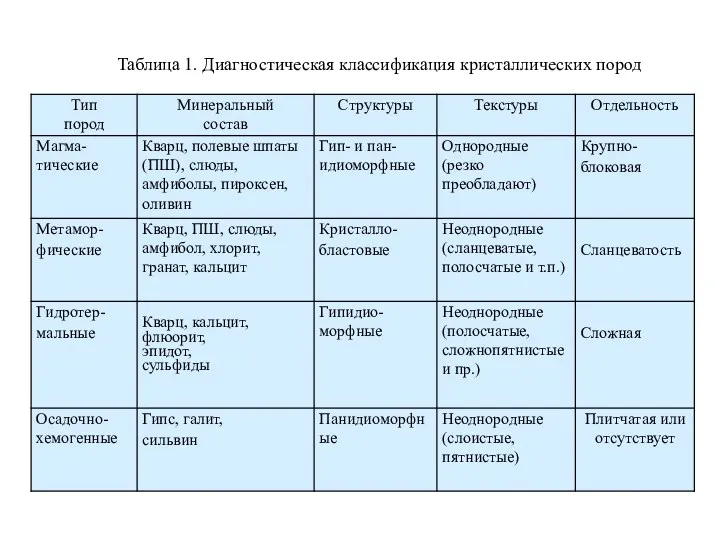 Диагностика метаморфических и гидротермальных горных пород
Диагностика метаморфических и гидротермальных горных пород La notion de catabolisme et d’anabolisme. La bioenergetique. La chaine mitochondriale de transfert d’electrons
La notion de catabolisme et d’anabolisme. La bioenergetique. La chaine mitochondriale de transfert d’electrons Комплексные (или координационные) соединения
Комплексные (или координационные) соединения Магний. Электронное строение атома Mg
Магний. Электронное строение атома Mg Периодический закон и периодическая система химических элементов Д.И. Менделеева
Периодический закон и периодическая система химических элементов Д.И. Менделеева Азотсодержащие органические соединения
Азотсодержащие органические соединения Оптические свойства и методы исследования дисперсных систем. Лекция 16
Оптические свойства и методы исследования дисперсных систем. Лекция 16 Електролітична дисоціація. Електроліти та неелектроліти. Урок хімії в 9 класі
Електролітична дисоціація. Електроліти та неелектроліти. Урок хімії в 9 класі Kарбонові кислоти. Гетерофункціональні похідні карбонових кислот
Kарбонові кислоти. Гетерофункціональні похідні карбонових кислот Электрохимический ряд напряжения металлов
Электрохимический ряд напряжения металлов Сағыз пайдалы ма, әлде зиян ба?
Сағыз пайдалы ма, әлде зиян ба? Химия в быту
Химия в быту Альдегиды и кетоны
Альдегиды и кетоны Chemical Equilibrium. Topic 3.3
Chemical Equilibrium. Topic 3.3 Соли. Классификация и свойства солей
Соли. Классификация и свойства солей Типы химических реакций
Типы химических реакций Ультраосновные породы (гипербазиты)
Ультраосновные породы (гипербазиты) Діагностика за показами газоаналізатора. Типи газоаналізаторів
Діагностика за показами газоаналізатора. Типи газоаналізаторів Аммиак. Физические и химические свойства. Получение, применение
Аммиак. Физические и химические свойства. Получение, применение Энергетический обмен
Энергетический обмен Композиты и композиционные материалы
Композиты и композиционные материалы Вода. Анализ и синтез. Состав оснований
Вода. Анализ и синтез. Состав оснований Электролитическая диссоциация
Электролитическая диссоциация Типы химических реакций
Типы химических реакций