Содержание
- 2. Превращения веществ
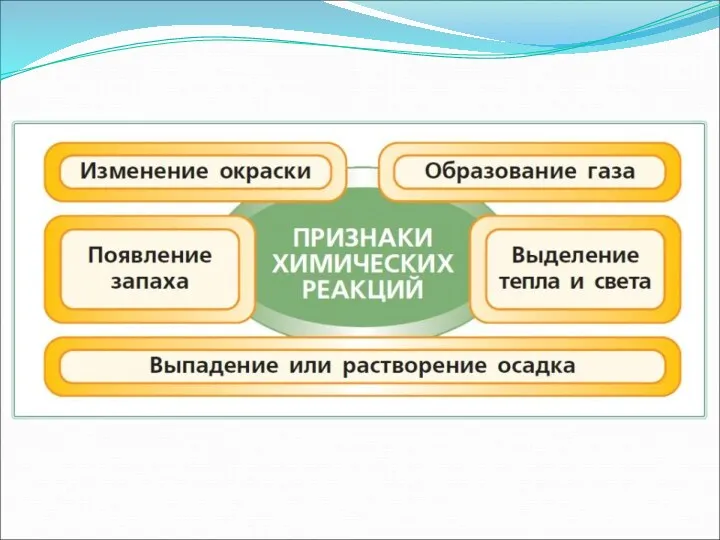
- 3. Химическая реакция – это …
- 5. Закон сохранения массы вещества Масса веществ, вступивших в реакцию, всегда равна массе веществ, получившихся в ходе
- 6. 10.12.11
- 7. 1) ? А + ?В = А2В3 2) ? А +….. =А2С 3) А + В
- 8. Типы реакций химические реакции соединения A + B = AB Из нескольких простых или сложных веществ
- 9. С О Е Д И Н Е Н И Я а) 2Р + 3Сl2 = 2РСl3;
- 10. Типы реакций химические реакции разложения AB = A + B Из сложного вещества образуется несколько простых
- 11. а) 2HgO = 2Hg + O2 б) 2Ag2O = 4Ag + O2 в) Fe(OH)2 = FeO
- 12. Типы реакций химические реакции замещения A + BC =AC + B Атом простого вещества замещает один
- 13. а) H2 + CuO = Cu + H2O б) C + FeO = Fe + CO
- 14. Типы реакций химические реакции ионного обмена AB+CD = AD+CB Сложные вещества обмениваются своими составными частями
- 15. а) MgO + 2HF = MgF2 + H2O б) NaOH + HNO3 = NaNO3 + H2O
- 16. ЗАКРЕПЛЯЕМ
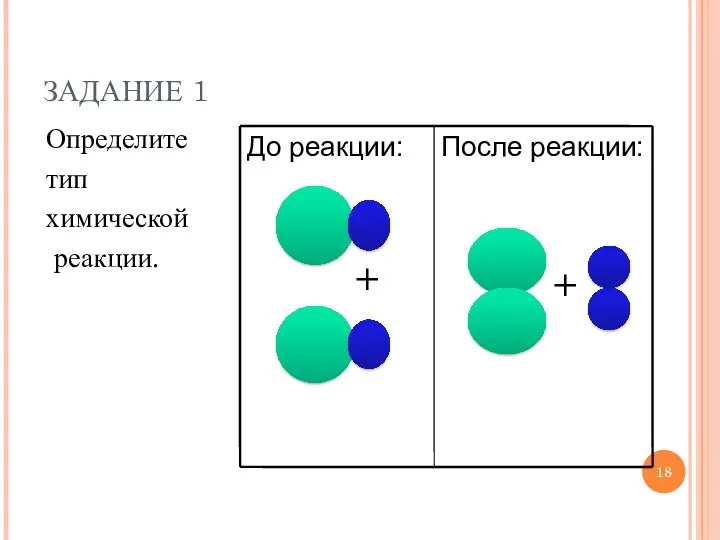
- 18. Определите тип химической реакции. + + ЗАДАНИЕ 1
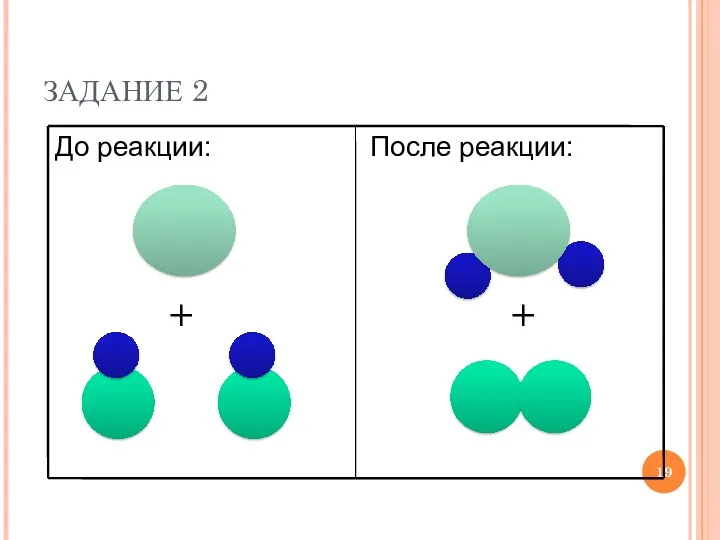
- 19. + + ЗАДАНИЕ 2
- 20. ЗАДАНИЕ 3 10.12.11 1. 2NaCl = 2Na + Cl2 2. CaO + CO2 = CaCO3 3.
- 21. ЗАДАНИЕ 4 10.12.11 1.2CuO + C = 2Cu + O2 2. 2NO + O2 = 2NO2
- 22. Определите тип приведенных ниже реакций: H2 + Br2 = 2HBr . . . . . .
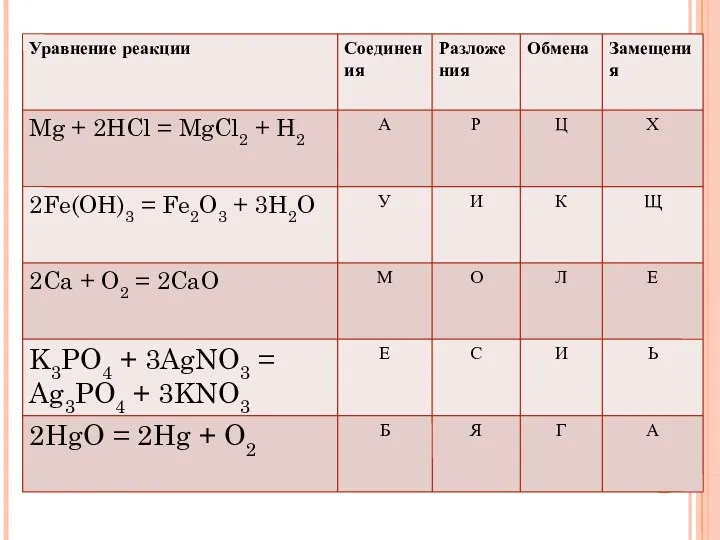
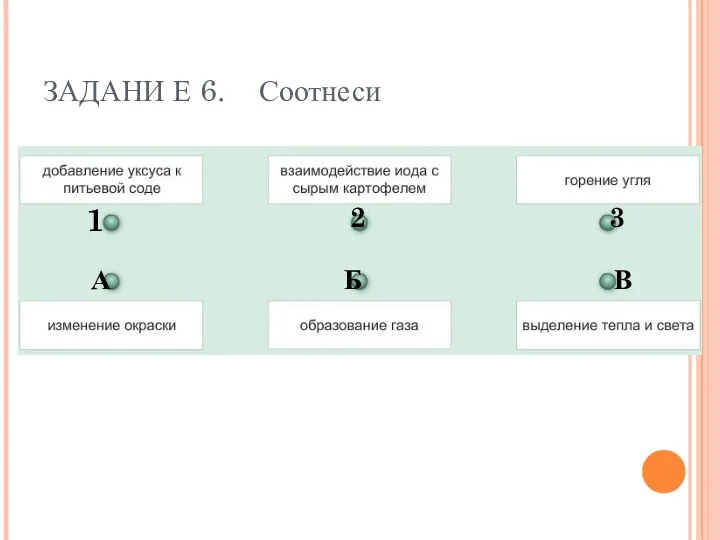
- 23. 1 2 3 А Б В ЗАДАНИ Е 6. Соотнеси
- 24. «Ты знаешь газ легчайший – водород. В соединенье с кислородом – это Июньский дождь от всех
- 25. Расставьте коэффициенты в уравнениях химических реакций. Укажите тип каждой реакции. 1. Cu + O2 ⭢ CuO
- 27. Скачать презентацию



















 Алкадиены. Циклоалканы. Лекция № 5
Алкадиены. Циклоалканы. Лекция № 5 Общая характеристика элементов I группы главной подгруппы Периодической системы химических элементов Д.И. Менделеева
Общая характеристика элементов I группы главной подгруппы Периодической системы химических элементов Д.И. Менделеева Электрохимический ряд напряжений металлов. Свойства металлов
Электрохимический ряд напряжений металлов. Свойства металлов Состав и свойства чая
Состав и свойства чая Сплавы и их свойства. Легирующие добавки
Сплавы и их свойства. Легирующие добавки Принципы наноармирования волокнистых композитов
Принципы наноармирования волокнистых композитов Важнейшие органические вещества пищевых продуктов. Жиры.(Липиды)
Важнейшие органические вещества пищевых продуктов. Жиры.(Липиды) General characteristics of halogens. Halogen compounds
General characteristics of halogens. Halogen compounds Золь-гель технология. Прорыв XXI века
Золь-гель технология. Прорыв XXI века Промышленные типы месторождений железа
Промышленные типы месторождений железа Напій кока-кола. Активні інгредієнти кока-коли
Напій кока-кола. Активні інгредієнти кока-коли Параметры токсичности продуктов горения материала. (Задача 3)
Параметры токсичности продуктов горения материала. (Задача 3) Периодический закон и периодическая система химических элементов Д.И. Менделеева
Периодический закон и периодическая система химических элементов Д.И. Менделеева Дисперсные системы
Дисперсные системы Гетерогенді химиялық реакциялар
Гетерогенді химиялық реакциялар Поверхностные явления
Поверхностные явления Химическая связь. 8 класс
Химическая связь. 8 класс Углеводы, липиды
Углеводы, липиды Состав газированной воды
Состав газированной воды Химический элемент медь
Химический элемент медь Неметаллы. 11 класс
Неметаллы. 11 класс Промышленные катализаторы
Промышленные катализаторы Непредельные углеводороды
Непредельные углеводороды Сероводород и сульфиды
Сероводород и сульфиды СПЛАВЫ. КОРРОЗИЯ МЕТАЛЛОВ
СПЛАВЫ. КОРРОЗИЯ МЕТАЛЛОВ Сплавы металлов. 11 класс
Сплавы металлов. 11 класс Растворы. Роль растворов в природе
Растворы. Роль растворов в природе Нефть. Свойства нефти
Нефть. Свойства нефти