Слайд 2

ПОЛОЖЕНИЕ В ПЕРИОДИЧЕСКОЙ СИСТЕМЕ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ МЕНДЕЛЕЕВА
Сурьма (химический символ — Sb; лат. Stibium) — химический элемент 15-й группы (по
устаревшей классификации — главной подгруппы пятой группы) пятого периода периодической системы Менделеева; имеет атомный номер – 51. Простое вещество сурьма —полуметалл серебристо-белого цвета с синеватым оттенком, грубозернистого строения. Известны четыре металлических аллотропных модификаций сурьмы, существующих при различных давлениях, и три аморфные модификации (взрывчатая, чёрная и жёлтая сурьма).
Слайд 3

ИСТОРИЯ
Сурьма известна с глубокой древности. В странах Востока она использовалась примерно
за 3000 лет до н. э. для изготовления сосудов. Подробное описание свойств и способов получения сурьмы и её соединений впервые дано алхимиком Василием Валентином (Германия) в 1604 году. В 1789 году А. Лавуазье включил сурьму в список химических элементов под названием antimoine. Русское слово «сурьма» произошло от турецкого и крымско-татарского sürmä: им обозначался порошок свинцового блеска PbS, также служивший для чернения бровей (по другим данным, «сурьма» — от персидского «сурме» — металл).
Слайд 4

НАХОЖДЕНИЕ В ПРИРОДЕ
Месторождения сурьмы известны в ЮАР, Алжире, Армении, Таджикистане, Болгарии,
Якутии, Финляндии, Китае, Киргизии.
Слайд 5

ФИЗИЧЕСКИЕ СВОЙСТВА
Сурьма в свободном состоянии образует серебристо-белые кристаллы с металлическим блеском,
плотность — 6,68 г/см³. Напоминая внешним видом металл, кристаллическая сурьма обладает большей хрупкостью и меньшей тепло- и электропроводностью. В отличие от большинства других металлов, при застывании расширяется. Примесь сурьмы понижает точки плавления и кристаллизации свинца, а сам сплав при отвердении несколько расширяется в объёме.
Температура плавления - 6305°C;
Температура кипения - 1634°C.
Слайд 6

ХИМИЧЕСКИЕ СВОЙСТВА
1) В соединениях проявляет степени окисления +5, +3 и -3
2)
С кислородом взаимодействует при температуре выше 630°C с образованием Sb2O3
3) При сплавлении с серой получаются сульфиды сурьмы, также взаимодействует с фосфором и мышьяком.
Слайд 7

ПОЛУЧЕНИЕ СУРЬМЫ
Существует два метода:
1) Сплавление сульфида с железом (метод вытеснения) –
Sb2S3 + 3Fe = 2Sb + 3FeS
2) Обжиг сульфида и восстановление полученной четырехокиси сурьмы углем (метод обжига-восстановления) –
Sb2S3 + 5O2 = Sb2O4 + 3SO2 Sb2O4 + 4C = 2Sb + 4CO






 Пестициды. Лекция
Пестициды. Лекция Энергетическое топливо
Энергетическое топливо Степень окисления
Степень окисления Химиялық өнеркәсіп шикізаты . Шикізат көздері Химиялық өндірістегі энергия және энергия көздері
Химиялық өнеркәсіп шикізаты . Шикізат көздері Химиялық өндірістегі энергия және энергия көздері Мыльная история. (3 класс)
Мыльная история. (3 класс) Соединения кремния
Соединения кремния Получение азотной кислоты
Получение азотной кислоты Знакомство с лабораторным оборудованием
Знакомство с лабораторным оборудованием Получение галогенов. Биологическое значение и применение галогенов
Получение галогенов. Биологическое значение и применение галогенов Биохимия. Лекция 7. Углеводы
Биохимия. Лекция 7. Углеводы Total Synthesis of (−) - Lepenine
Total Synthesis of (−) - Lepenine Стали и чугуны. Классификация и маркировка
Стали и чугуны. Классификация и маркировка Подгруппа азота. 9 класс
Подгруппа азота. 9 класс Щелочи
Щелочи Азотная кислота и нитраты
Азотная кислота и нитраты Жёсткость воды и способы её устранения
Жёсткость воды и способы её устранения Ерітінділер туралы ілім. Буферлік ерітінділер
Ерітінділер туралы ілім. Буферлік ерітінділер Redox Reactions
Redox Reactions Строение атомов. Понятие о квантовой механике
Строение атомов. Понятие о квантовой механике Технология производства хлорбензола
Технология производства хлорбензола Химиялық реакция белгілерін атаңыз
Химиялық реакция белгілерін атаңыз Коррозия металлов
Коррозия металлов МЫШЬЯК
МЫШЬЯК Относительная молекулярная масса
Относительная молекулярная масса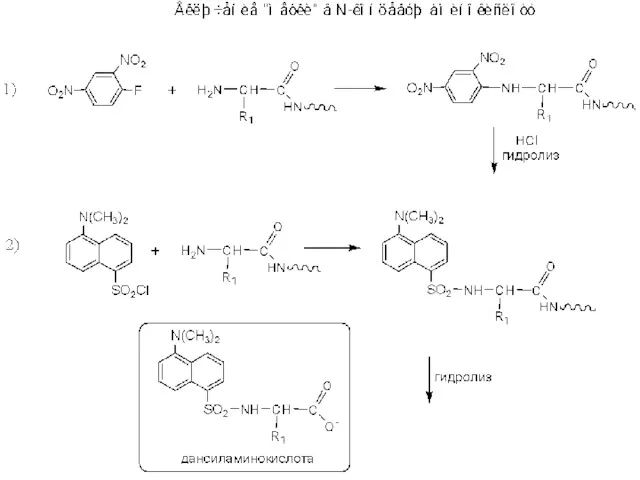 Установление структуры биополимеров
Установление структуры биополимеров Классификация строительных материалов. Коррозия бетона и железобетона
Классификация строительных материалов. Коррозия бетона и железобетона Биофизическая химия. Предмет и задачи курса
Биофизическая химия. Предмет и задачи курса Буферное кислотно - основное взаимодействие
Буферное кислотно - основное взаимодействие