Содержание
- 2. Этические проблемы в системе доклинических и клинических испытаний ЛС Цель доклинических исследований ЛС – получение научными
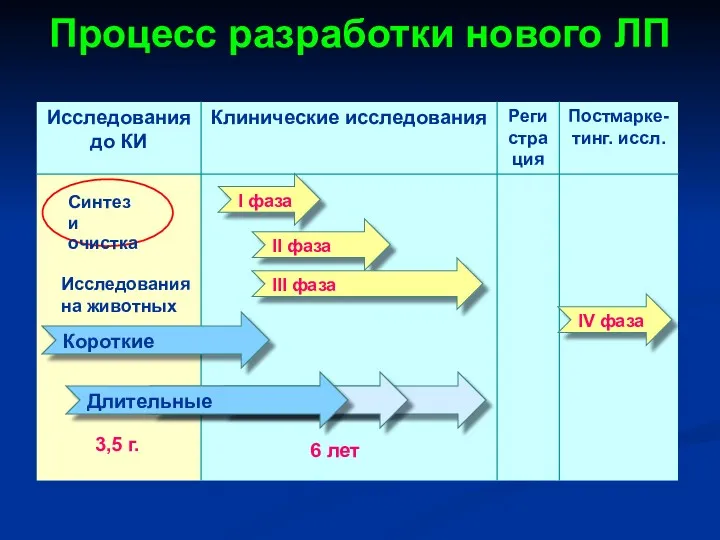
- 3. Процесс разработки нового ЛП Синтез и очистка Исследования на животных Короткие Длительные І фаза ІІ фаза
- 4. Регулирование исследований Европейская конвенция о защите позвоночных животных, которые используются для исследовательских и других научных целей,
- 5. Этические принципы Обоснованность (необходимость) исследований. Альтернативные методы Возможность получить в ходе исследования необходимый результат (результативность) Адекватность
- 6. Требования этичности эксперимента В принципе использование животных для научных целей нежелательно; - по возможности следует применять
- 7. Принцип «трех R» Замена ("replacement") - переход, по мере возможности, на использование вместо животных математических моделей,
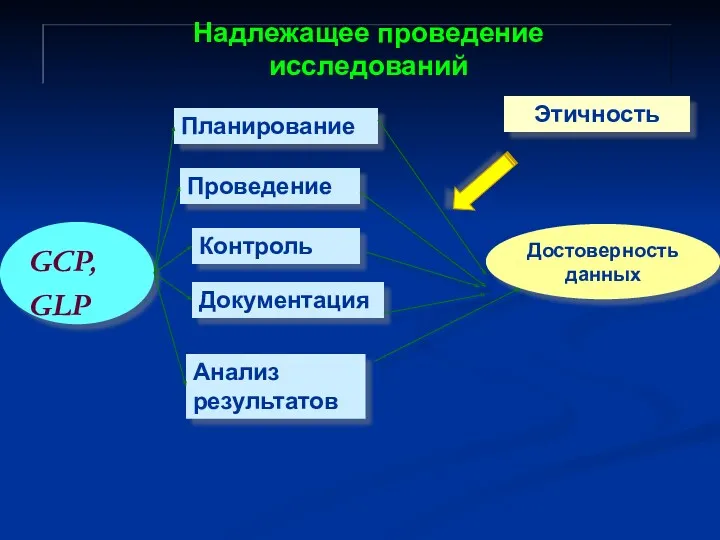
- 9. GCP, GLP Планирование Проведение Контроль Анализ результатов Достоверность данных Документация Этичность Надлежащее проведение исследований
- 10. Альтернативные методы экспериментирования - улучшенная система хранения и использования информации, а также обмен информацией об экспериментах,
- 11. «Чем полнее будет проделан опыт на животных, тем менее часто больным придется быть в положении опытного
- 12. Цель Комитета: содействовать внедрению современных этических стандартов и соблюдению принципов высокой морали при проведении исследований с
- 13. ЭК ведет список своих членов с указанием их квалификации Рекомендации к составу ЭК доклинические исследования: врача-ветеринара
- 14. Деятельность ЭК Одобрение исследований (план проведения, этичность, квалификация исследователей, пригодность помещений, внесение изменений) Мониторинг соблюдения этичности
- 15. ДОКЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ Фармакологическая активность действующего вещества (первичная и вторичная фармакодинамика; фармакология безопасности); Фармакокинетика (абсорбция, распределение, метаболизм,
- 16. Внедрение фармакологических препаратов в клинику – поэтапный процесс, который включает в себя оценку данных безопасности, полученных
- 17. ГРУППЫ ЛС, ДЛЯ КОТОРЫХ НЕОБХОДИМО ПРОВЕДЕНИЕ ДИ Новые ЛС; Препараты – генерики; ЛС, для которых внесены
- 18. НОВЫЕ ЛС ВИДЫ ТОКСИКОЛОГИЧЕСКИХ ИССЛЕДОВАНИЙ: острая токсичность (одноразовое введение); хроническая токсичность (многоразовое введение); репродуктивная токсичность; генотоксичность;
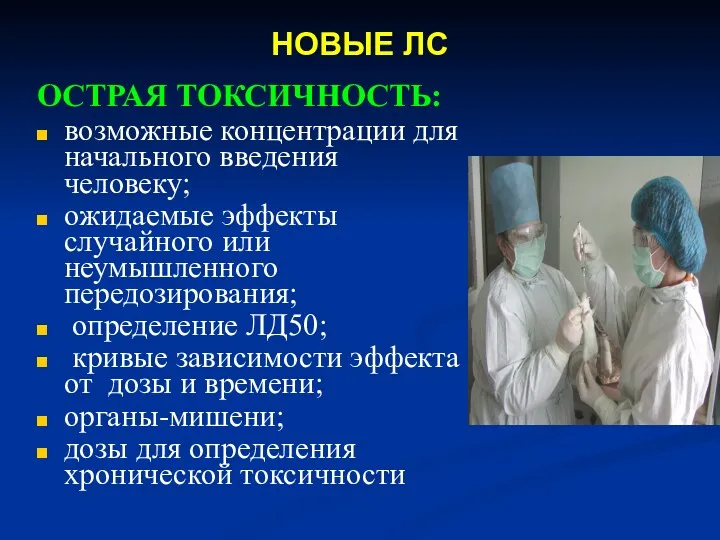
- 19. ОСТРАЯ ТОКСИЧНОСТЬ: возможные концентрации для начального введения человеку; ожидаемые эффекты случайного или неумышленного передозирования; определение ЛД50;
- 20. НОВЫЕ ЛС ХРОНИЧЕСКАЯ ТОКСИЧНОСТЬ: - зависимость от дозы и длительности экспозиции; - определение органов-мишеней; - оценка
- 21. НОВЫЕ ЛС ЭМБРИОТОКСИЧНОСТЬ И ТЕРАТОГЕННОСТЬ НОВЫХ ЛС проводят в случае, если ЛС предлагается для использования при
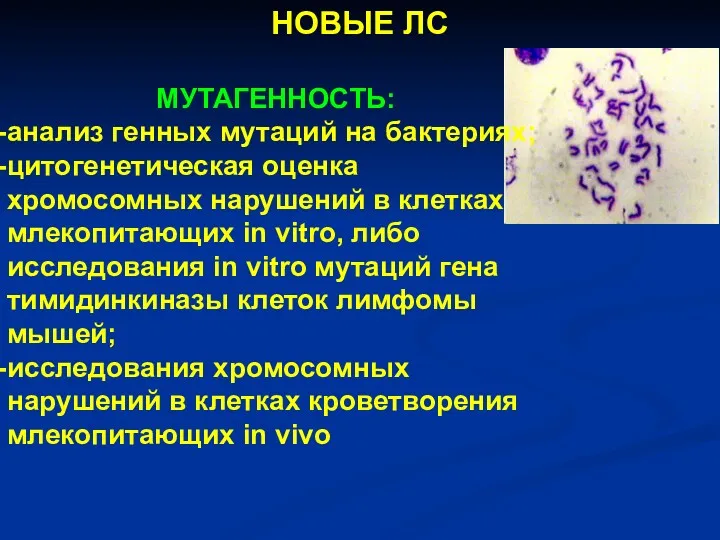
- 22. НОВЫЕ ЛС МУТАГЕННОСТЬ: анализ генных мутаций на бактериях; цитогенетическая оценка хромосомных нарушений в клетках млекопитающих in
- 23. НОВЫЕ ЛС КАНЦЕРОГЕННЫЙ ПОТЕНЦИАЛ: Исследования проводят если: получен позитивный результат в отношении мутагенности нового ЛС; ЛС
- 24. НОВЫЕ ЛС КАНЦЕРОГЕННЫЙ ПОТЕНЦИАЛ: (продолжение) - ЛС относится к классу веществ с канцерогенным действием; структура-активность указывает
- 25. НОВЫЕ ЛС В случае местного применения (кожа, глаза), а также при условии гарантии отсутствия системного действия
- 26. РЕЗУЛЬТАТЫ ТОКСИКОЛОГИЧЕСКИХ ИССЛЕДОВАНИЙ: данные комплексных токсикологических исследований; установление органов-мишеней; зависимость «доза – эффект»; обратимость выявленных эффектов.
- 27. РЕЗУЛЬТАТЫ ФАРМАКОЛОГИЧЕСКИХ ИССЛЕДОВАНИЙ: количественные показатели эффективности (ЕД 50); кривая зависимости «доза – эффект»; сравнения с данными
- 28. НОВЫЕ ЛС ФАРМАКОЛОГИЯ БЕЗОПАСНОСТИ Установления влияния ЛС на основные функции организма: ССС; Дыхательная система; ЦНС; Мочеполовая
- 29. НОВЫЕ ЛС ФАРМАКОКИНЕТИКА Исследования фармакокинетических параметров должны предоставить данные про метаболизм и выведение действующего вещества из
- 30. НОВЫЕ ЛС Исследования распределения исследуемого ЛС в тканях при повторном введении проводятся если: - после одноразового
- 31. доклинические исследования токсичности и фармакологической спецефичности и эффективности не проводят если предоставлены: данные, которые доказывают эквивалентность
- 32. ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ - ГЕНЕРИКИ В других случаях изучается: острая токсичность в сравнении с референс-препаратом (оригинальным) на
- 33. ИЗМЕНЕНИЯ В ЛС, ТРЕБУЮЩИЕ НОВОЙ РЕГИСТРАЦИИ: изменения действующих веществ; изменения терапевтических показаний; изменения дозирования, лекарственной формы
- 34. ИЗМЕНЕНИЯ В ЛС Доклинические исследования в объеме, установленном для новых дейтсвующих веществ проводятся если: изменение одного
- 35. ИЗМЕНЕНИЯ В ТЕРАПЕВТИЧЕСКИХ ПОКАЗАНИЯХЛС В случае, если изменения терапевтических показаний, т.е. расширение показаний касаются другой терапевтической
- 36. ИЗМЕНЕНИЯ В ЛС, КАСАЮЩИЕСЯ ДОЗИРОВАНИЯ ЛС И СПОСОБА ПРИМЕНЕНИЯ Проводится сравнительное исследование фармакологической эффективности на нескольких
- 37. ЛС РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ Лекарственные средства растительного поисхождения, которые содержат растительное сырье, не описанное в Европейской фармакопее/или
- 38. ЛС РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ Традиционные в Украине ЛС из растительного сырья для перорального применения, безопасность которых подтверждена
- 39. ЛС РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ В случае, если растительные сборы содержат хорощо известные в Украине составляющие, безопасность которых.
- 41. Скачать презентацию


































 Неонатальный период после рождения ребенка
Неонатальный период после рождения ребенка Патология иммунной системы
Патология иммунной системы Понятие об онтогенезе. Введение в эмбриологию
Понятие об онтогенезе. Введение в эмбриологию Созылмалы аурулармен, және аурудың өршуі кезінде үй жағдайындағы мейіргерлік күтімі
Созылмалы аурулармен, және аурудың өршуі кезінде үй жағдайындағы мейіргерлік күтімі Скарлатина кезіндегі шаралардың стандарттары және алгоритмдері
Скарлатина кезіндегі шаралардың стандарттары және алгоритмдері Иммунитет. Виды иммунитета
Иммунитет. Виды иммунитета Работоспособность женщин
Работоспособность женщин Анкилоздағыш спондилоартрит (бехтерев ауруы)
Анкилоздағыш спондилоартрит (бехтерев ауруы) SAM иммобилизация таза II
SAM иммобилизация таза II Обращение с медицинскими отходами
Обращение с медицинскими отходами Мемлекеттік бақылау және қадағалау туралы
Мемлекеттік бақылау және қадағалау туралы Паранеопластический синдром. Общая характеристика ПНС
Паранеопластический синдром. Общая характеристика ПНС Биомаркеры ишемического инсульта
Биомаркеры ишемического инсульта Рани. Види ран
Рани. Види ран Понятие здоровье и болезнь. Этика и деонтология в медицине
Понятие здоровье и болезнь. Этика и деонтология в медицине Организация работы медицинской сестры при сборе и утилизации медицинских отходов
Организация работы медицинской сестры при сборе и утилизации медицинских отходов Пародонтит у детей. Этиология, патогенез, клиника, диагностика, дифференциальная диагностика, лечение
Пародонтит у детей. Этиология, патогенез, клиника, диагностика, дифференциальная диагностика, лечение СПИД – чума 21 века
СПИД – чума 21 века ДВС-синдром. Система гемостаза
ДВС-синдром. Система гемостаза Екатерина Бакунина – основоположница сестринского дела в России
Екатерина Бакунина – основоположница сестринского дела в России Лейкоциттік формуланы, лимфоциттердіѕ абсолюттік жјне салыстырмалы санын есептеу
Лейкоциттік формуланы, лимфоциттердіѕ абсолюттік жјне салыстырмалы санын есептеу Синдром удлиненного интервала QT
Синдром удлиненного интервала QT IV, V, VI нервтар
IV, V, VI нервтар Диагностика туберкулеза и рака легких
Диагностика туберкулеза и рака легких Этические аспекты деятельности ВОП. Врачебная тайна
Этические аспекты деятельности ВОП. Врачебная тайна Стоматиты и гельминтозы у детей
Стоматиты и гельминтозы у детей Врожденная олигофрения. Геронтопсихиатрия. Негативные психопатологические синдромы
Врожденная олигофрения. Геронтопсихиатрия. Негативные психопатологические синдромы Пищевые отравления немикробной этиологии
Пищевые отравления немикробной этиологии