Содержание
- 2. Фибрилляция предсердий– это нарушение сердечного ритма, при котором на протяжении всего сердечного цикла наблюдается частое (от
- 3. Раньше эта аритмия называлась arhythmia perpetua, т. е. вечная, постоянная аритмия. Однако в настоящее время доказано,
- 4. ФП по своей природе является полиэтиологическим и гетерогенным нарушением ритма. Существует ряд заболевания, в той или
- 5. Заболевания сердечно-сосудистой системы органического генеза, сопровождающиеся поражением клапанов сердца: Хроническая ревматическая болезнь сердца (наиболее широко представленная
- 6. 2. Заболевания сердечно-сосудистой системы органического генеза, не связанные с поражением клапанного аппарата: Ишемическая болезнь сердца –
- 7. 3. Внесердечные заболевания, приводящие к развитию ФП: Хронические обструктивные заболевания легких Тиреотоксикоз 4. Идиопатическая форма ФП
- 8. Т.к. ФП может быть Пароксизмальной, т.е. проявляться в виде периодически возникающих приступов и Перманентной (постоянной), то
- 9. Каковы причины пароксизмальной ФП?
- 10. Каковы причины перманентной ФП?
- 11. У 25-35% больных причину ФП установить не удается, а детальное обследование сердечно-сосудистой системы (включая ЭхоКГ) у
- 12. С клинической точки зрения целесообразно подразделять все имеющиеся причины возникновения ФП на 4 основные группы: Острые
- 13. ФП может быть связана с острыми, временными причинами, такими, как прием алкоголя («синдром праздничного сердца»), хирургическое
- 14. Из названия нетрудно догадаться, что в развитии нейрогенной формы играет роль вегетативная нервная cистема. Кумель описал
- 15. Вагус-индуцированный («вагусный») вариант ФП развивается в результате рефлекторного воздействия на сердце блуждающего нерва, что укорачивает эффективный
- 16. Вагусная форма ФП характеризуется следующими особенностями: частота встречаемости у мужчин в 4 раза выше, чем у
- 17. Гиперадренергический вариант ФП возникает чаще у лиц (чаще женщин) с повышенной активностью САС. Так же, как
- 18. Встречается реже, чем вагусная; приступ ФП обычно развивается утром или днем, после физической или психоэмоциональной нагрузки
- 19. Фибрилляция предсердий – сложная аритмия, патогенез которой до конца не изучен. Развитию ФП предшествуют многочисленные патофизиологические
- 20. Каковы «факторы риска» ФП?
- 21. Среди анатомических факторов риска ведущее место отводится дилатации и гипертрофии ЛП до определенного «критического» уровня, а
- 22. В настоящее время имеются 2 теории, объясняющих механизмы ФП. 1. Повторный вход волны возбуждения (re-entry) 2.
- 23. Выделяют «первичную» ФП, в генезе которой не имеет значения перегрузка давлением и объемом при алкогольной интоксикации,
- 24. Во всех этих случаях выявляется выраженная электрическая негомогенность миокарда предсердий, которая лежит в основе формирования механизма
- 25. Устойчивая повторяемость феномена re-entry, сопровождающаяся длительной циркуляцией волны возбуждения по замкнутой петле, возможна только в том
- 26. При ФП в предсердиях образуются множественные волны microre-entry, не менее 5-6. При этом направление волны возбуждения
- 27. Согласно другой теории, ФП вызывается частым образованием импульсов в нескольких эктопических предсердных очагах. Происхождение ФП связывают
- 28. Повышенный автоматизм и множественные очаги циркуляции возбуждения re-entry, не исключают друг друга и могут сочетаться. Современная
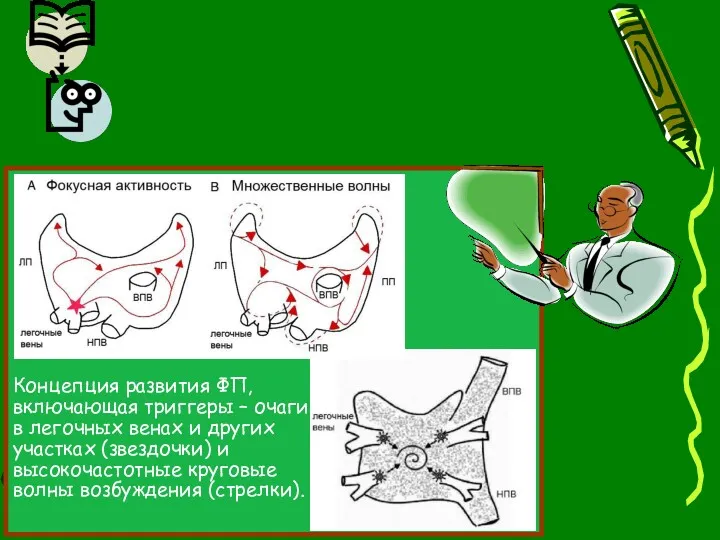
- 29. Концепция развития ФП, включающая триггеры – очаги в легочных венах и других участках (звездочки) и высокочастотные
- 30. Ткань предсердий в легочных венах у больных с ФП характеризуется более коротким рефрактерным периодом по сравнению
- 31. ФП вызывают предсердные экстрасистолы или импульсы ЭКС, которые попадают в уязвимый период сердечного цикла, а также,
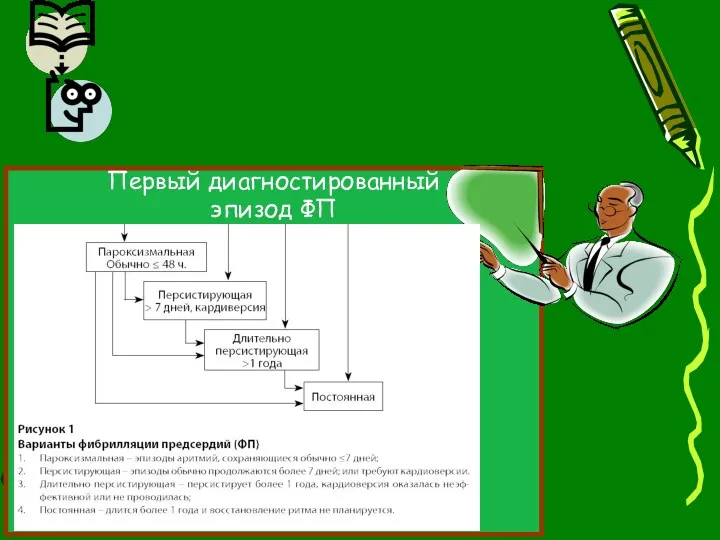
- 32. Исходя из манифестации и продолжительности аритмии, клинически целесообразно выделить пять (форм) типов ФП. Согласно новым Рекомендациям
- 33. Первый диагностированный эпизод ФП
- 34. Как пароксизмальная, так и персистирующая форма ФП могут быть рецидивирующими. Если у пациента было 2 приступа
- 35. Аритмия стремится к прогрессу от пароксизмальной через персистирующую и длительную персистирующую и в конечном итоге к
- 36. В зависимости от частоты желудочковых сокращений различают следующие формы ФП: брадисистолическая форма – число желудочковых сокращений
- 37. Частота желудочкового ритма зависит от электрофизиологических свойств атриовентрикулярного узла и других проводящих тканей, тонуса симпатической и
- 38. ЭКГ-признаки ФП : 1. Отсутствие во всех ЭКГ-отведениях зубца Р. 2. Наличие на протяжении всего сердечного
- 40. Клиническая картина у больных ФП определяется, с одной стороны, симптоматикой основного заболевания, с другой стороны, наличием
- 41. При ФП наблюдается беспорядочное появление пульсовых волн (аритмия пульса); постоянно меняющаяся амплитуда пульсовых волн; дефицит пульса
- 42. При аускультации сердца можно Выявить следующие признаки ФП: абсолютно беспорядочная, аритмичная деятельность сердца (delirium cordis); постоянно
- 43. Влияние ФП на гемодинамику зависит от частоты желудочковых сокращений длительности аритмии состояния сократительного миокарда. Таким образом,
- 44. Каковы последствия ФП?
- 45. Основными осложнениями ФП являются Сердечная недостаточность и системные тромбоэмболии. У больных с синдромом WPW возможна ее
- 46. Риск инсульта и системной эмболии у пациентов с ФП связан с числом лежащих в их основе
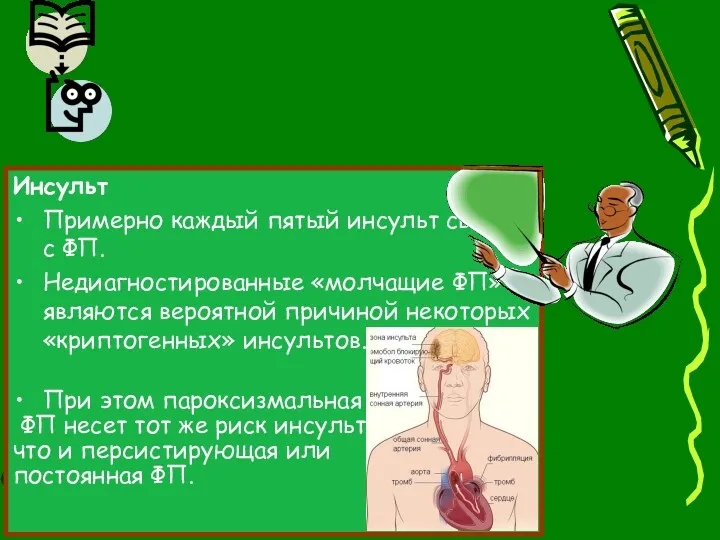
- 47. Инсульт Примерно каждый пятый инсульт связан с ФП. Недиагностированные «молчащие ФП» являются вероятной причиной некоторых «криптогенных»
- 48. На фоне тахисистолии развиваются диастолическая сократительная дисфункция миокарда ЛЖ, в дальнейшем - систолическая сократительная дисфункция и
- 49. У пациента с подозреваемой или выявленной ФП должна быть тщательно собран анамнез. Cоответствующие вопросы для пациентов
- 50. Клиническая оценка должна включать определение состояния по шкале EHRA , оценку риска инсульта и поиск обстоятельств,
- 51. Шкала EHRA (European Heart Rhythm Association) – это шкала тяжести ФП Значение Характеристика Что такое шкала
- 52. Факторы риска инсульта условно делятся на категории риска инсульта "высокий", "умеренный" и "низкий". Для оценки риска
- 53. Критерии основаны на балльной системе, в которых 2 балла предназначены для перенесших инсульт или ТИА и
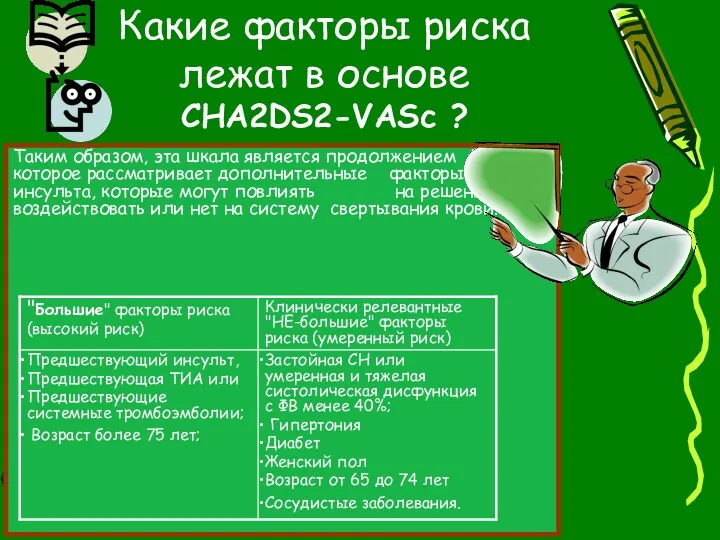
- 54. Однако, так как CHADS2 оценка не включает в себя многие факторы риска инсульта, была предложена более
- 55. Таким образом, эта шкала является продолжением CHADS2, которое рассматривает дополнительные факторы риска инсульта, которые могут повлиять
- 56. Основанная на балльной оценке факторов риска шкала CHA2DS2-VASc (максимальное количество баллов – 9, оценка возраста может
- 57. Следует искать основные причины ФП. Эхокардиография полезна для обнаружения поражения желудочков, клапанов и предсердий, а также
- 58. Лечение больных ФП направлено на смягчение симптомов и на предотвращение тяжелых осложнений, связанных с ФП. Эти
- 59. Существует два основных метода лечения рецидивов ФП: восстановление и поддержание синусового ритма (rhythm control) и Сохранение
- 60. При контроле ритма выявлены лучшая переносимость физических нагрузок, более высокое качество жизни, тенденция к увеличению риска
- 61. Вопрос о выборе той или иной тактики ведения решается индивидуально. У пожилых пациентов с персистирующей ФП
- 62. Относительно низкая эффективность восстановления и поддержания синусового ритма отмечается в следующих ситуациях: В каких случаях восстановления
- 63. Недавно возникшая ФП ( Основным предиктором высокой частоты спонтанного восстановления синусового ритма является небольшая продолжительность аритмии.
- 65. Быстрое снижение ЧСС с целью уменьшения симптомов применяется в первые сутки ФП, когда ожидают спонтанного прекращения
- 66. Назначают бета–блокаторы, антагонисты кальция и дигоксин, которые редко восстанавливают синусовый ритм. Следует помнить об опасности такого
- 67. Восстанавливают синусовый ритм с помощью фармакологических (пероральных или внутривенных) средств или электроимпульсной терапии (ЭИТ). Каждая методика
- 68. Во время ФП происходят морфологические и электрические изменения предсердий (ремоделирование), которые способствуют сохранению аритмии. Поэтому нужно
- 69. Обычно назначают варфарин в дозе 5 мг/сут и подбирают дозу по МНО (2–3). До развертывания эффекта
- 70. Пероральный ингибитор тромбина дабигатран (прадакса) предупреждает инсульты и тромбоэмболии также эффективно, как и варфарин (в дозе
- 71. В случае экстренной кардиоверсии при ФП длительностью >48 ч и гемодинамическими осложнениями (стенокардия, инфаркт миокарда, шок,
- 72. После электрической и, по–видимому, медикаментозной кардиоверсии развивается состояние «оглушенных» предсердий (atrial stunning) со снижением сократимости в
- 73. Для восстановления синусового ритма можно использовать препараты IА, IС и III класса. В целом наибольший эффект
- 74. Медикаментозная кардиоверсия может быть осуществлена пероральными или парентеральными приемом антиаритмических препаратов. Устранение ФП пероральными антиаритмическими препаратами
- 75. Применяют хинидина сульфат, пропафенон и амиодарон. Какие препараты применяют при пероральном приеме?
- 76. Если состояние пациентов стабильное, а безопасность и эффективность препаратов подтверждены в стационаре, то пациенты могут самостоятельно
- 77. Назначение хинидина в больших дозах требует стационарных условий, вследствие риска синдрома удлиненного интервала QT. Поэтому во
- 78. Амиодарон при пероральном приеме в дозе 30 мг/кг однократно восстанавливал синусовый ритм в 52% через 8
- 79. Наиболее эффективны для восстановления синусового ритма препараты 1С и 3 класса Какие препараты используются при парентеральной
- 80. Вместе с тем препараты 1А и 1С класса могут вызвать выраженную тахикардию (часто ширококомплексную), связанную с
- 81. Некоторые специалисты после введения основной дозы антиаритмического препарата для повышения эффективности кардиоверсии и профилактики ранних рецидивов
- 82. Антиаритмический эффект амиодарона в первые 2–6 ч не отличается от плацебо, но через 24 ч частота
- 83. Чаще всего используют трансторакальную кардиоверсию, эффективность которой повышается с увеличением разряда, но возрастает риск повреждения миокарда.
- 84. При монофазном дефибрилляторе рекомендуют начинать с разряда 200 дж, а в случае отсутствия эффекта с интервалом
- 85. При популярном гибридном методе восстановления синусового ритма вначале назначают антиаритмические препараты, а затем при неэффективности последних
- 87. Если причину тахиаритмии не удается устранить, то без лечения ФП рецидивирует в течение года в 80%
- 88. Профилактика рецидивов, т.е. длительная терапия контроля ритма, может осуществляться медикаментозными и немедикаментозными методами. Медикаментозная профилактика рецидивов
- 89. При первом эпизоде ФП профилактическое лечение обычно не проводят, поскольку следующий эпизод аритмии может развиться через
- 90. Выбор препарата определятся в основном наличием структурного поражения сердца и сопутствующей патологией. Чем определяется выбор препарата
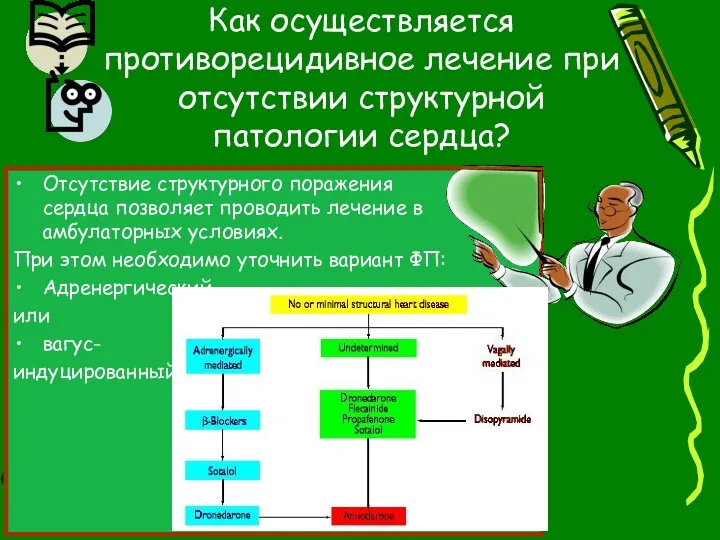
- 91. Отсутствие структурного поражения сердца позволяет проводить лечение в амбулаторных условиях. При этом необходимо уточнить вариант ФП:
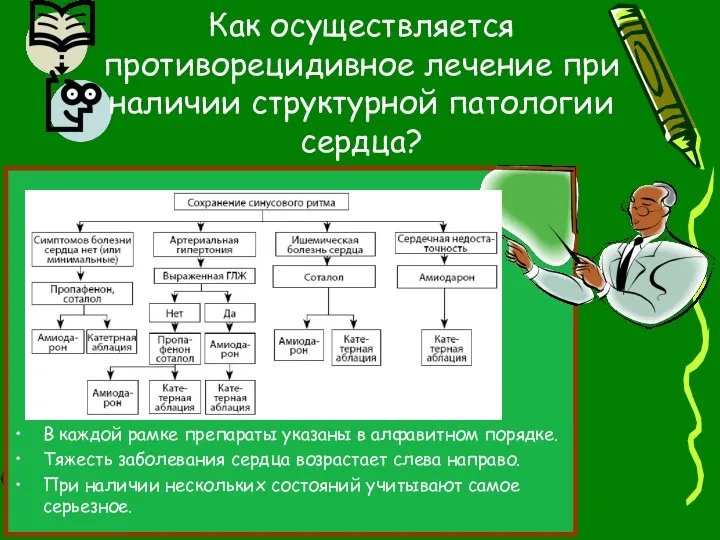
- 92. В каждой рамке препараты указаны в алфавитном порядке. Тяжесть заболевания сердца возрастает слева направо. При наличии
- 93. Немедикаментозные методы для профилактики рецидивов ФП включают Хирургическую абляцию и Катетерную абляцию эктопического очага. Какие немедикаментозные
- 94. В настоящее время применяется процедура Mazе-III, которая стала техникой выбора при хирургической коррекции фибрилляции предсердий. Операция
- 95. Какие имеются показания к хирургической абляции?
- 96. Операция электрофизиологически обоснована и анатомически ориентирована. Основана на теории множественных кругов macro re-entry, формирующихся вокруг анатомических
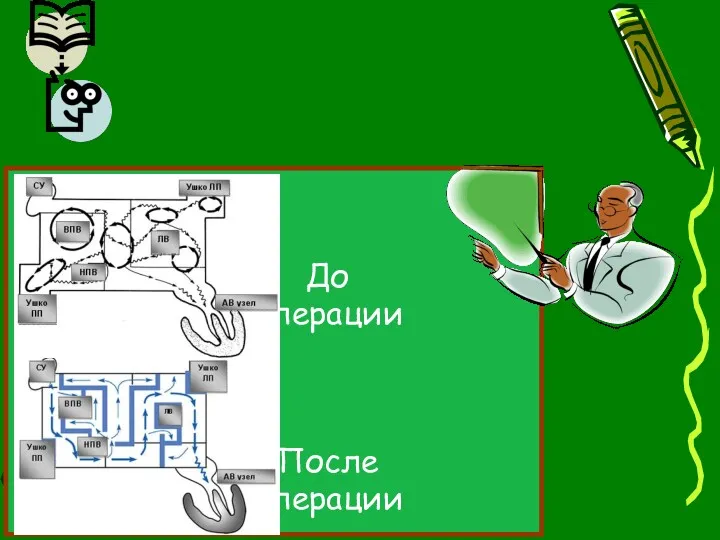
- 97. Хирургические разрезы проводятся таким образом, чтобы электрический импульс, выходя из любой точки предсердия, не мог вернуться
- 98. До операции После операции
- 99. Необходимость операции на открытом сердце с длительным периодом искусственного кровообращения, техническая сложность и высокая стоимость сдерживают
- 100. Для этого предложены: криовоздействие, радиочастотная, микроволновая, лазерная энергии и высокочастотный фокусированный ультразвук. В последние годы шире
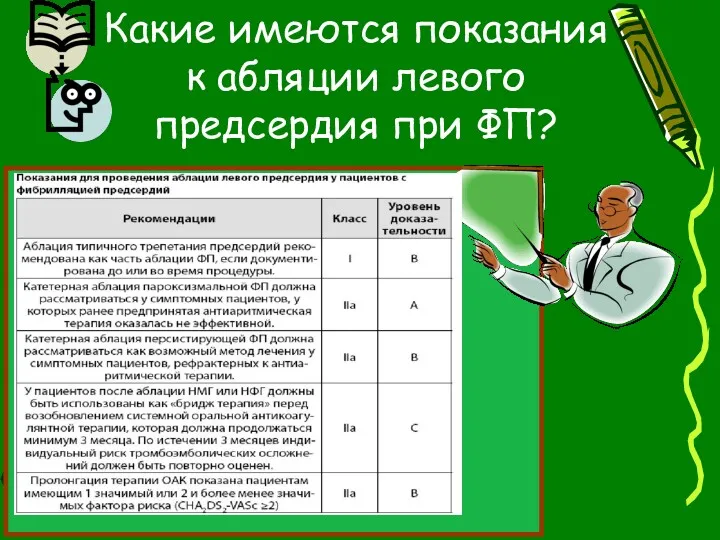
- 101. Какие имеются показания к абляции левого предсердия при ФП?
- 103. Многие пациенты лучше переносят постоянную ФП, чем периодически рецидивирующую аритмию. Поэтому если профилактическая антиаритмическая терапия малоэффективна,
- 104. Функциональный рефрактерный период атриовентрикулярного узла обратно коррелирует с частотой желудочкового ритма во время ФП, поэтому препараты,
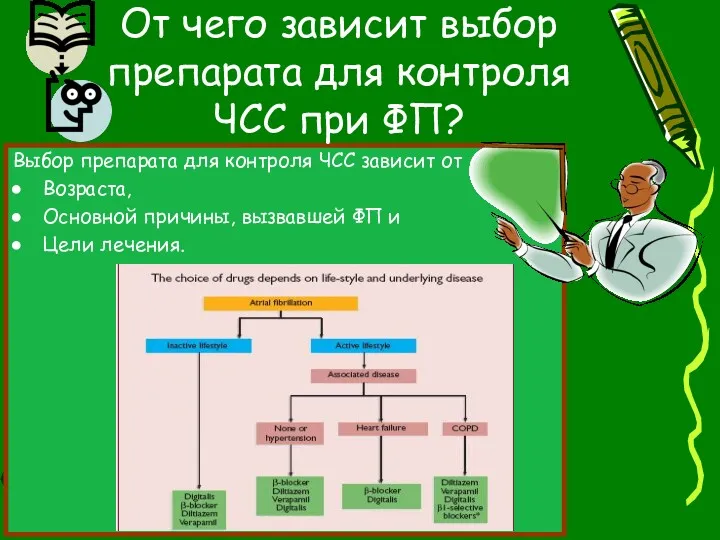
- 106. Выбор препарата для контроля ЧСС зависит от Возраста, Основной причины, вызвавшей ФП и Цели лечения. От
- 107. При дисфункции левого желудочка предпочтение отдают сердечным гликозидам. Поскольку эффект дигоксина обусловлен ваготонией, часто с его
- 108. Если сократимость левого желудочка не страдает, то назначают бета–блокаторы или антагонисты кальция. Встречаются случаи рефрактерной тахикардии
- 109. Во время постоянной ФП рекомендуют поддерживать невысокую частоту сокращений желудочков (AFFIRM): Возможно использование нагрузочного теста для
- 110. Существуют следующие методы немедикаментозного контроля ЧСС при ФП: Регуляция атриовентрикулярного проведения с помощью стимуляции и Аблация
- 111. Кардиостимуляция обеспечивает контроль желудочкового ритма у больных с ФП. Стимуляция желудочков удлиняет рефрактерный период АВ узла,
- 112. Контроль ЧСС с помощью катетерной аблация АВ узлаосуществляют двумя способами: модуляция АВ-проведения деструкцией медленных α-путей, деструкция
- 113. C целью контроля ЧСС проводят полную аблацию АВ узла с имплантацией ЭКС, поскольку в большинстве случаев
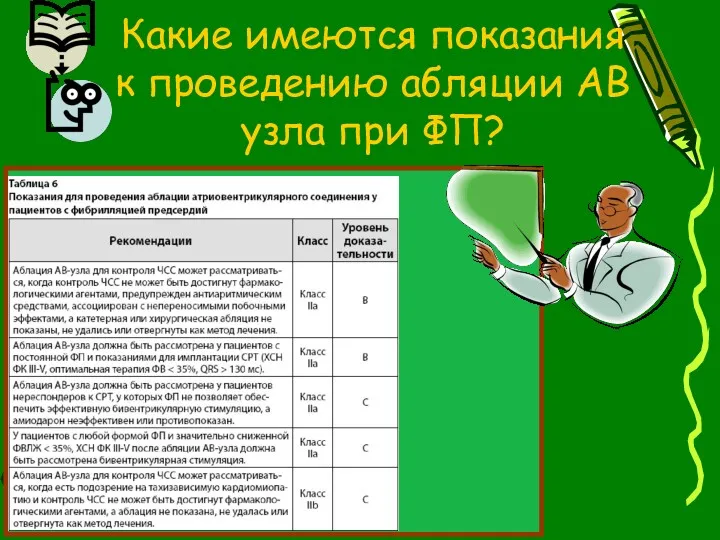
- 114. Какие имеются показания к проведению абляции АВ узла при ФП?
- 116. Бэта-блокаторы рекомендованы в качестве первой линии терапии для контроля частоты желудочкового ритма у пациентов с сердечной
- 117. Абляция AV узла должна быть рассмотрена для контроля ЧЖС, когда другие меры неэффективны или противопоказаны больным
- 118. Upstream-терапия или терапия «против течения» - это т.н. «опережающая терапия». Она направлена на предотвращение или отсрочку
- 119. К upstream-терапии относится применение следующих ЛС: ингибиторами АПФ (ИАПФ), блокаторами рецепторов ангиотензина (БРА), антагонистами альдостерона, статинами,
- 132. Скачать презентацию























































































































 Подходы в диагностике и лечении болезней перикарда
Подходы в диагностике и лечении болезней перикарда Умирание, смерть и трупные изменения
Умирание, смерть и трупные изменения Нейродегенеративные заболевания
Нейродегенеративные заболевания Жүйке жүйесі
Жүйке жүйесі Патофизиология обмена веществ
Патофизиология обмена веществ Жаңа туған нәрестенің физиологиясы және патологиясы
Жаңа туған нәрестенің физиологиясы және патологиясы Лечение в санаториях Белокурихи
Лечение в санаториях Белокурихи Диспансеризация и диспансерное наблюдение
Диспансеризация и диспансерное наблюдение Отходы медицинских учреждений
Отходы медицинских учреждений Вирусные инфекции кожи и слизистых оболочек
Вирусные инфекции кожи и слизистых оболочек Инфекционная безопасность пациентов ОРИТ
Инфекционная безопасность пациентов ОРИТ Биполярное расстройство I типа
Биполярное расстройство I типа Мировые стандарты оказания неотложной медицинской помощи
Мировые стандарты оказания неотложной медицинской помощи Асептика. Определение асептики
Асептика. Определение асептики Свойства рыбы. Рубрика Какая рыба полезнее?
Свойства рыбы. Рубрика Какая рыба полезнее? Олигофрения: классификация, профилактика, пути коррекции
Олигофрения: классификация, профилактика, пути коррекции Дәлелді медицина бойынша қоғам пікірі. Біздің елде және тмд елдеріндегі дәлелді медицина орталықтары
Дәлелді медицина бойынша қоғам пікірі. Біздің елде және тмд елдеріндегі дәлелді медицина орталықтары Дифференциальный диагноз нефротического синдрома
Дифференциальный диагноз нефротического синдрома Режимы аппаратной (механической) вентиляции лёгких
Режимы аппаратной (механической) вентиляции лёгких Генные заболевания
Генные заболевания ВИЧ-инфекция
ВИЧ-инфекция Гнозис и его расстройства
Гнозис и его расстройства Острые респираторные заболевания у детей
Острые респираторные заболевания у детей Методы исследования сердечно-сосудистой системы
Методы исследования сердечно-сосудистой системы Острая ревматическая лихорадка и тактика ведения больных с ревматическими пороками сердца
Острая ревматическая лихорадка и тактика ведения больных с ревматическими пороками сердца Эндодонтическая система K3 Endo (Kerr)
Эндодонтическая система K3 Endo (Kerr) Гнойно-воспалительные заболевания мягких тканей. Медиастинит
Гнойно-воспалительные заболевания мягких тканей. Медиастинит Қан қозғалысының гемодинамикалық заңдылықтары. Қанның реологиялық қасиеттері
Қан қозғалысының гемодинамикалық заңдылықтары. Қанның реологиялық қасиеттері