Содержание
- 2. При попадании в организм антигена возможны три следствия: 1. Выработка иммунитета. 2. Возникновение иммунологической толерантности. 3.
- 3. Основные факторы иммунитета, обеспечивающие защиту от латентных вирусных и бактериальных инфекций Врожденный иммунитет Специфический иммунитет Система
- 7. Фазы иммунного ответа в первые 0-4 часа после попадания возбудителя активируются механизмы врожденного иммунитета. Инфекционные агенты
- 8. СРАВНИТЕЛЬНЫЕ ХАРАКТЕРИСТИКИ КЛЕТОЧНО-ОПОСРЕДОВАННОГО И ГУМОРАЛЬНОГО ИММУНИТЕТА
- 9. ГУМОРАЛЬНЫЙ ИММУННЫЙ ОТВЕТ Активация В-лимфоцитов (В2 CD5-) и их дифференцировка в антителообразующие (АОК) плазматические клетки: Иммуноглобулиновый
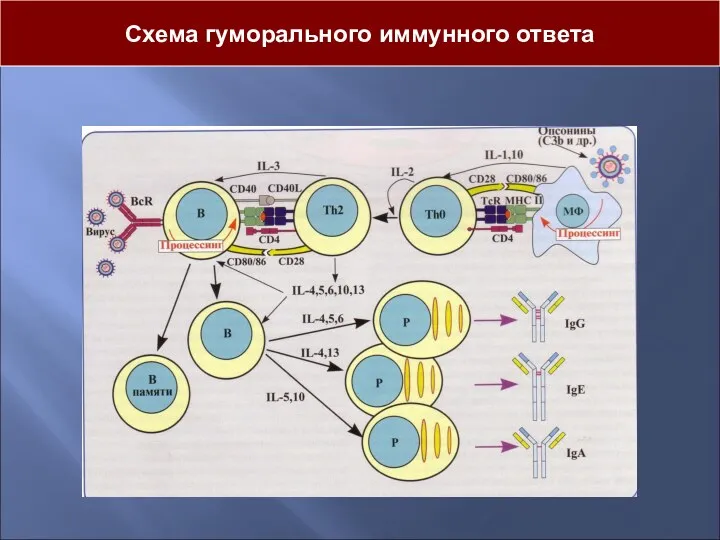
- 10. Схема гуморального иммунного ответа
- 11. Клеточный иммунный ответ Участвуют популяции Тх-1 CD4+ и цитотоксические Т-лимфоциты (CD8+) Антигенпредставляющие клетки, обычно дендритные, после
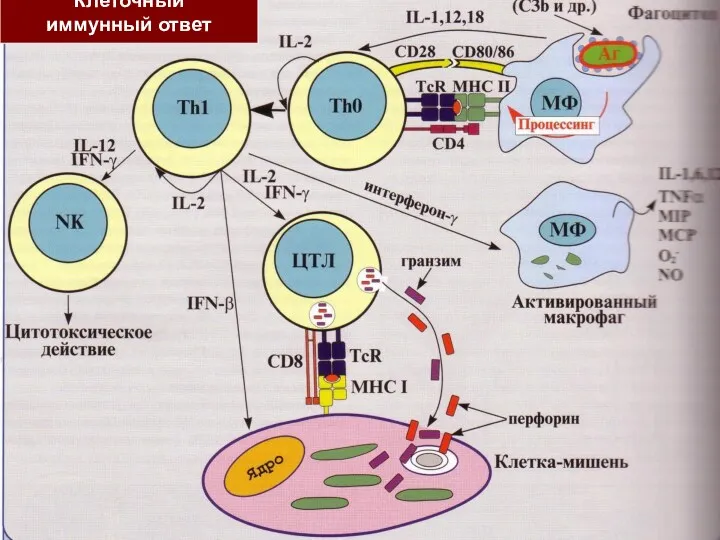
- 12. Клеточный иммунный ответ
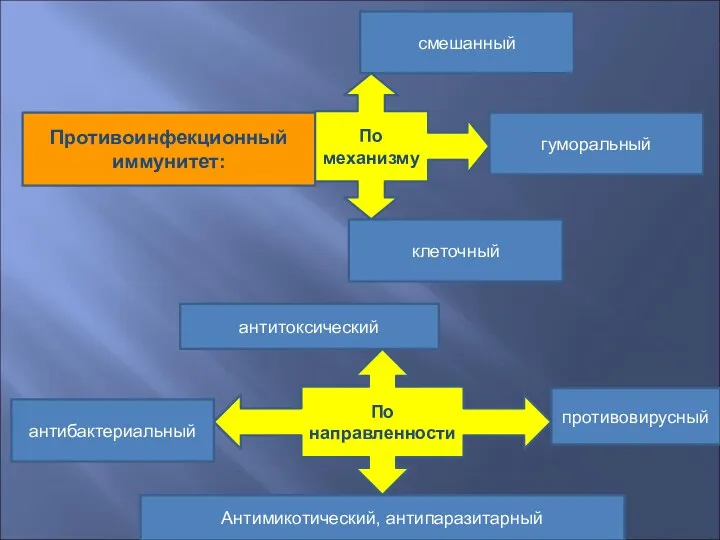
- 13. По механизму По направленности гуморальный клеточный смешанный Противоинфекционный иммунитет: антитоксический антибактериальный противовирусный Антимикотический, антипаразитарный
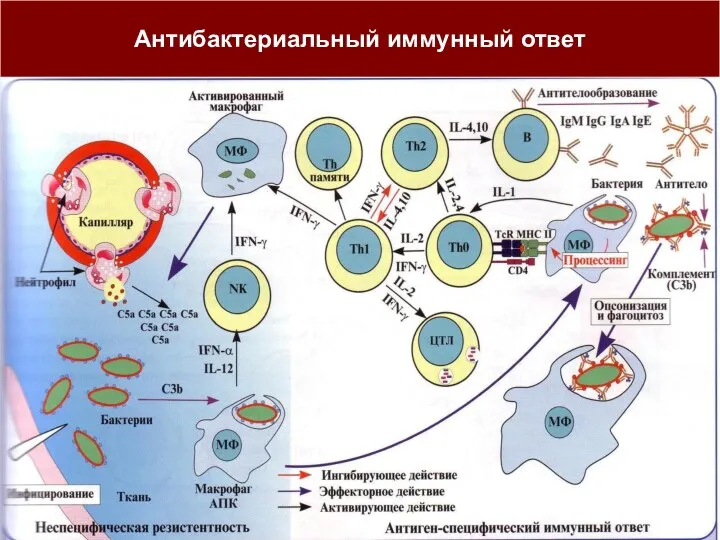
- 14. Особенности иммунитета при бактериальных инфекциях Иммунная реакция макроорганизма в ответ на бактериальную инфекцию в значительной степени
- 15. Основными факторами антибактериальной защиты в подавляющем большинстве случаев являются антитела и фагоциты. Антитела эффективно инактивируют биологически
- 16. Кроме перечисленных, на внедрившиеся бактерии воздействует весь арсенал факторов неспецифической резистентности. Среди них важная роль в
- 17. Ряд бактерий, относящихся к факультативным внутриклеточным паразитам, отличается повышенной устойчивостью к действию комплемента, лизоцима и фагоцитов
- 18. Противобактериальный иммунитет Направлен против бактерий и их токсинов Бактерии и токсины нейтрализуются антибактериальными и антитоксическими антителами
- 19. Антибактериальный иммунный ответ
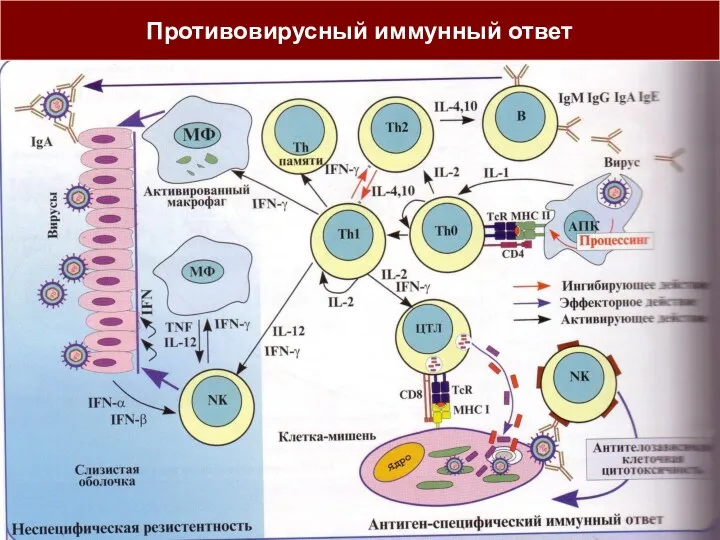
- 20. Особенности противовирусного иммунитета Иммунная защита макроорганизма при вирусных инфекциях имеет особенности, обусловленные двумя формами существования вируса:
- 21. Специфические противовирусные антитела способны взаимодействовать только с внеклеточным вирусом, внутриклеточные структуры прижизненно для них недоступны. Антитела
- 22. Мощным противовирусным действием обладает интерферон. Он не действует непосредственно на внутриклеточный вирус, а связывается с рецептором
- 23. Сывороточные ингибиторы неспецифически связываются с вирусной частицей и нейтрализуют ее, препятствуя тем самым адсорбции вируса на
- 24. Противовирусный иммунитет Основой является клеточный иммунитет Клетки-мишени (инфицированные вирусом) уничтожаются цитотоксическими лимфоцитами, а также NK-клетками и
- 25. Противовирусный иммунный ответ
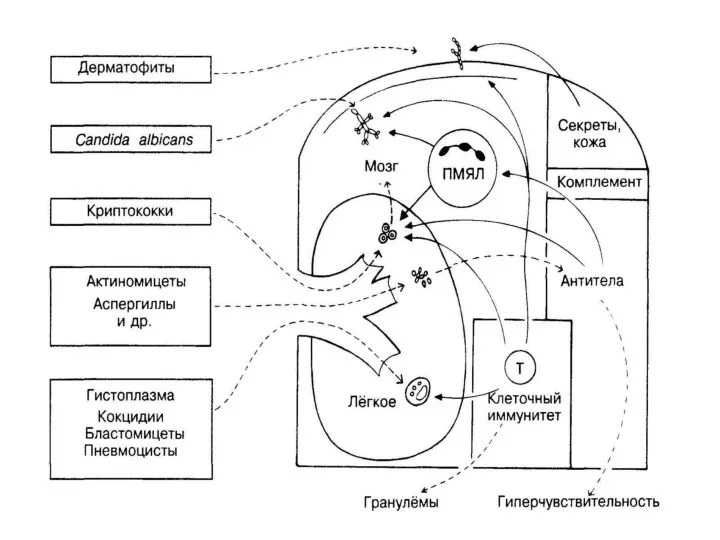
- 26. Особенности противогрибкового иммунитета Антигены грибов имеют относительно низкую иммуногенность: они практически не индуцируют антителообразование (титры специфических
- 27. При микозах наблюдается аллергизация макроорганизма. Кожные и глубокие микозы сопровождаются, как правило, ГЗТ. Грибковые поражения слизистых
- 28. Противогрибковый иммунитет Антитела (IgМ, IgG) при микозах выявляются в низких титрах Основой противогрибкового иммунитета является клеточный
- 31. Особенности иммунитета при протозойных инвазиях Противопаразитарный иммунитет изучен слабо. Известно, что паразитарная инвазия сопровождается формированием в
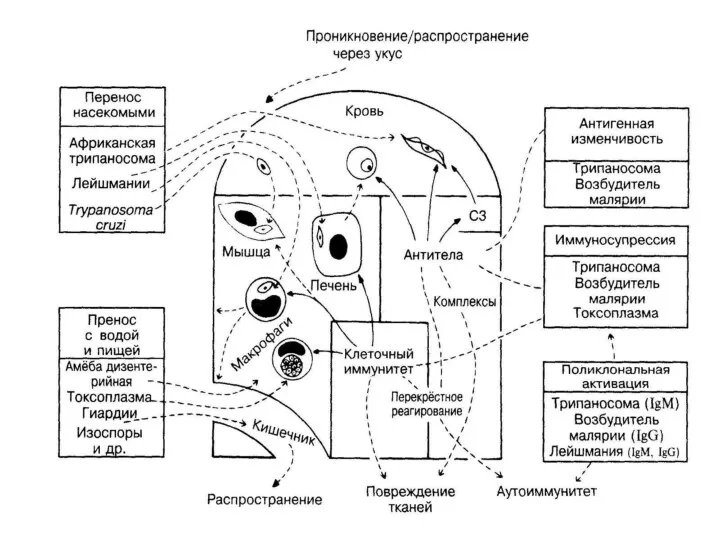
- 32. Характер противопаразитарного иммунитета определяется структурно-функциональными особенностями паразита и его жизненного цикла при инвазии макроорганизма. Многие паразиты
- 33. Противопротозойный иммунитет Антитела (IgМ, IgG) против простейших действуют на внеклеточные формы паразитов. Часто иммунитет является стадиоспецифическим
- 35. Иммунитет при гельминтозах Отличается слабой напряженностью и низкой специфичностью. Иммунологические показатели повышаются преимущественно в личиночную стадию
- 36. Некоторые механизмы, позволяющие паразитирующим организмам избежать воздействия иммунного ответа хозяина
- 37. Противоопухолевый иммунитет Основан на Тх-1-зависимом клеточном иммунном ответе, активирующем ЦТЛ, макрофаги и NK-клетки. Роль гуморального иммунитета
- 38. Адаптивный иммунный ответ к инфекционным агентам может сопровождаться: образованием иммунных комплексов, синтезом перекрестно-реагирующих антител, которые связываются
- 40. Особенности диагностики инфекционных заболеваний
- 41. Иммунологические методы, применяемые для диагностики инфекционных заболеваний РИА ИФЛА Метод прямой иммунофлюоресценции применяют для выявления антигенов.
- 42. Иммунологические методы, применяемые для диагностики инфекционных заболеваний Методы, основанные на реакции преципитации Иммунодиффузия — наиболее распространенный
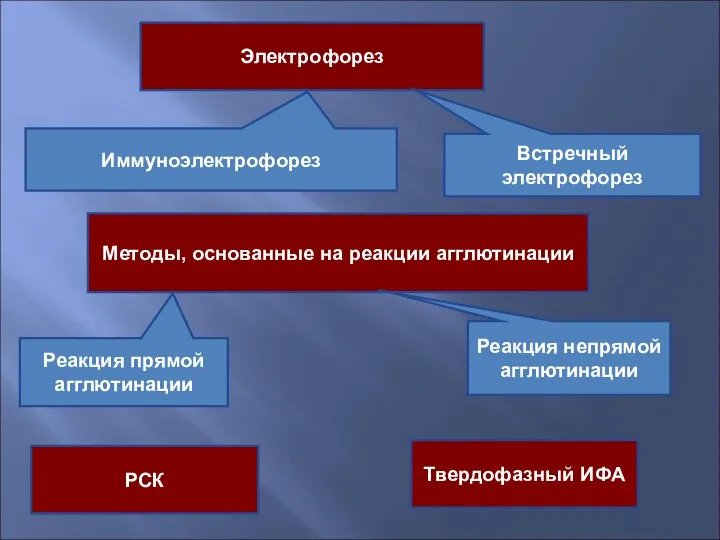
- 43. Электрофорез Иммуноэлектрофорез Встречный электрофорез Методы, основанные на реакции агглютинации Реакция прямой агглютинации Реакция непрямой агглютинации РСК
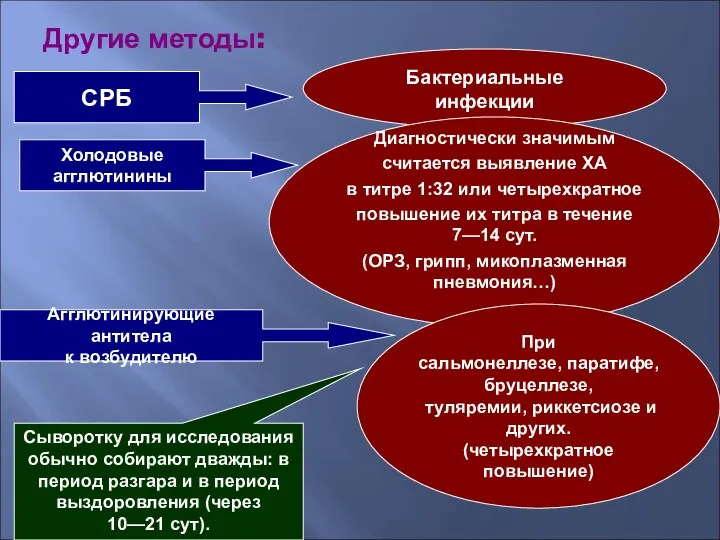
- 44. Другие методы: СРБ Бактериальные инфекции Холодовые агглютинины Диагностически значимым считается выявление ХА в титре 1:32 или
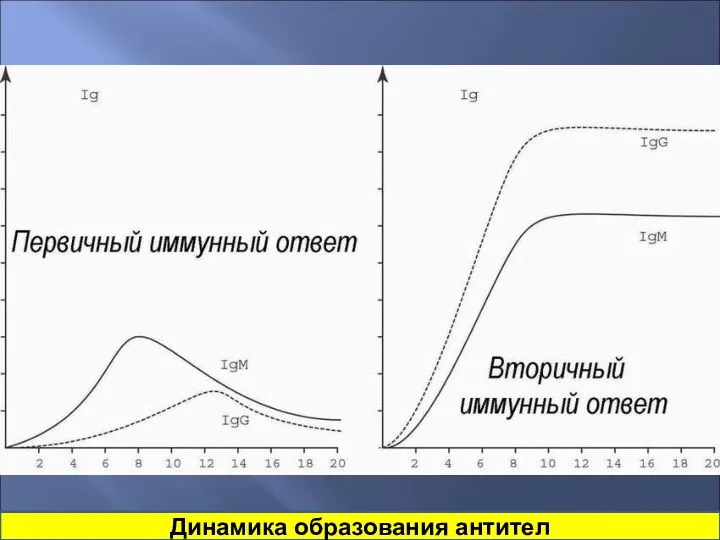
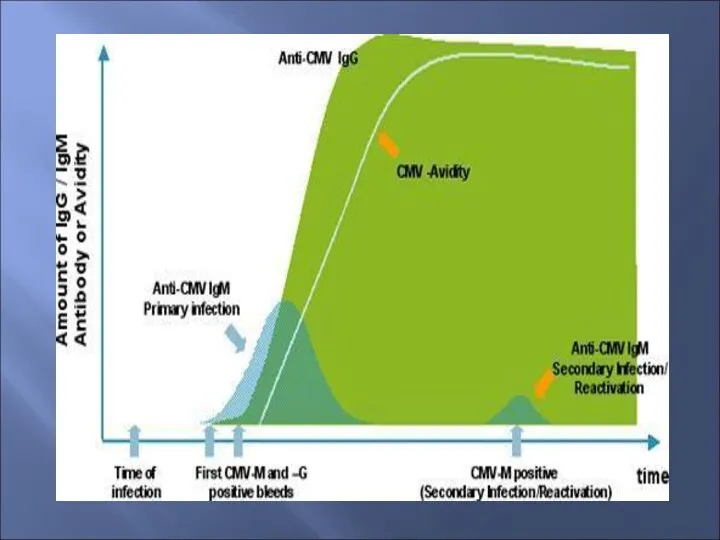
- 45. Динамика образования антител
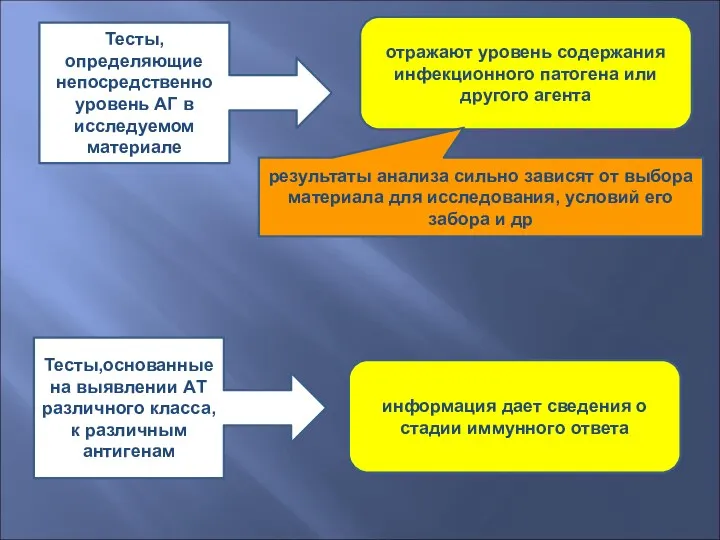
- 46. Тесты, определяющие непосредственно уровень АГ в исследуемом материале отражают уровень содержания инфекционного патогена или другого агента
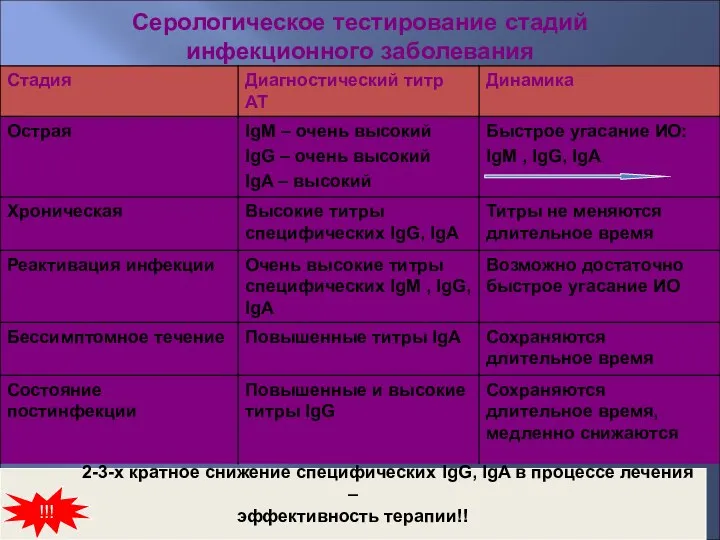
- 48. Серологическое тестирование стадий инфекционного заболевания 2-3-х кратное снижение специфических IgG, IgA в процессе лечения – эффективность
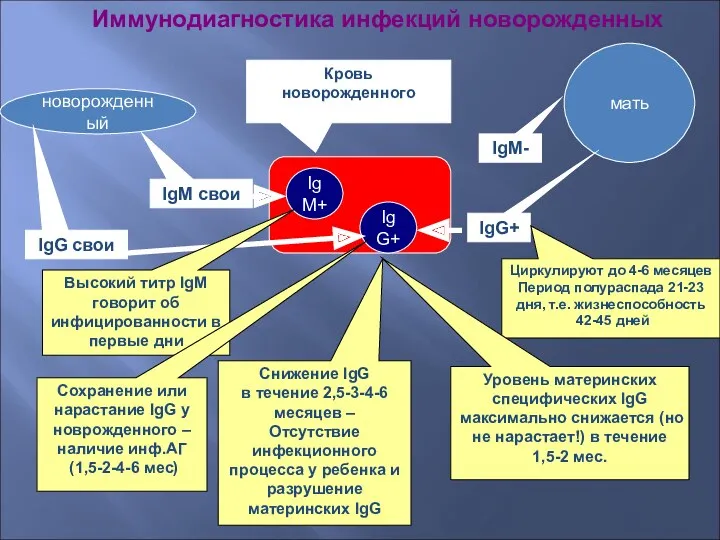
- 49. Иммунодиагностика инфекций новорожденных IgM+ IgG+ Кровь новорожденного новорожденный мать IgM- IgG+ Циркулируют до 4-6 месяцев Период
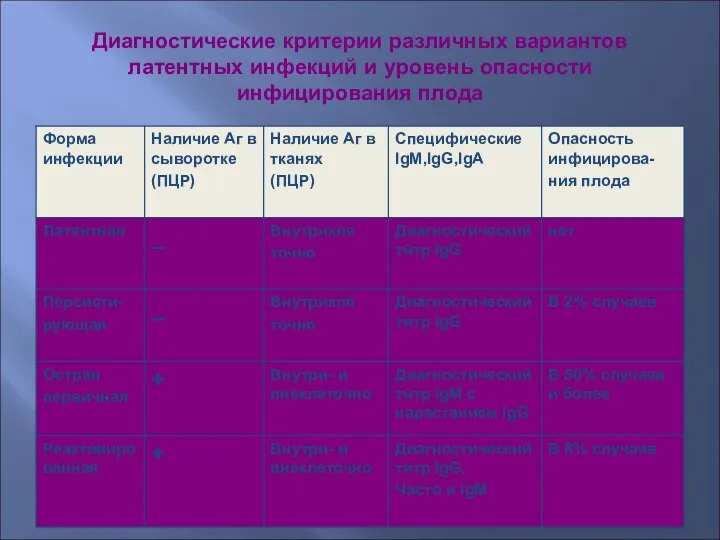
- 50. Диагностические критерии различных вариантов латентных инфекций и уровень опасности инфицирования плода
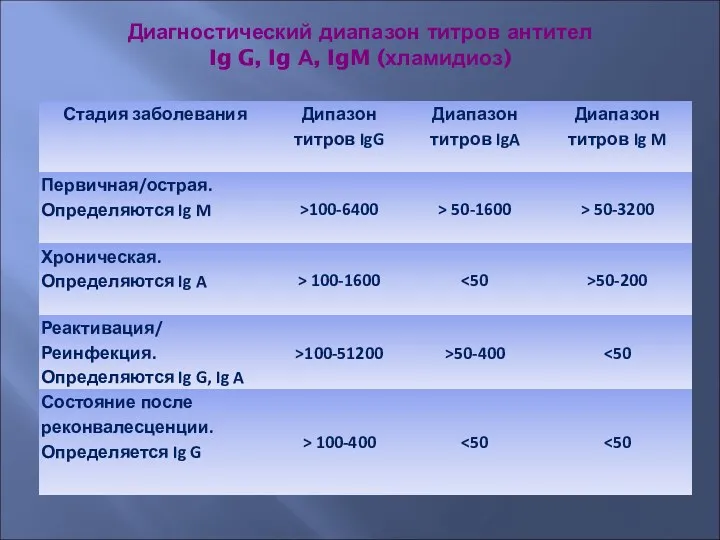
- 51. Диагностический диапазон титров антител Ig G, Ig А, IgM (хламидиоз)
- 52. Очень ранняя стадия инфекции (сомнительно). “Пограничные титры” в первой сыворотке Острая первичная инфекция. “Диагностические титры” во
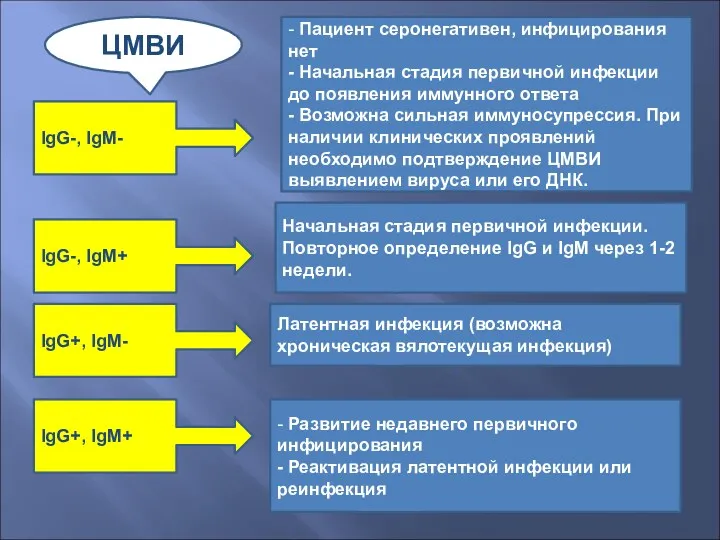
- 53. IgG-, IgM- - Пациент серонегативен, инфицирования нет - Начальная стадия первичной инфекции до появления иммунного ответа
- 54. Клинико-эпидемиологическое значение маркеров вируса гепатита A
- 55. Клинико-эпидемиологическое значение маркеров вируса гепатита В
- 56. Клинико-эпидемиологическое значение маркеров вируса гепатита С и Д
- 57. Традиционные серологические методы имеют ряд ограничений: Часто невозможно дифференцировать первичную инфекцию, реинфекцию, обострение (нетипичная динамика антителогенеза
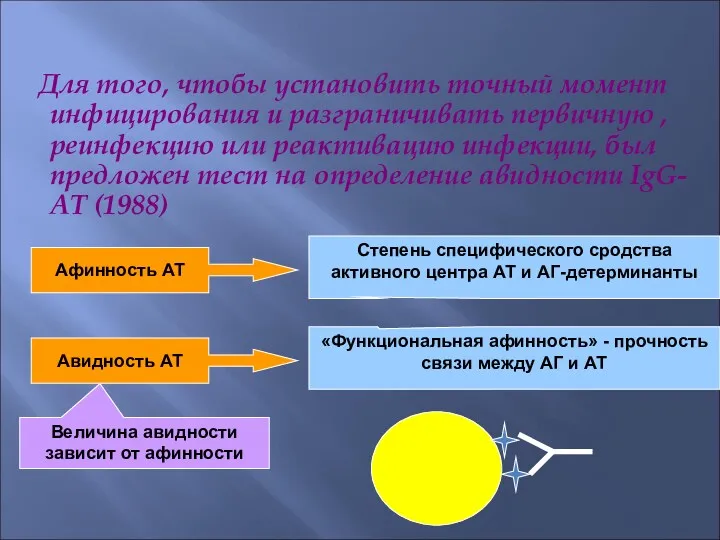
- 58. Для того, чтобы установить точный момент инфицирования и разграничивать первичную , реинфекцию или реактивацию инфекции, был
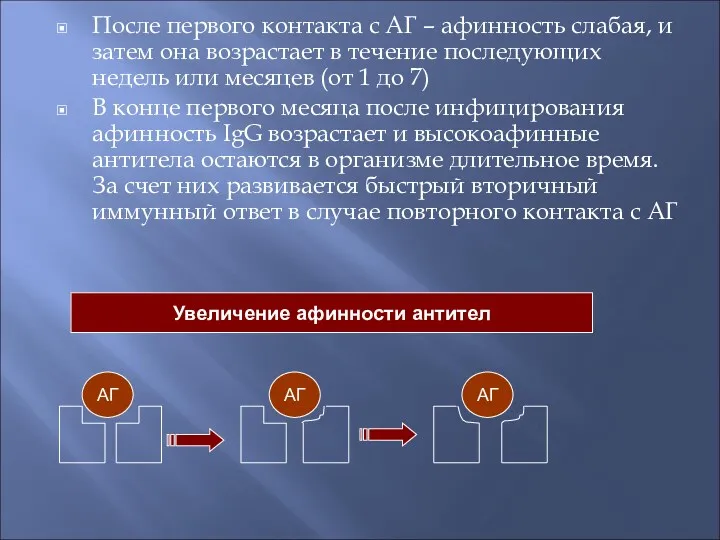
- 59. После первого контакта с АГ – афинность слабая, и затем она возрастает в течение последующих недель
- 60. Низкие дозы Аг приводят к быстрому возрастанию авидности, а высокие – к более медленному Т.о. низкоавидные
- 61. Методы оценки авидности IgG-антител Метод агглюцинации РИА РСК ИФА Электроблотинг электрофорез
- 62. Метод ИФА для определения авидности антител Инкубация сыворотки крови с адсорбированными на планшете Аг – образование
- 63. Интерпретация результатов Авидность ниже 30-50% - свежая первичная инфекция Авидность выше 50% - наличие в сыворотке
- 64. Антибиотики – незаменимые средства, спасшие миллионы жизней ЗАЩИТА ОТ ИНФЕКЦИИ Врожденный и адаптивный иммунитет
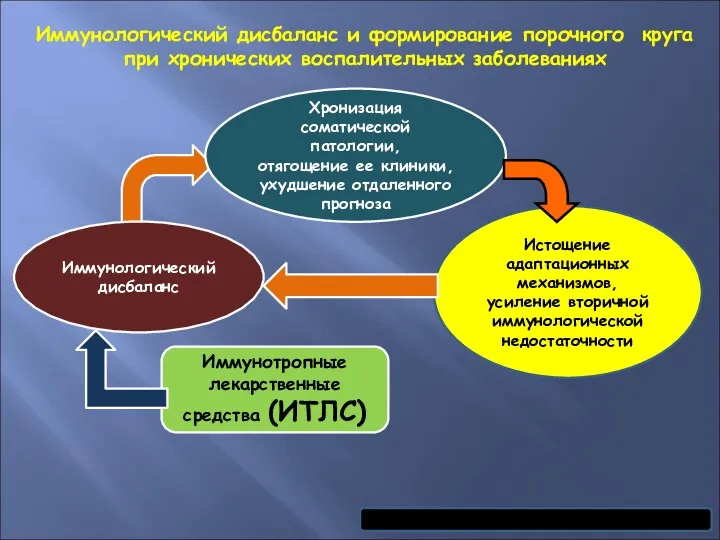
- 65. Иммунологический дисбаланс и формирование порочного круга при хронических воспалительных заболеваниях Иммунологический дисбаланс Хронизация соматической патологии, отягощение
- 66. В отличие от адаптивной иммунной системы, тонко настраиваемой на каждый проникший в организм антиген, система врожденного
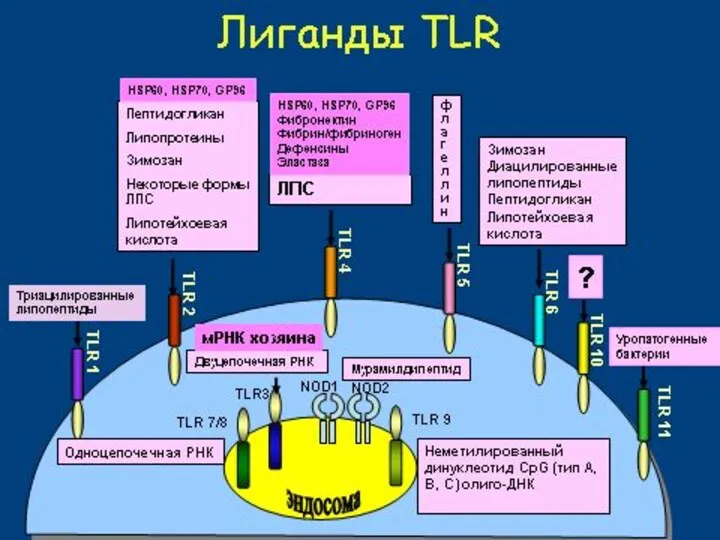
- 67. Рецепторы врожденного иммунитета Рецепторы-мусорщики (scavenger-рецепторы) Маннозные Рецепторы к комплементу (CR1, CR3,CR4) Лектиновые Паттерн-распознающие (PRR) Toll-подобные (TLR)
- 68. РЕГУЛЯЦИЯ ИММУНИТЕТА ЧЕРЕЗ PRR РАМР enPRR Фагоцитоз и лизис Презентация антигена Адаптивный иммунный ответ РАМР sPRR
- 69. Treating Infectious Diseases in a Microbial World: Immunomodulation National Academy of Sciences, USA ISBN: 0-309-65490-4, 103
- 71. Скачать презентацию













































 Иммунитеттің Т және В-жүйесін бағалаудың зертханалық әдістері
Иммунитеттің Т және В-жүйесін бағалаудың зертханалық әдістері Болезни, поражающие все части глаза
Болезни, поражающие все части глаза Государственное учреждение здравоохранения Детская инфекционная больница № 2 г. Тулы
Государственное учреждение здравоохранения Детская инфекционная больница № 2 г. Тулы Эмоциональді лабильдік(астениялық) бұзылыстардың(F06.6), жеңіл депрессивті эпизодтың(F32.0), адаптация бұзылыстарының (F43.2
Эмоциональді лабильдік(астениялық) бұзылыстардың(F06.6), жеңіл депрессивті эпизодтың(F32.0), адаптация бұзылыстарының (F43.2 Анализ государственной поддержки СО НКО, занимающихся профилактикой ВИЧ-инфекции
Анализ государственной поддержки СО НКО, занимающихся профилактикой ВИЧ-инфекции Классификация детей с нарушениями зрения
Классификация детей с нарушениями зрения Методы самоконтроля за функциональным состоянием организма
Методы самоконтроля за функциональным состоянием организма Нормальный менструальный цикл и его регуляция
Нормальный менструальный цикл и его регуляция Проблемы боли в детской стоматологии и психологические принципы ее решения
Проблемы боли в детской стоматологии и психологические принципы ее решения Лекарственные препараты, действующие на афферентную нервную систему
Лекарственные препараты, действующие на афферентную нервную систему Нутритивная поддержка у больных с черепно-мозговой травмой
Нутритивная поддержка у больных с черепно-мозговой травмой Патология сердечно-сосудистой системы при гипотиреозе
Патология сердечно-сосудистой системы при гипотиреозе Денсаулық-2020 бағдарламасы
Денсаулық-2020 бағдарламасы Продукты питания и витамины, необходимые для профилактики рахита
Продукты питания и витамины, необходимые для профилактики рахита Неотложные состояния в неврологии на до госпитальном этапе
Неотложные состояния в неврологии на до госпитальном этапе Көз қызметінің бұзылуы және гигиенасы
Көз қызметінің бұзылуы және гигиенасы Одышка. Распространенность одышки
Одышка. Распространенность одышки Аппаратный массаж
Аппаратный массаж Оказание первой помощи при ушибах, вывихах суставов и переломах костей
Оказание первой помощи при ушибах, вывихах суставов и переломах костей Формулярлық жүйенің рөлі. Дәрілік формулярды құрастыру. Қазақстандық ұлттық формулярдың рөлі
Формулярлық жүйенің рөлі. Дәрілік формулярды құрастыру. Қазақстандық ұлттық формулярдың рөлі Инфекция костей и суставов
Инфекция костей и суставов Эндокардит. Миокардит. Перикардит. Инфаркт миокарда
Эндокардит. Миокардит. Перикардит. Инфаркт миокарда Синдромы поражения височной доли
Синдромы поражения височной доли Броксинак: показания к применению
Броксинак: показания к применению Беременность и артериальная гипотония
Беременность и артериальная гипотония Макропрепараты к экзамену
Макропрепараты к экзамену Балалардағы ас қорыту жүйесінің бұзылу семиотикасы мен синдромдары. Балалардағы ас қорыту жүйесінің зерттеудің қосымша әдістері
Балалардағы ас қорыту жүйесінің бұзылу семиотикасы мен синдромдары. Балалардағы ас қорыту жүйесінің зерттеудің қосымша әдістері Нейробластома. Определения понятия
Нейробластома. Определения понятия