Содержание
- 2. Применение ферментов в медицине
- 3. Изоферменты фермент, существующий в виде нескольких изоформ ферменты из одного источника катализируют одну и ту же
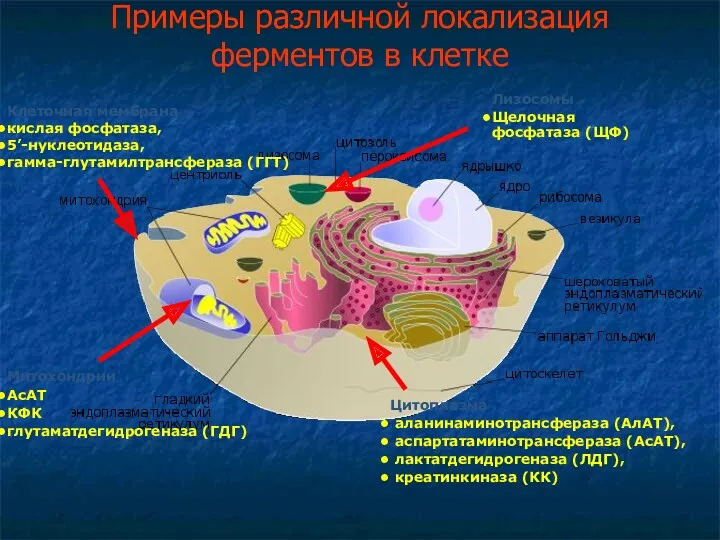
- 4. Примеры различной локализация ферментов в клетке Клеточная мембрана кислая фосфатаза, 5’-нуклеотидаза, гамма-глутамилтрансфераза (ГГТ) Цитоплазма аланинаминотрансфераза (АлАТ),
- 5. ЕДИНИЦЫ АКТИВНОСТИ ФЕРМЕНТОВ За международную единицу активности принимается количество фермента, способного превратить один микромоль (мкмоль) субстрата
- 6. катал (символ – кат.), что являет собой количество фермента, способное осуществить превращение 1 моля субстрата за
- 7. Принципы энзимодиагностики 1. Состав ферментов и их тканевое деление постоянны и могут изменяться при разных патологических
- 8. Ферменты сыворотки Клеточные поступают в кровь из органов и тканей. Уровень их сывороточной активности зависит от
- 9. Причины повышения активности клеточных ферментов в крови нарушение проницаемости мембраны клеток (при воспалительных процессах) нарушение целостности
- 10. Основные ферменты, которые исследуются в лабораториях аспартатаминотрансфераза (AcAT) аланинаминотрансфераза (АЛАТ) глутаматдегидрогеназа (ГЛД) лактатдегидрогеназа (ЛДГ) креатинкиназа (КК)
- 11. Аминотрансферазы играют важную роль в азотистом обмене, принимают участие в расщеплении аминокислот, которые не используются в
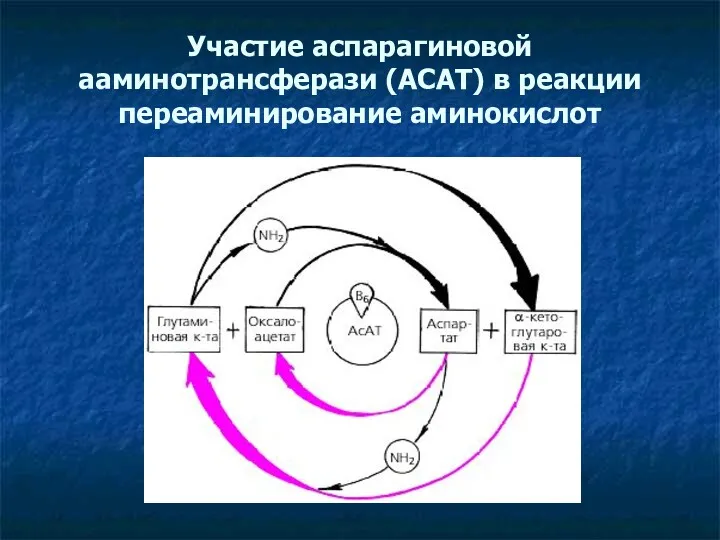
- 12. Участие аспарагиновой ааминотрансферази (АСАТ) в реакции переаминирование аминокислот
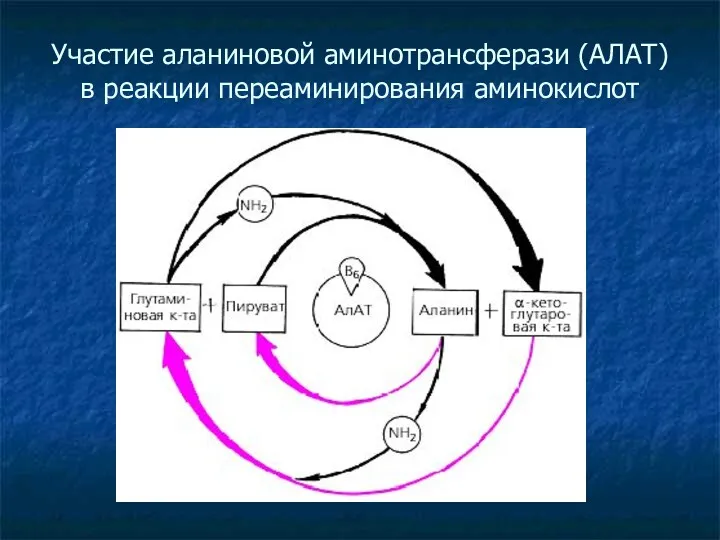
- 13. Участие аланиновой аминотрансферази (АЛАТ) в реакции переаминирования аминокислот
- 14. Аспартатаминотрансфераза (АСАТ) [КФ 2.6.1.1]. N 0,1-0,45 ммоль/(час/л) Основные источники: сердечная мышца, печень, скелетная мускулатура, головной мозг,
- 15. Аланинаминотрансфераза (АЛАТ) [КФ 2.6.1.2.]. N 0,1-0,68 ммоль/(час*л) Основные источники: печень, поджелудочная железа, сердце, скелетная мускулатура, почки.
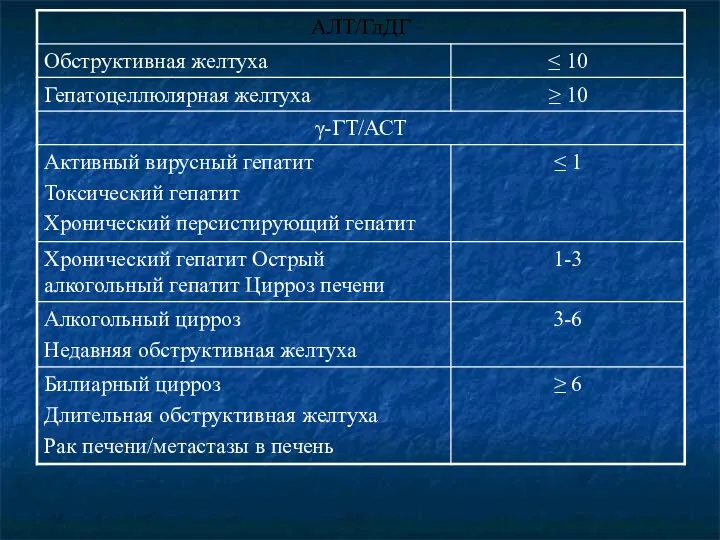
- 16. 1. При остром ИМ активность АСАТ более высока, чем АЛАТ (коэффициент де-Ритиса больше 1,3). 2. При
- 17. Фосфатазы - ферменты, которые катализируют отщепление фосфорной кислоты от органических соединений. Фосфатазы разделяют на фосфодиэстеразы I
- 18. Щелочная фосфатаза (ЩФ) [КФ 3.1.3.1.] N 0,5-1,3 ммоль/(час* л). Действие: фермент, который гидролизует эфиры ортофосфорной кислоты
- 19. Y-Глутамилтранспептидаза (ГГТП) КФ [2.3.2.2] N мужчины: 250-1767 нмоль/(с*л) или 15-106 МО, женщины: 167-1100 нмоль/(с*л) или 10-66
- 20. Креатинкиназа (КК) КФ [2.7.3.2] N 0,152-0,305 ммоль/(час*л) Основные источники: миокард, скелетные мышцы, язык, селезенка, диафрагма, почки,
- 21. Клиническое значение определения КК Физиологическое повышение активности креатинкиназы (КК) обнаружено в сыворотке крови: у новорожденных (небольшое),
- 22. Лактатдегидрогеназа (ЛДГ) КФ [1.1.1.27] N 220-1100 нмоль/(с*л) или 0,8-4,0мкмоль/(час*мл) Действие: обратное превращение лактата в пируват. Основные
- 25. Энзимотерапия Как элемент комплексной терапии - применение ферментов в сочетании с другой терапией. В качестве дополнительных
- 26. Применение ферментов в качестве специфических реактивов специфические эндонуклеазы, катализирующие разрывы межнуклеотидных связей ДНК, для диагностики фенилкетонурии,
- 28. Скачать презентацию








![Аспартатаминотрансфераза (АСАТ) [КФ 2.6.1.1]. N 0,1-0,45 ммоль/(час/л) Основные источники: сердечная](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/270623/slide-13.jpg)
![Аланинаминотрансфераза (АЛАТ) [КФ 2.6.1.2.]. N 0,1-0,68 ммоль/(час*л) Основные источники: печень,](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/270623/slide-14.jpg)


![Щелочная фосфатаза (ЩФ) [КФ 3.1.3.1.] N 0,5-1,3 ммоль/(час* л). Действие:](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/270623/slide-17.jpg)
![Y-Глутамилтранспептидаза (ГГТП) КФ [2.3.2.2] N мужчины: 250-1767 нмоль/(с*л) или 15-106](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/270623/slide-18.jpg)
![Креатинкиназа (КК) КФ [2.7.3.2] N 0,152-0,305 ммоль/(час*л) Основные источники: миокард,](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/270623/slide-19.jpg)

![Лактатдегидрогеназа (ЛДГ) КФ [1.1.1.27] N 220-1100 нмоль/(с*л) или 0,8-4,0мкмоль/(час*мл) Действие:](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/270623/slide-21.jpg)



 Иммунитеттің Т және В-жүйесін бағалаудың зертханалық әдістері
Иммунитеттің Т және В-жүйесін бағалаудың зертханалық әдістері Болезни, поражающие все части глаза
Болезни, поражающие все части глаза Государственное учреждение здравоохранения Детская инфекционная больница № 2 г. Тулы
Государственное учреждение здравоохранения Детская инфекционная больница № 2 г. Тулы Эмоциональді лабильдік(астениялық) бұзылыстардың(F06.6), жеңіл депрессивті эпизодтың(F32.0), адаптация бұзылыстарының (F43.2
Эмоциональді лабильдік(астениялық) бұзылыстардың(F06.6), жеңіл депрессивті эпизодтың(F32.0), адаптация бұзылыстарының (F43.2 Анализ государственной поддержки СО НКО, занимающихся профилактикой ВИЧ-инфекции
Анализ государственной поддержки СО НКО, занимающихся профилактикой ВИЧ-инфекции Классификация детей с нарушениями зрения
Классификация детей с нарушениями зрения Методы самоконтроля за функциональным состоянием организма
Методы самоконтроля за функциональным состоянием организма Нормальный менструальный цикл и его регуляция
Нормальный менструальный цикл и его регуляция Проблемы боли в детской стоматологии и психологические принципы ее решения
Проблемы боли в детской стоматологии и психологические принципы ее решения Лекарственные препараты, действующие на афферентную нервную систему
Лекарственные препараты, действующие на афферентную нервную систему Нутритивная поддержка у больных с черепно-мозговой травмой
Нутритивная поддержка у больных с черепно-мозговой травмой Патология сердечно-сосудистой системы при гипотиреозе
Патология сердечно-сосудистой системы при гипотиреозе Денсаулық-2020 бағдарламасы
Денсаулық-2020 бағдарламасы Продукты питания и витамины, необходимые для профилактики рахита
Продукты питания и витамины, необходимые для профилактики рахита Неотложные состояния в неврологии на до госпитальном этапе
Неотложные состояния в неврологии на до госпитальном этапе Көз қызметінің бұзылуы және гигиенасы
Көз қызметінің бұзылуы және гигиенасы Одышка. Распространенность одышки
Одышка. Распространенность одышки Аппаратный массаж
Аппаратный массаж Оказание первой помощи при ушибах, вывихах суставов и переломах костей
Оказание первой помощи при ушибах, вывихах суставов и переломах костей Формулярлық жүйенің рөлі. Дәрілік формулярды құрастыру. Қазақстандық ұлттық формулярдың рөлі
Формулярлық жүйенің рөлі. Дәрілік формулярды құрастыру. Қазақстандық ұлттық формулярдың рөлі Инфекция костей и суставов
Инфекция костей и суставов Эндокардит. Миокардит. Перикардит. Инфаркт миокарда
Эндокардит. Миокардит. Перикардит. Инфаркт миокарда Синдромы поражения височной доли
Синдромы поражения височной доли Броксинак: показания к применению
Броксинак: показания к применению Беременность и артериальная гипотония
Беременность и артериальная гипотония Макропрепараты к экзамену
Макропрепараты к экзамену Балалардағы ас қорыту жүйесінің бұзылу семиотикасы мен синдромдары. Балалардағы ас қорыту жүйесінің зерттеудің қосымша әдістері
Балалардағы ас қорыту жүйесінің бұзылу семиотикасы мен синдромдары. Балалардағы ас қорыту жүйесінің зерттеудің қосымша әдістері Нейробластома. Определения понятия
Нейробластома. Определения понятия