Содержание
- 2. Аминокислоты Производные карбоновых кислот, содержащие в своем составе одну или несколько аминогрупп. N H2 – C
- 3. Открытие аминокислот 1806 г Луи Никола Воклен, Пьр Жан Робике из сока спаржи выделили первую аминокислоту-аспарагиновую
- 4. Аминокислоты Природные Их известно около 150 Содержатся в живых организмах 20 из них входят в состав
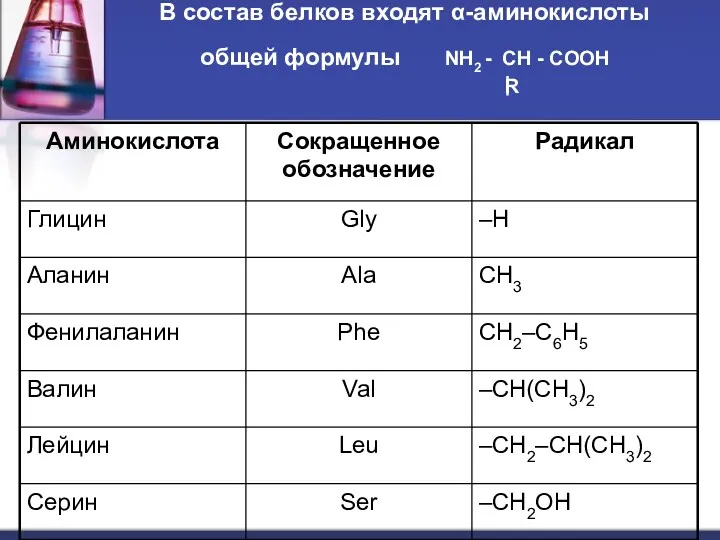
- 5. В состав белков входят α-аминокислоты общей формулы NH2 - CH - COOH R
- 6. Номенклатура По систематической номенклатуре названия аминокислот образуются из названий соответствующих кислот прибавлением приставки амино- и указанием
- 7. Номенклатура Часто используется другой способ построения названий аминокислот, согласно которому к тривиальному названию карбоновой кислоты добавляется
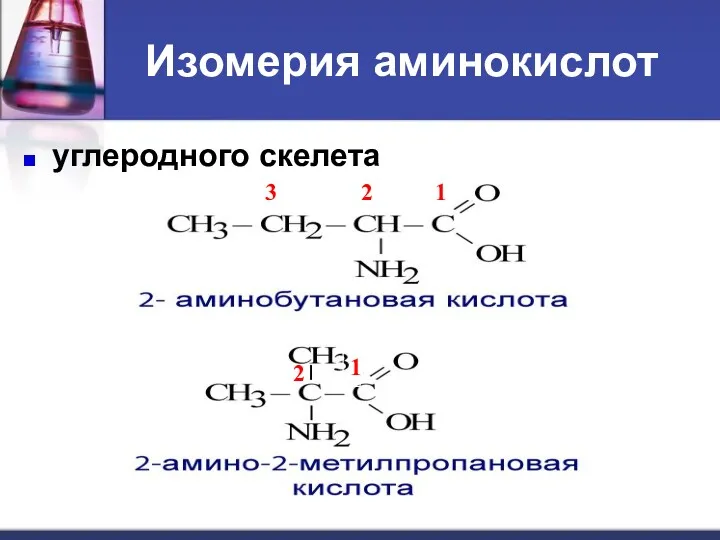
- 8. Изомерия аминокислот углеродного скелета ; положения функциональных групп ; межклассовая (нитросоединения); оптическая.
- 9. Изомерия аминокислот углеродного скелета 1 2 3 1 2
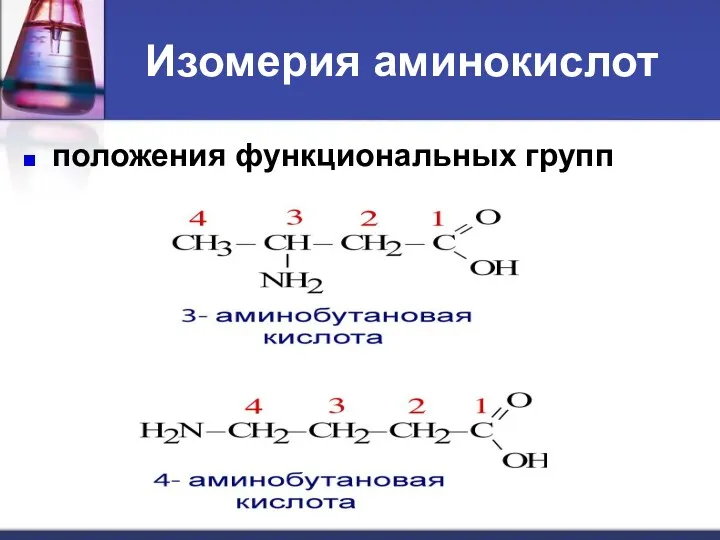
- 10. Изомерия аминокислот положения функциональных групп
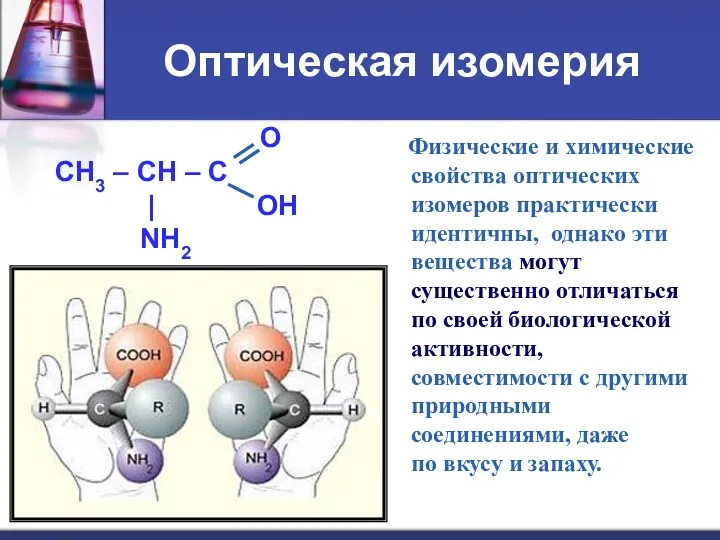
- 11. Оптическая изомерия O CH3 – CH – C | OH NH2 Физические и химические свойства оптических
- 12. Физические свойства Аминокислоты бесцветные; кристаллические; хорошо растворимы в воде, но нерастворимы в эфире; в зависимости от
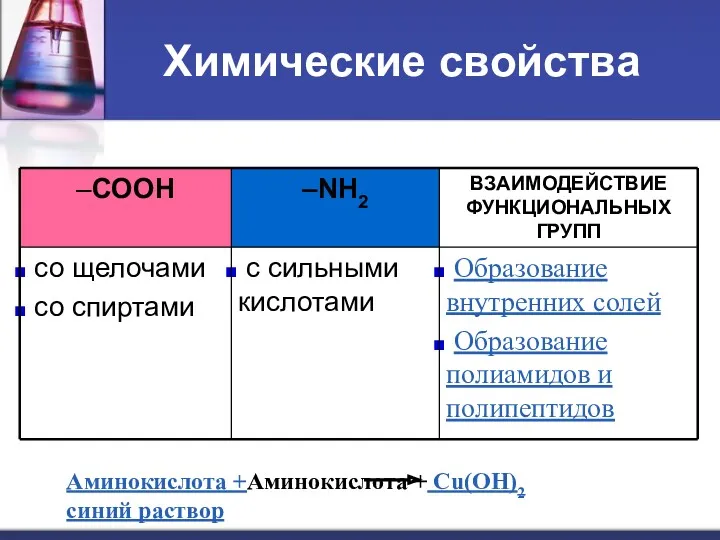
- 13. Химические свойства Наличие амино- и карбоксильной групп определяет двойственность химических свойств аминокислот. Амфотерность (от греч. amphуteros
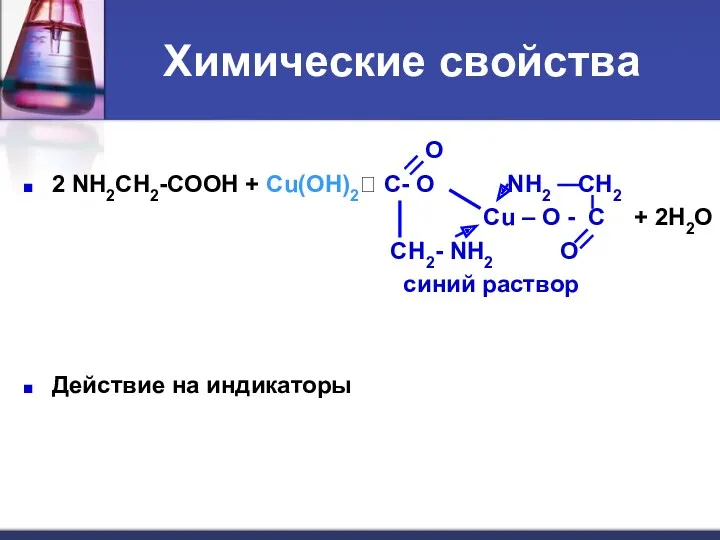
- 14. Химические свойства Аминокислота +Аминокислота + Cu(OH)2 синий раствор
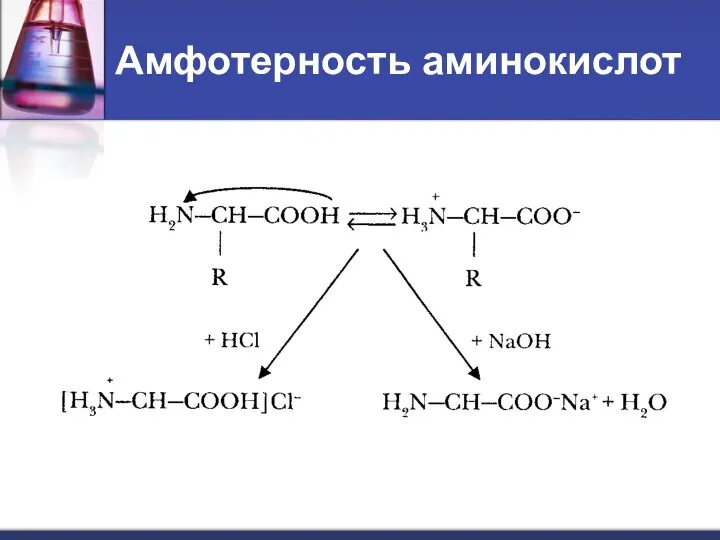
- 15. Амфотерность аминокислот
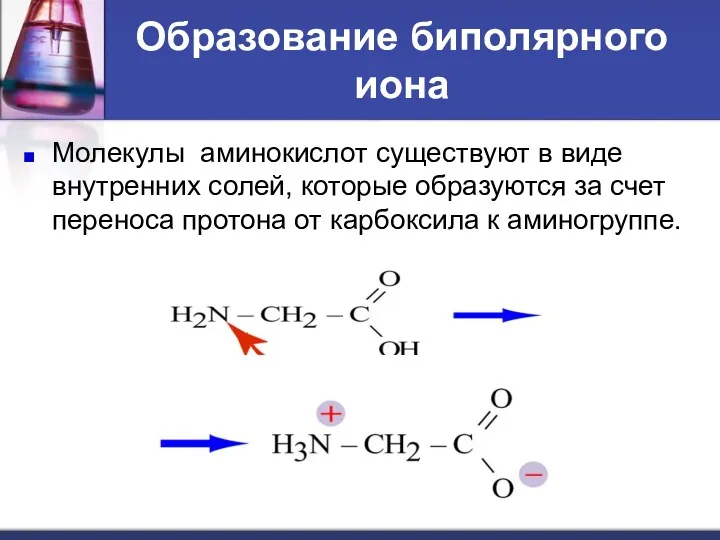
- 16. Образование биполярного иона Молекулы аминокислот существуют в виде внутренних солей, которые образуются за счет переноса протона
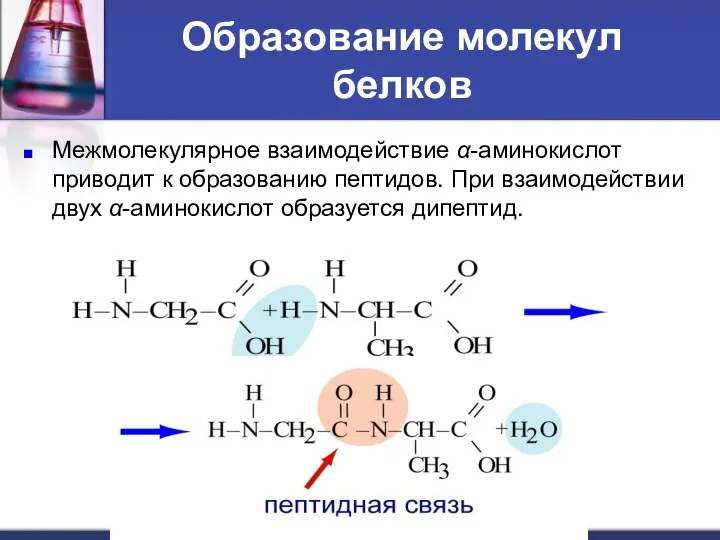
- 17. Образование молекул белков Межмолекулярное взаимодействие α-аминокислот приводит к образованию пептидов. При взаимодействии двух α-аминокислот образуется дипептид.
- 18. Химические свойства O 2 NH2CH2-COOH + Cu(OH)2? C- O NH2 CH2 Cu – O - C
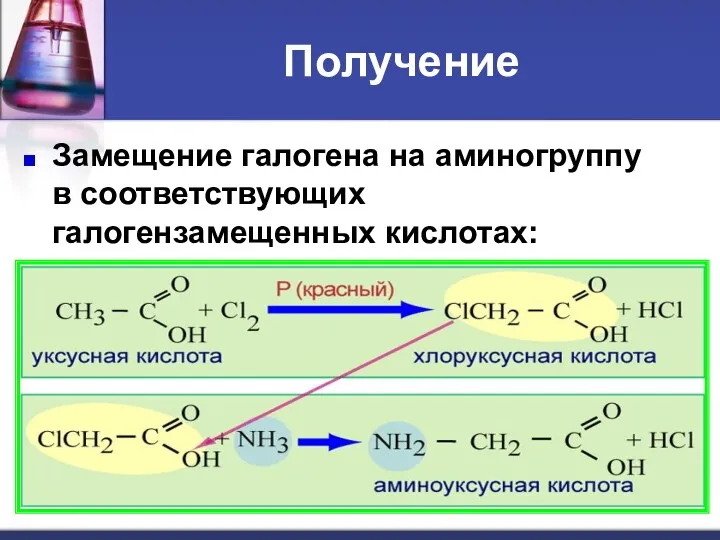
- 19. Получение Замещение галогена на аминогруппу в соответствующих галогензамещенных кислотах:
- 20. Получение аминокислот Присоединение аммиака к α, β-непредельным кислотам с образованием β-аминокислот: CH2=CH–COOH + NH3 H2N–CH2–CH2–COOH Гидролиз
- 21. Применение аминокислот В медицине - лекарственные препараты(глицин) В животноводстве- кормовые добавки (лизин, метионин, треонин) В пищевой
- 22. Аминокислоты - пищевые добавки 1909 г Японский ученый К.Икеда установил, что глутаминовая кислота и ее соли
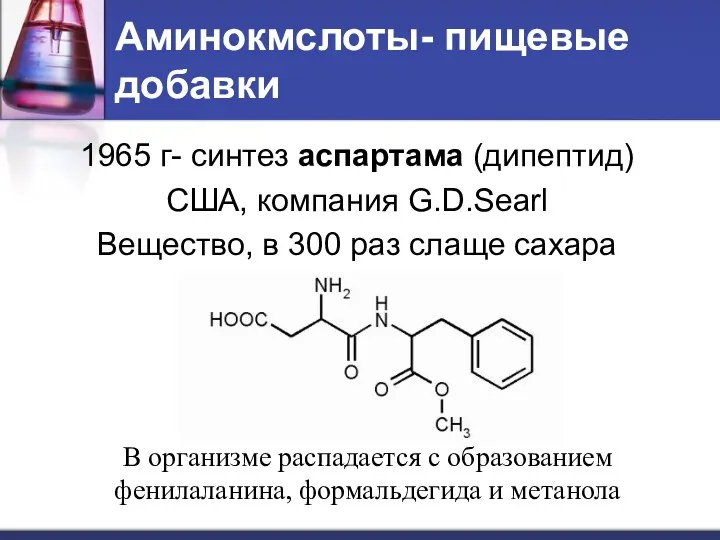
- 23. Аминокмслоты- пищевые добавки 1965 г- синтез аспартама (дипептид) США, компания G.D.Searl Вещество, в 300 раз слаще
- 25. Скачать презентацию











 Информационная система управления грузовыми авиаперевозками
Информационная система управления грузовыми авиаперевозками Врожденные и приобретенные формы поведения
Врожденные и приобретенные формы поведения Вода. Какая она? Тест. Часть 2
Вода. Какая она? Тест. Часть 2 Моё хобби
Моё хобби История обыкновенных дробей
История обыкновенных дробей ОПЕК. Международные товарные соглашения
ОПЕК. Международные товарные соглашения Игра-презентация Дифференциация г-к
Игра-презентация Дифференциация г-к Польша
Польша Сталинградская битва. (17 июля 1942 — 2 февраля 1943)
Сталинградская битва. (17 июля 1942 — 2 февраля 1943) Безопасность школьников в сети интернет
Безопасность школьников в сети интернет Презентация MsPP Дни воинской славы России, часть 1
Презентация MsPP Дни воинской славы России, часть 1 Память. Триггеры и защелки
Память. Триггеры и защелки основное свойство дроби 6 класс
основное свойство дроби 6 класс Презентация Лесостепи и степи России
Презентация Лесостепи и степи России презентация к уроку производственного обучения по профессии Пекарь
презентация к уроку производственного обучения по профессии Пекарь Найди своего героя
Найди своего героя Пьеса Жана Батиста Мольера Мещанин во дворянстве
Пьеса Жана Батиста Мольера Мещанин во дворянстве Создание мультимедийной презентации
Создание мультимедийной презентации Лекция 8 проектирование АТК. Системы электропривода конвейеров 2
Лекция 8 проектирование АТК. Системы электропривода конвейеров 2 Млекопитающие
Млекопитающие Су-джок терапия в логопедии
Су-джок терапия в логопедии Иформатика пәнімен кіріктірілген сабатар жуйесі
Иформатика пәнімен кіріктірілген сабатар жуйесі Выпуклый анализ. Теория двойственности. Лекция 27
Выпуклый анализ. Теория двойственности. Лекция 27 Делимость чисел. Правила
Делимость чисел. Правила Шаблон для презентации
Шаблон для презентации Hip Hura. Creative presentation template
Hip Hura. Creative presentation template Сеть фитнес клубов My Fit
Сеть фитнес клубов My Fit Педагогическая теория Константина Дмитриевича Ушинского (1824—1870)
Педагогическая теория Константина Дмитриевича Ушинского (1824—1870)