Содержание
- 2. Жизнь – есть способ существования белковых тел. Ф. Энгельс
- 3. Белки, являясь основой всех проявлений материальной жизни, выполняют в организме ряд важнейших функций: Пластическая Каталитическая Сократительная
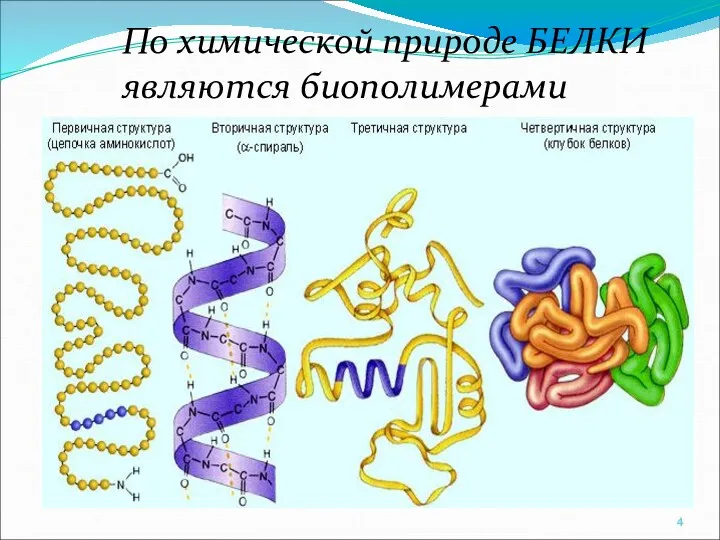
- 4. По химической природе БЕЛКИ являются биополимерами
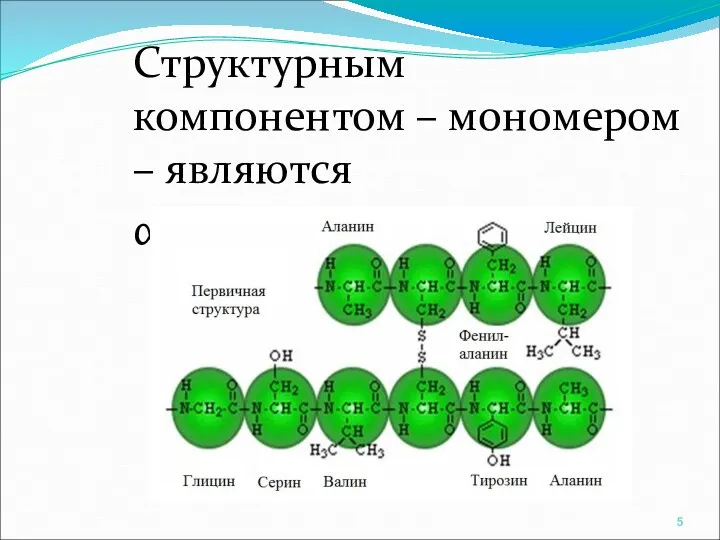
- 5. Структурным компонентом – мономером – являются α-АМК
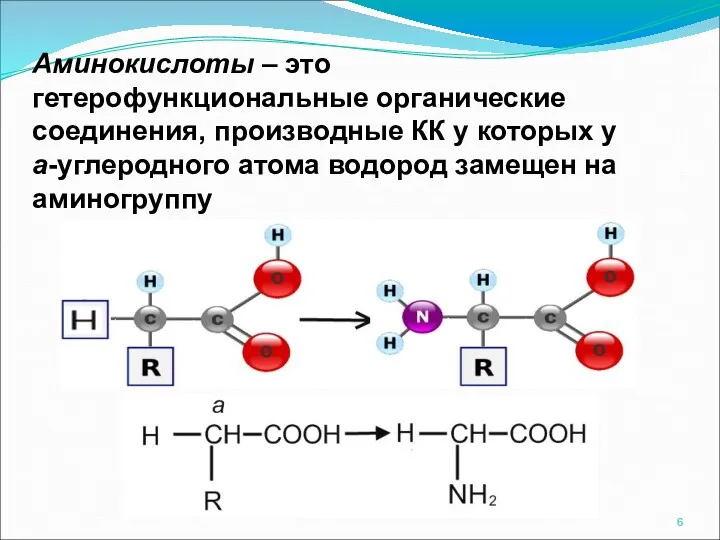
- 6. Аминокислоты – это гетерофункциональные органические соединения, производные КК у которых у a-углеродного атома водород замещен на
- 7. Все a-АМК имеют общую группу и отличаются друг от друга строением радикала
- 8. В состав белков животного и растительного происхождения входит: 19 АМК, 2 амида АМК 2 иминокислоты.
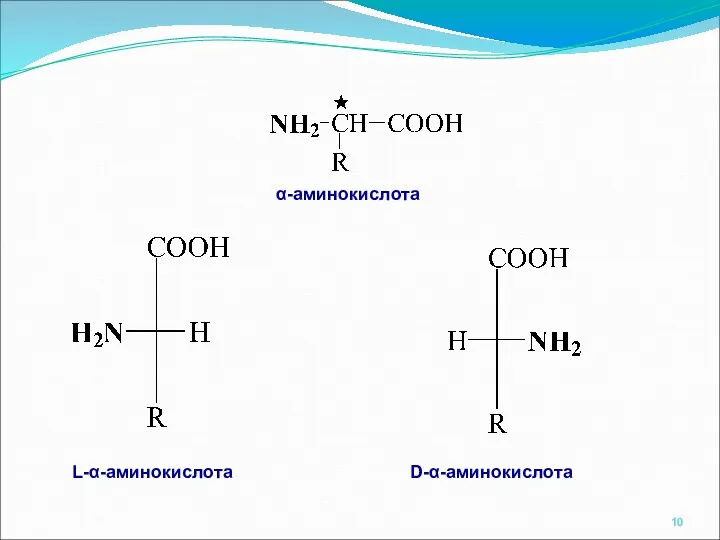
- 9. Во всех природных АМК, за исключением глицина, a-С атом ассиметричен и a-АМК обладают оптической активностью. Растворы
- 10. α-аминокислота L-α-аминокислота D-α-аминокислота
- 11. Классификация, строение, номенклатура a-АМК
- 12. I. По химической природе радикала и характеру содержащихся в нем заместителей: АЛИФАТИЧЕСКИЕ ЦИКЛИЧЕСКИЕ
- 13. Алифатические а-АМК в зависимости от количества в их составе аминогрупп и карбоксильных групп подразделяют на: МАМК
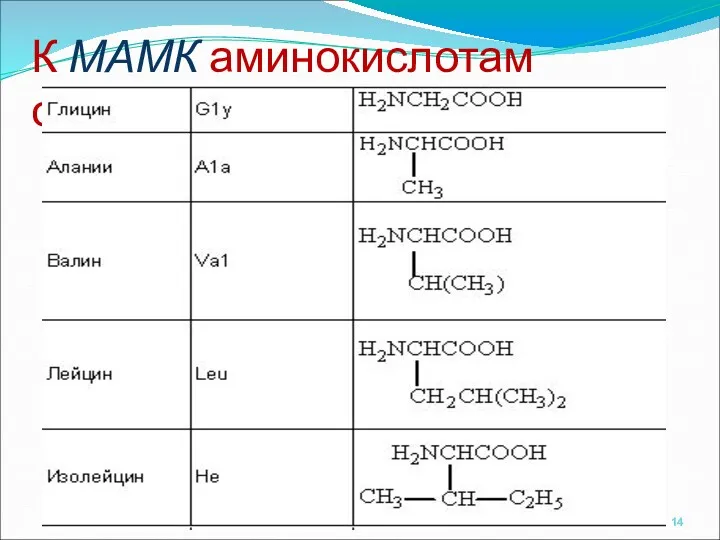
- 14. К МАМК аминокислотам относят:
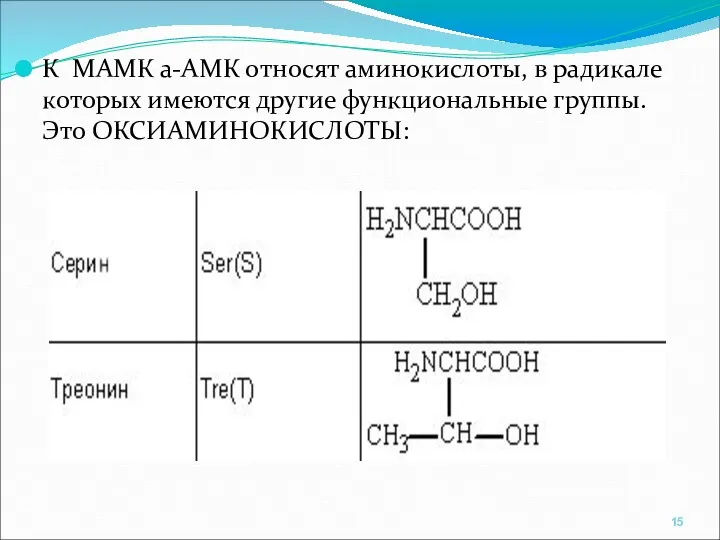
- 15. К МАМК а-АМК относят аминокислоты, в радикале которых имеются другие функциональные группы. Это ОКСИАМИНОКИСЛОТЫ:
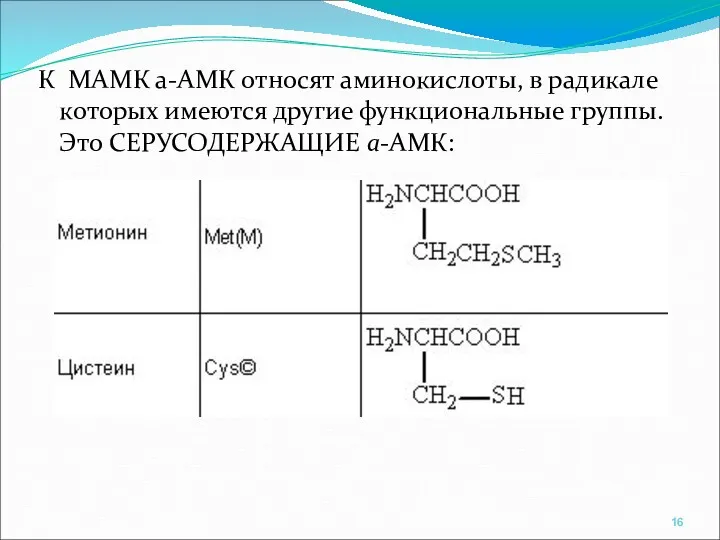
- 16. К МАМК а-АМК относят аминокислоты, в радикале которых имеются другие функциональные группы. Это СЕРУСОДЕРЖАЩИЕ а-АМК:
- 17. К МАДК аминокислоты представлены:
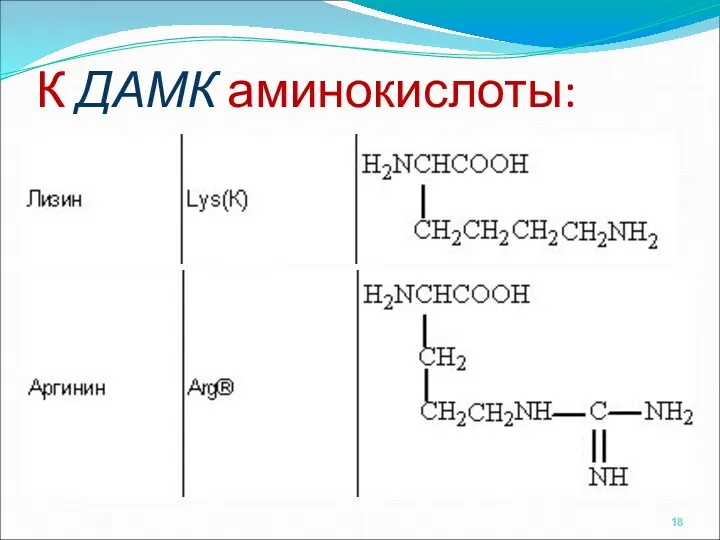
- 18. К ДАМК аминокислоты:
- 19. Циклические аминокислоты в зависимости от природы цикла делятся на: 1. карбоциклические 2. гетероциклические
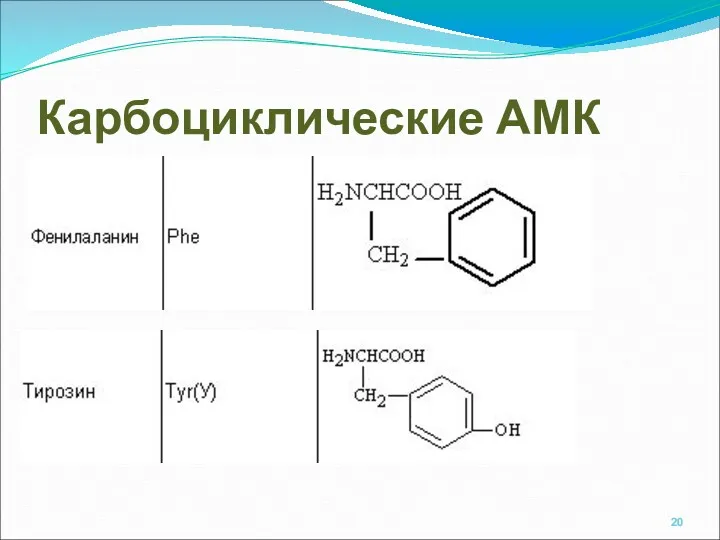
- 20. Карбоциклические АМК
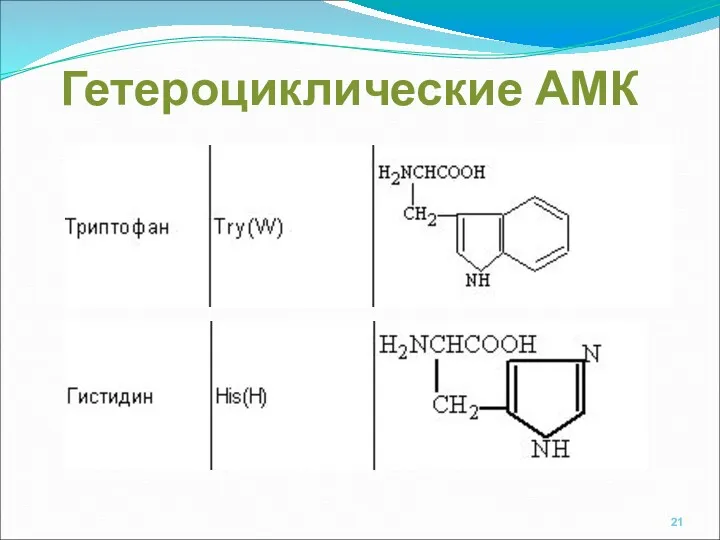
- 21. Гетероциклические АМК
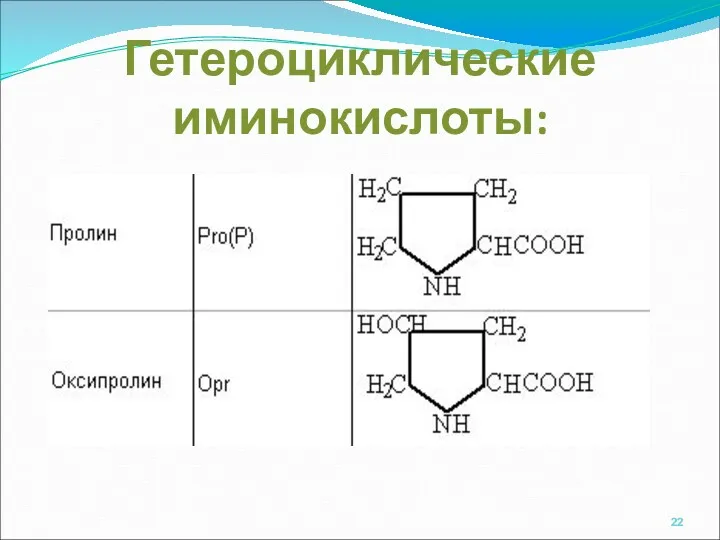
- 22. Гетероциклические иминокислоты:
- 23. II. По полярности радикала: ПОЛЯРНЫЕ НЕПОЛЯРНЫЕ
- 25. К НЕПОЛЯРНЫМ АМК относят аминокислоты не содержащие полярных функциональных групп: глицин, аланин, валин, лейцин, изолейцин, фенилаланин.
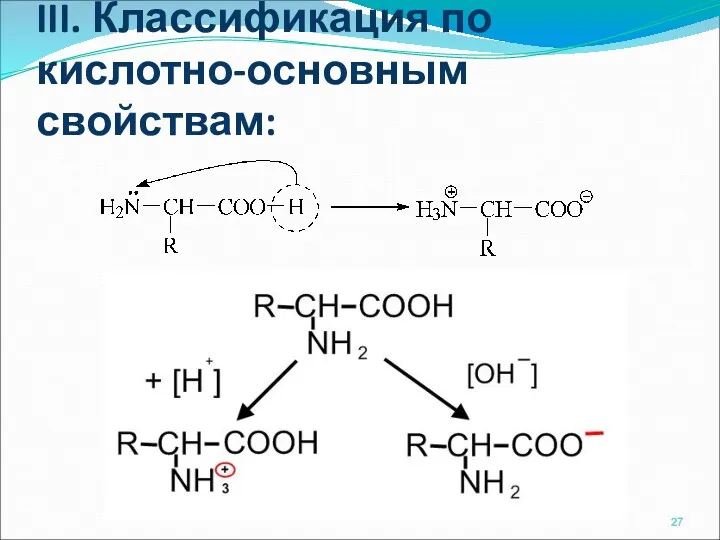
- 27. III. Классификация по кислотно-основным свойствам:
- 28. Значение рН, при котором концентрация дипольных форм АМК максимальна, а концентрация анионных и катионных форм минимальна
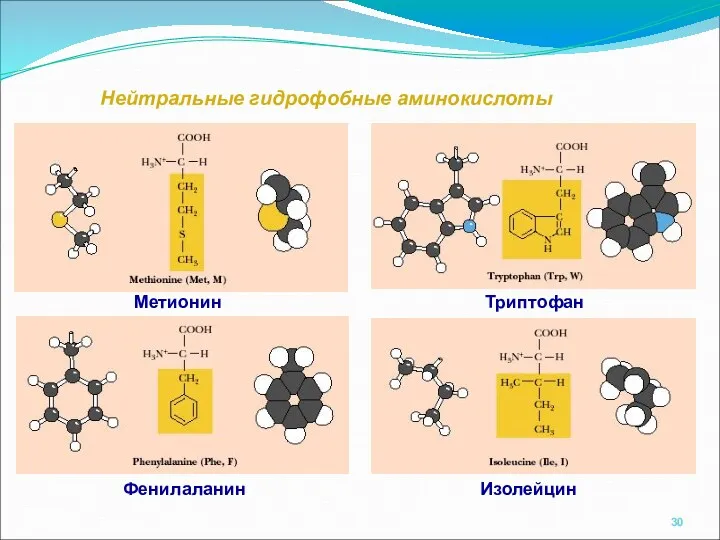
- 30. Нейтральные гидрофобные аминокислоты Изолейцин Фенилаланин Метионин Триптофан
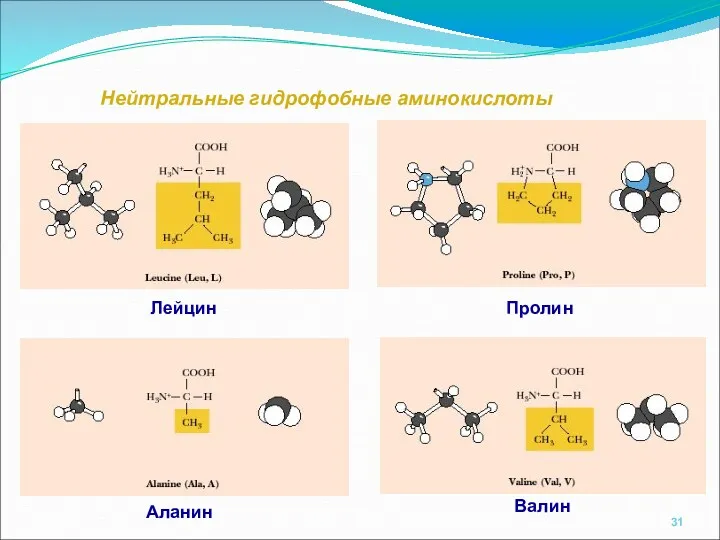
- 31. Нейтральные гидрофобные аминокислоты Аланин Валин Лейцин Пролин
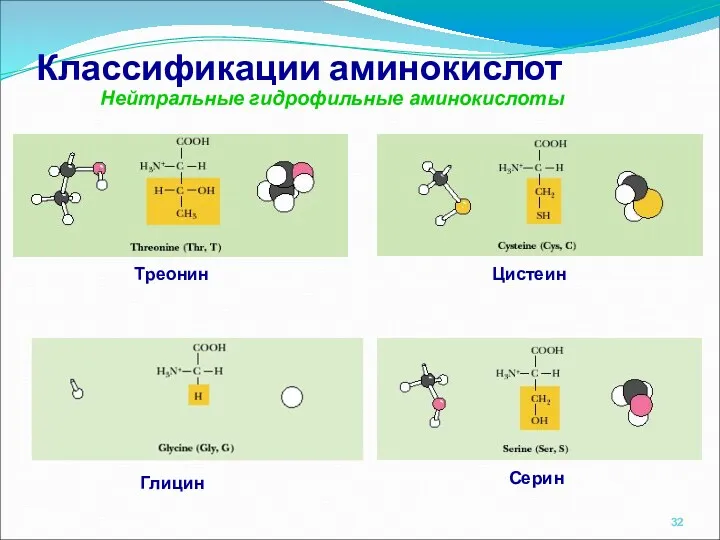
- 32. Классификации аминокислот Нейтральные гидрофильные аминокислоты Глицин Серин Треонин Цистеин
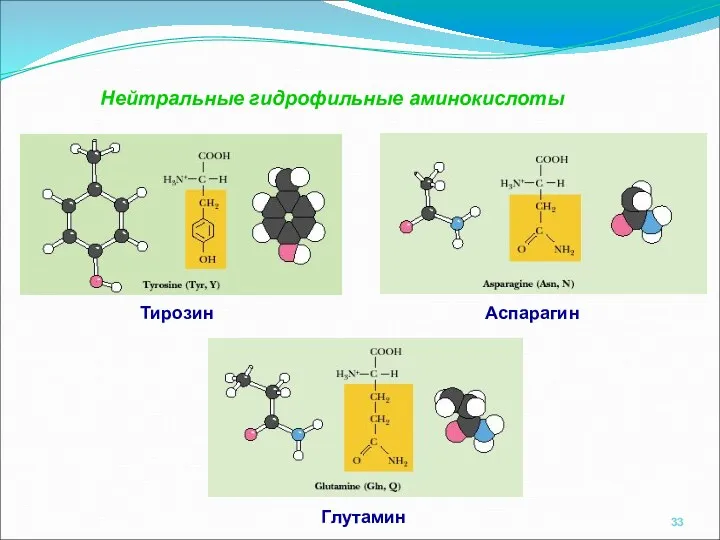
- 33. Нейтральные гидрофильные аминокислоты Тирозин Аспарагин Глутамин
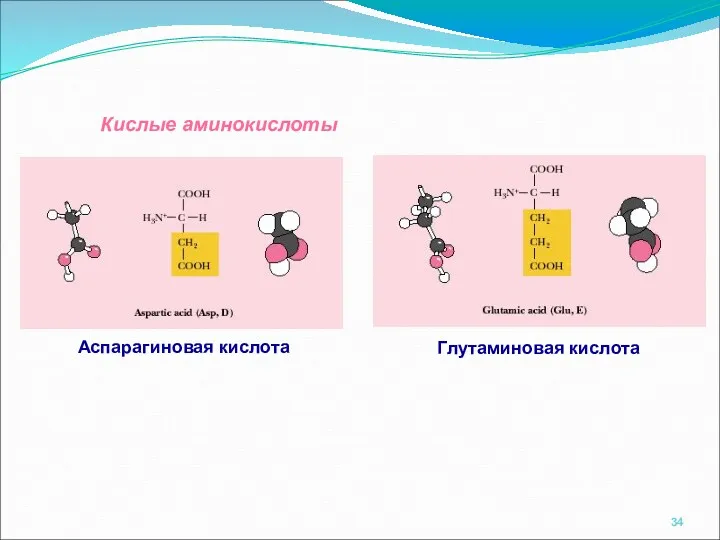
- 34. Кислые аминокислоты Глутаминовая кислота Аспарагиновая кислота
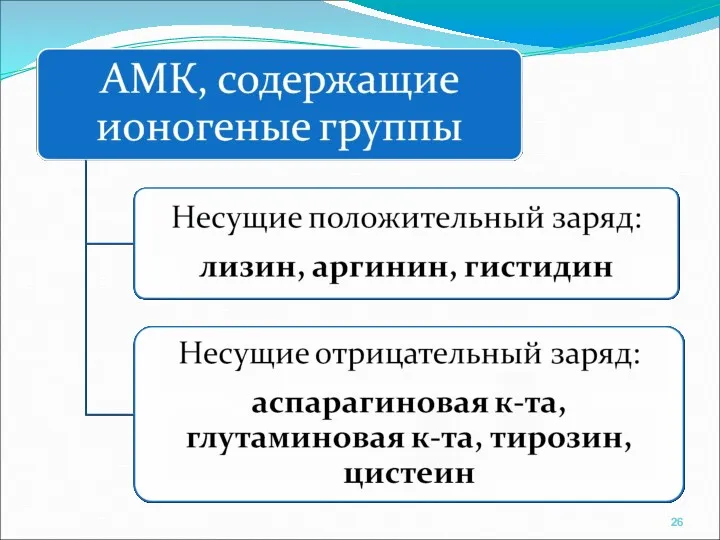
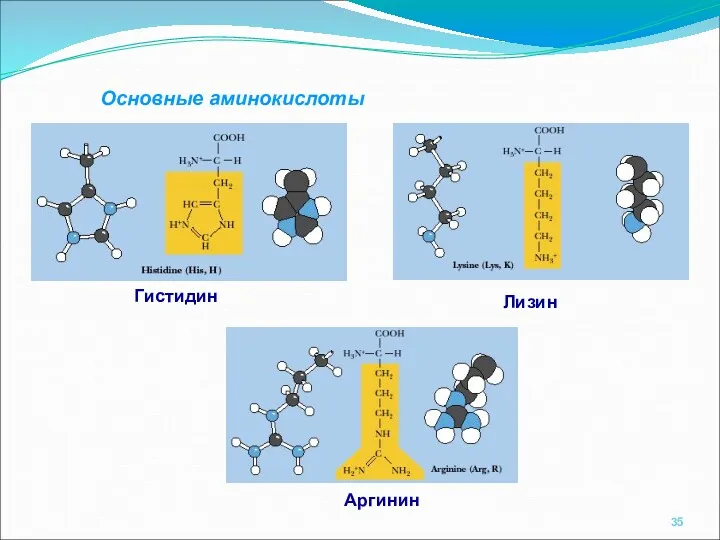
- 35. Основные аминокислоты Лизин Аргинин Гистидин
- 36. III. Классификация АМК по биологическому принципу: ЗАМЕНИМЫЕ НЕЗАМЕНИМЫЕ
- 37. Незаменимые - не синтезируются в организме и должны поступать с пищей: валин, лейцин, изолейцин, треонин, метионин,
- 38. Названия аминокислот произошли в основном от исходных материалов, из которых они были впервые выделены; аспарагин (от
- 39. Другие названия связаны с методами выделения: аргинин (от лат. argentum — серебро) был впервые получен в
- 40. Структурные связи с другими природными соединениями также внесли вклад в названия некоторых аминокислот: валин назван как
- 41. Аминоацильные остатки общей формулы NH2-CHR-CO- называют, добавляя к корню слова окончание –ил (исключение: триптофан и аминодикарбоновые
- 42. Синтез аминокислот Восстановительное аминирование a-кетонокислот Переаминирование или трансаминирование
- 43. Образование аланина из пировиноградной кислоты ПВК АЛАНИН
- 44. Аналогичным образом синтезируется из a-кетоглутаровой кислоты глутаминовая кислота
- 45. Реакции переаминирования Сущность этого процесса заключается в ферментативном переносе аминогруппы с α-аминокислоты на α-кетонокислоту с образованием
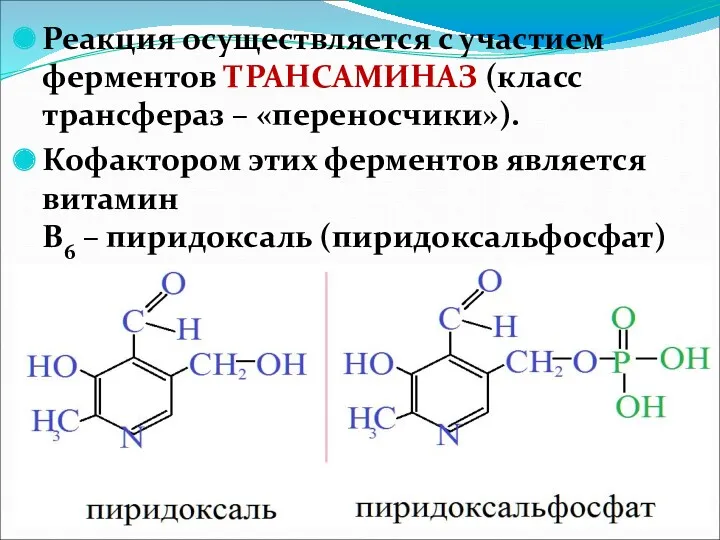
- 48. Реакция осуществляется с участием ферментов ТРАНСАМИНАЗ (класс трансфераз – «переносчики»). Кофактором этих ферментов является витамин В6
- 51. Химические свойства аминокислот
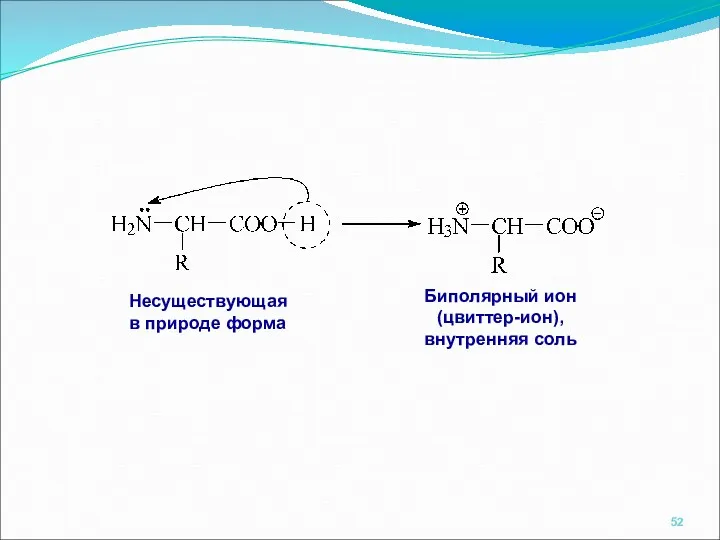
- 52. Несуществующая в природе форма Биполярный ион (цвиттер-ион), внутренняя соль
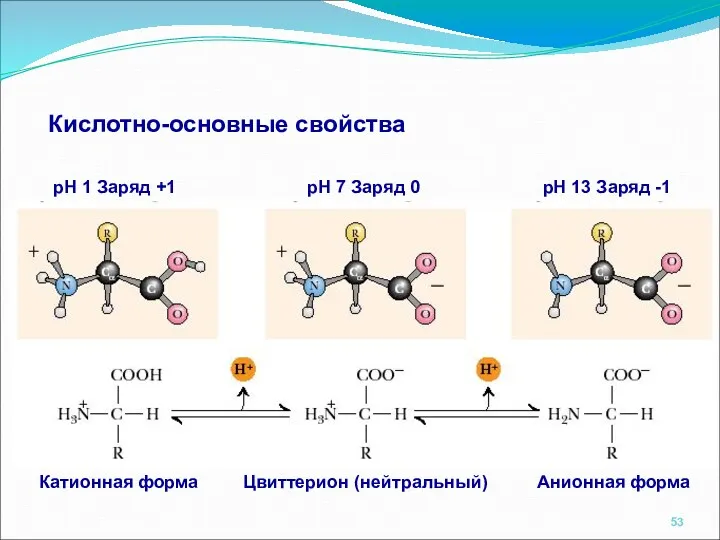
- 53. Кислотно-основные свойства pH 1 Заряд +1 pH 7 Заряд 0 pH 13 Заряд -1 Цвиттерион (нейтральный)
- 54. 1) NH2 – CH2 – COOH + НС| → [NH3 – CH2 – COOH ] С|
- 55. Химические свойства определяемые карбоксильной группой Образование эфиров Э. Фишер (1901)
- 56. Образование галогенангидридов
- 57. Реакции с участием только аминогруппы Образование N-ацильных производных Карбобензоксизащита (1932 г) карбобензоксихлорид (бензиловый эфир хлормуравьиной кислоты).
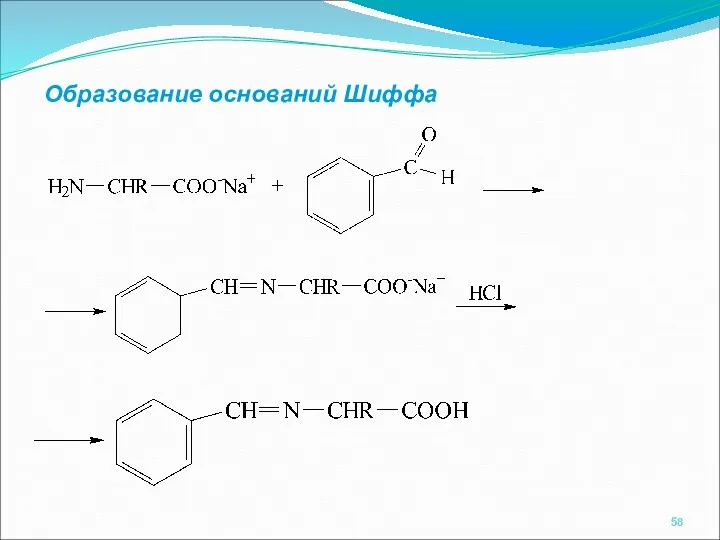
- 58. Образование оснований Шиффа
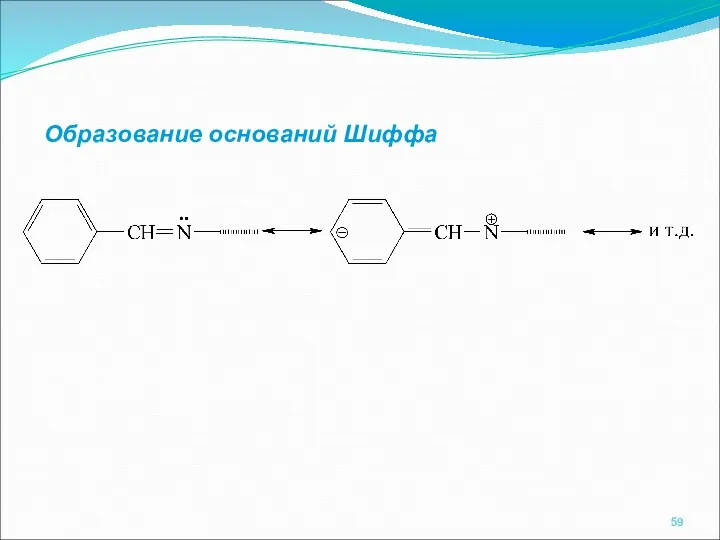
- 59. Образование оснований Шиффа
- 60. Биологически значимые реакции
- 61. Реакции гидроксилирования
- 62. Дезаминирование аминокислот Метод Ван-Слайка А. Внутримолекулярное дезаминирование (таким образом у некоторых микроорганизмов и высших растений аспарагиновая
- 63. Б. Восстановительное дезаминирование (у некоторых микроорганизмов ) В. Гидролитическое дезаминирование (тип дезаминирования, характерный для микроорганизмов)
- 64. Биологически важные химические реакции Окислительное дезаминирование
- 65. Биологически важные химические реакции Декарбоксилирование
- 66. Биологически важные химические реакции Декарбоксилирование глютаминовой кислоты приводит к образованию у-аминомасляной кислоты Декарбоксилирование в организме
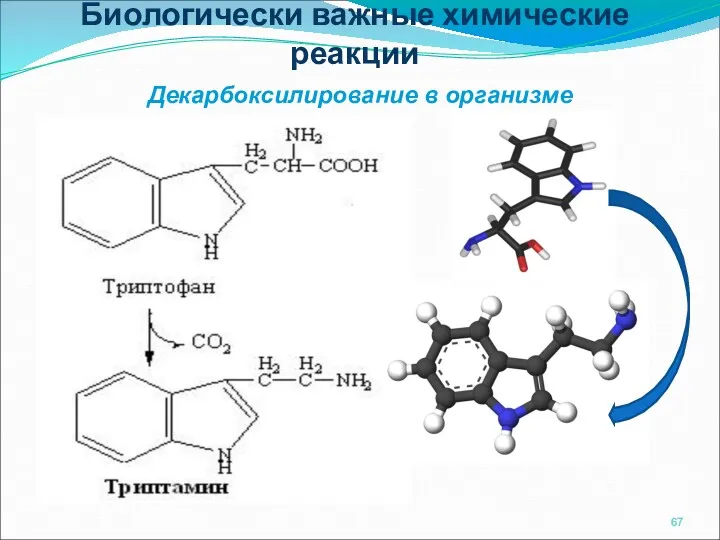
- 67. Биологически важные химические реакции Декарбоксилирование в организме
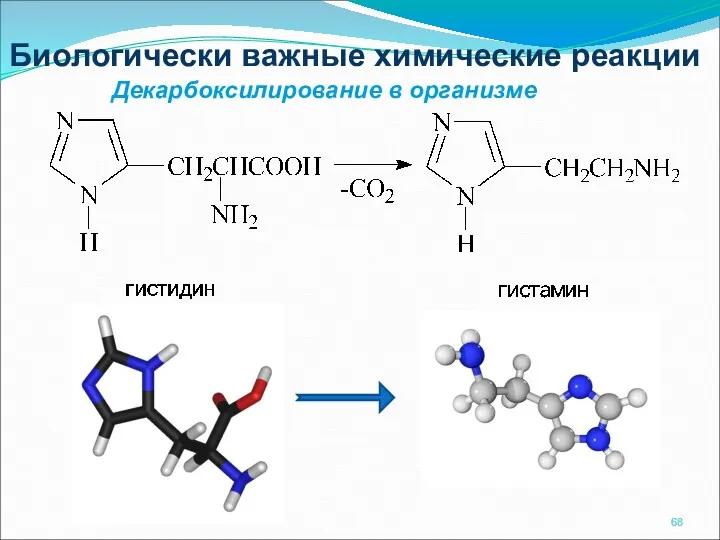
- 68. Биологически важные химические реакции Декарбоксилирование в организме
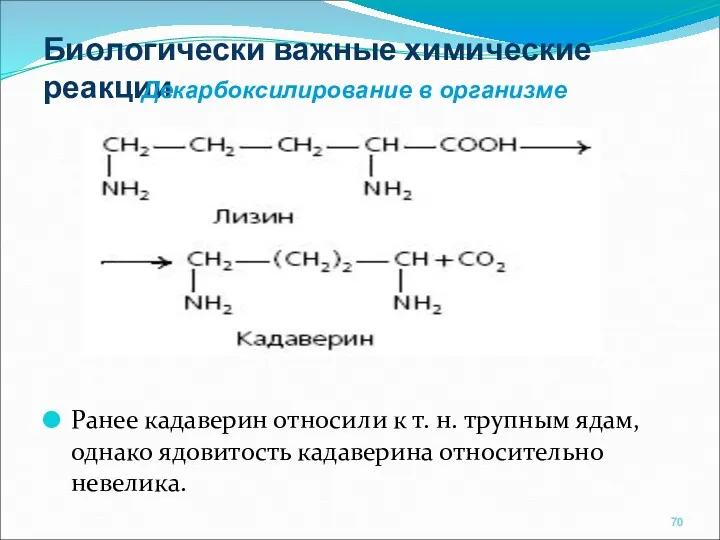
- 70. Биологически важные химические реакции Ранее кадаверин относили к т. н. трупным ядам, однако ядовитость кадаверина относительно
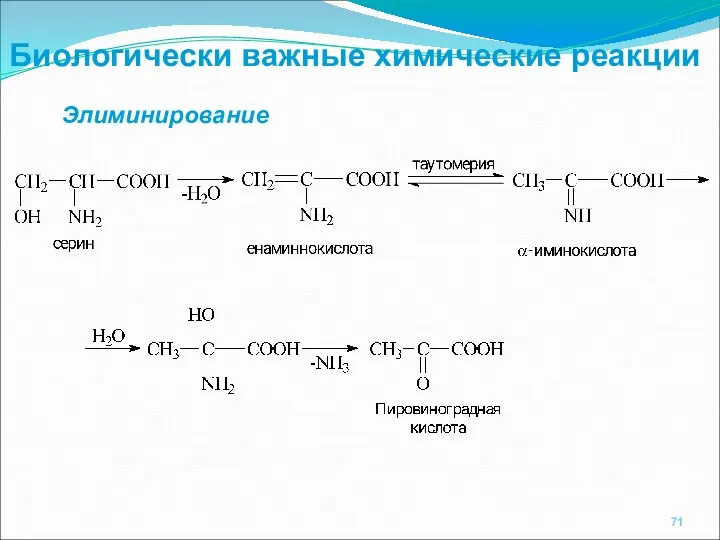
- 71. Биологически важные химические реакции Элиминирование
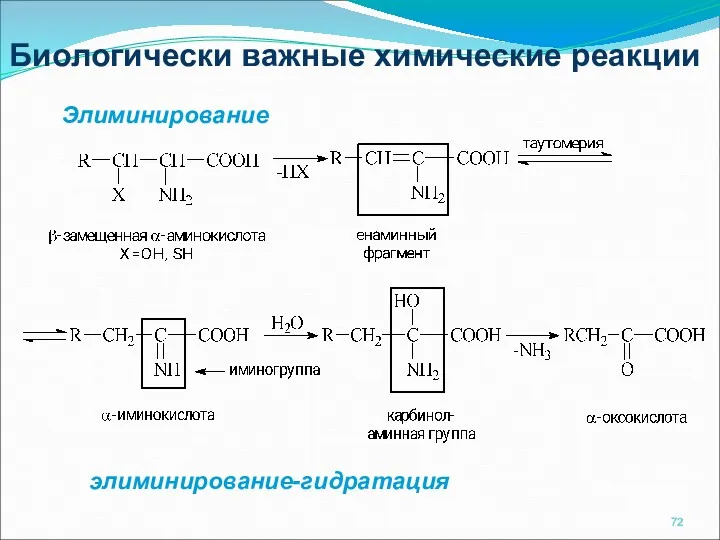
- 72. Биологически важные химические реакции Элиминирование элиминирование-гидратация
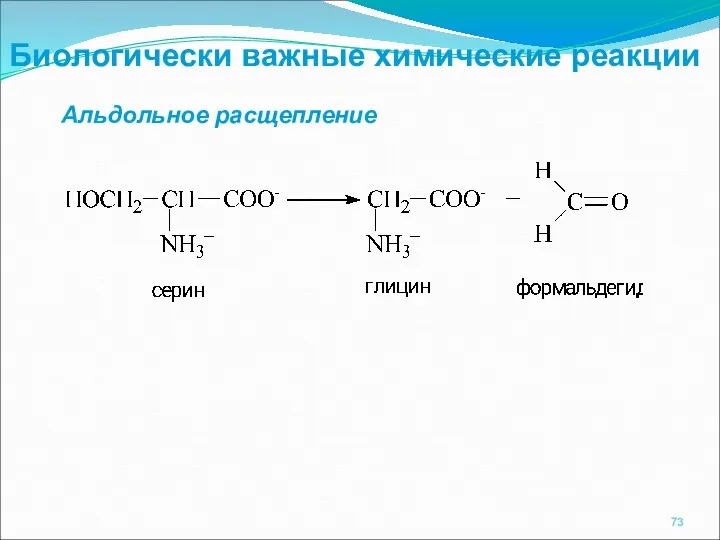
- 73. Биологически важные химические реакции Альдольное расщепление
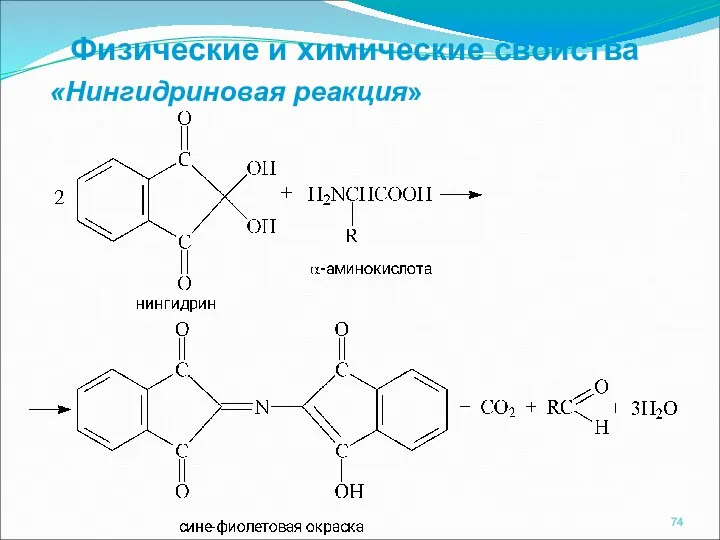
- 74. «Нингидриновая реакция» Физические и химические свойства
- 76. Скачать презентацию









































 Военно-мостовая подготовка. Итоговый тест
Военно-мостовая подготовка. Итоговый тест Модернизация автоматизированной системы управления паровым котлом ДЕ – 25/14 ГМ в котельном цехе
Модернизация автоматизированной системы управления паровым котлом ДЕ – 25/14 ГМ в котельном цехе Добрые дела – это не скучно
Добрые дела – это не скучно Представления. Проектирование и разработка веб-сервисов
Представления. Проектирование и разработка веб-сервисов Ретинол
Ретинол Все вместе сейчас - новый телевизионный музыкальный формат
Все вместе сейчас - новый телевизионный музыкальный формат Measuring instruments
Measuring instruments Этапы развития менеджмента в туризме
Этапы развития менеджмента в туризме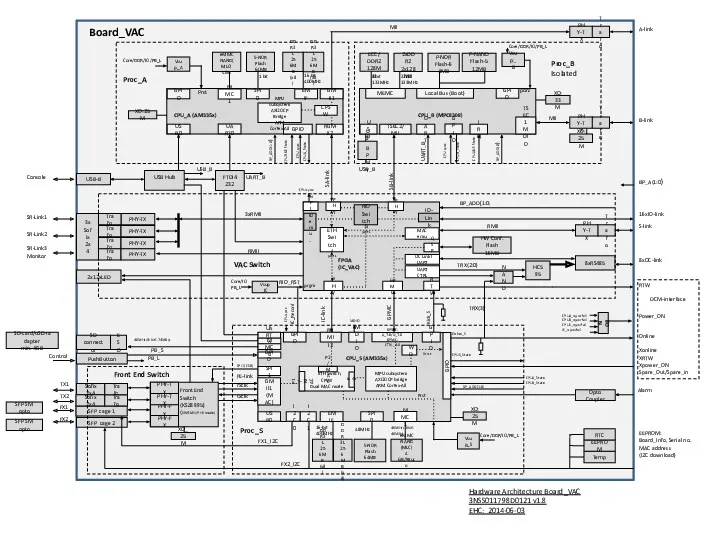 Схема opto coupler alarm
Схема opto coupler alarm Антарктида. Географическое положение и история исследования
Антарктида. Географическое положение и история исследования Let's get a Pet
Let's get a Pet Раскол в русской православной церкви во второй половине XVII века
Раскол в русской православной церкви во второй половине XVII века Корпоративные ценные бумаги: Акции
Корпоративные ценные бумаги: Акции Модульные системы индустриального остекления CARBOGLASS PRO
Модульные системы индустриального остекления CARBOGLASS PRO Игорь Васильев. Первые 50 лет
Игорь Васильев. Первые 50 лет Использование ЦОР и ЭОР в работе учителя начальных классов
Использование ЦОР и ЭОР в работе учителя начальных классов Вusiness for 50 thousand dollars
Вusiness for 50 thousand dollars Badges. Stationery boxes
Badges. Stationery boxes Опорный конспект Коррозия металлов
Опорный конспект Коррозия металлов Депофорез гидроокиси меди-кальция. Эффективность применения при лечении осложненного кариеса
Депофорез гидроокиси меди-кальция. Эффективность применения при лечении осложненного кариеса : Олимпиада 2014.
: Олимпиада 2014. Изучение электродвигателя. Занятие 3
Изучение электродвигателя. Занятие 3 Создание условий для развития инициативы и творческих способностей детей старшего дошкольного возраста в центре нравственно-патриотического воспитания.
Создание условий для развития инициативы и творческих способностей детей старшего дошкольного возраста в центре нравственно-патриотического воспитания. Интерьер жилого дома (ИЗО)
Интерьер жилого дома (ИЗО) Богоматерь Владимирская. Первая треть XII в
Богоматерь Владимирская. Первая треть XII в Магнитные наночастицы. Применение в биомедицине
Магнитные наночастицы. Применение в биомедицине Соматические заболевания
Соматические заболевания Ландшафтоведение. Типы морфолитогенеза (часть 2)
Ландшафтоведение. Типы морфолитогенеза (часть 2)