Содержание
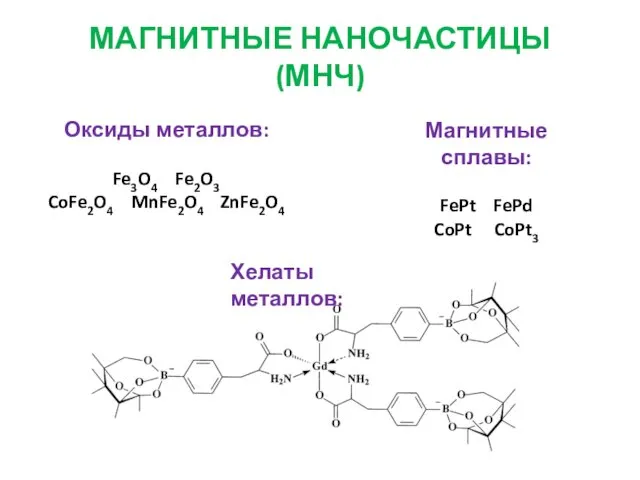
- 2. Оксиды металлов: Fe3O4 Fe2O3 CoFe2O4 MnFe2O4 ZnFe2O4 Магнитные сплавы: FePt FePd CoPt CoPt3 Хелаты металлов: МАГНИТНЫЕ
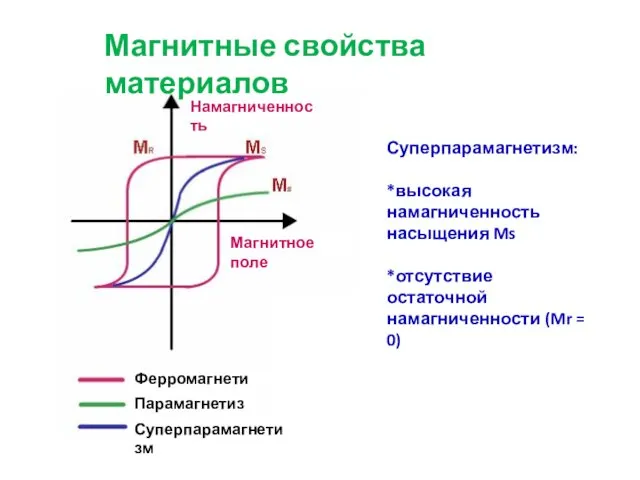
- 3. Суперпарамагнетизм: *высокая намагниченность насыщения Ms *отсутствие остаточной намагниченности (Mr = 0) Магнитные свойства материалов
- 4. Методы синтеза МНЧ. Осаждение из раствора. Механизм образования одинаковых частиц в растворе: I – одиночная нуклеация
- 5. Методы синтеза МНЧ . Термическое разложение органических прекурсоров. Морфология наночастиц магемита, полученных методом термического разложения различных
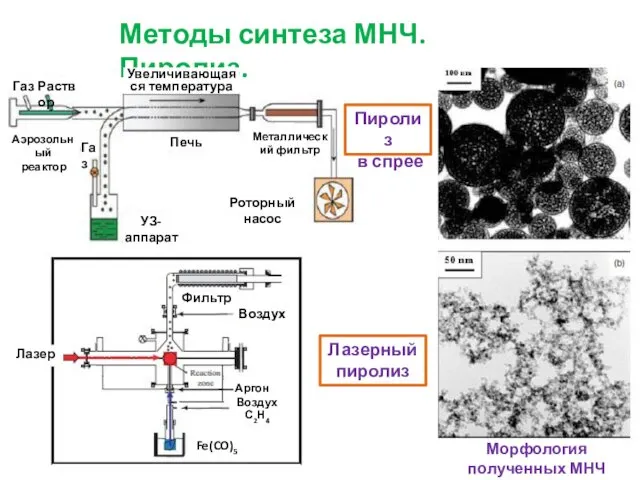
- 6. Лазерный пиролиз Методы синтеза МНЧ. Пиролиз. Пиролиз в спрее Морфология полученных МНЧ Газ Раствор Аэрозольный реактор
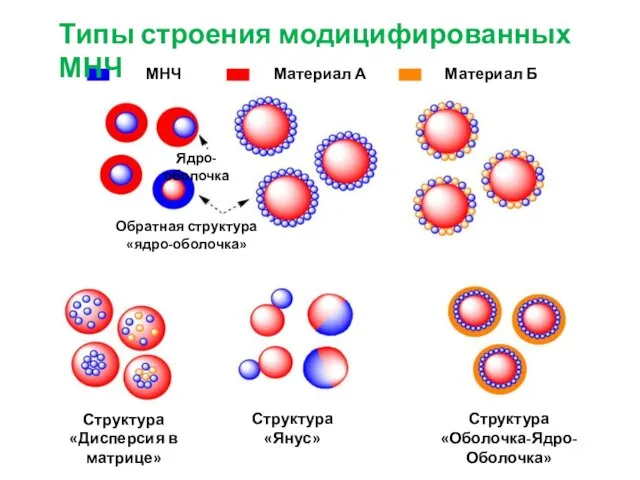
- 7. МНЧ Материал А Материал Б Ядро-оболочка Обратная структура «ядро-оболочка» Структура «Дисперсия в матрице» Структура «Янус» Структура
- 8. органические синтетические полимеры (хитозан, декстран, ПЭГ, ПВП, ПВС и пр.) белки силаны оксид кремния золото, гадолиний
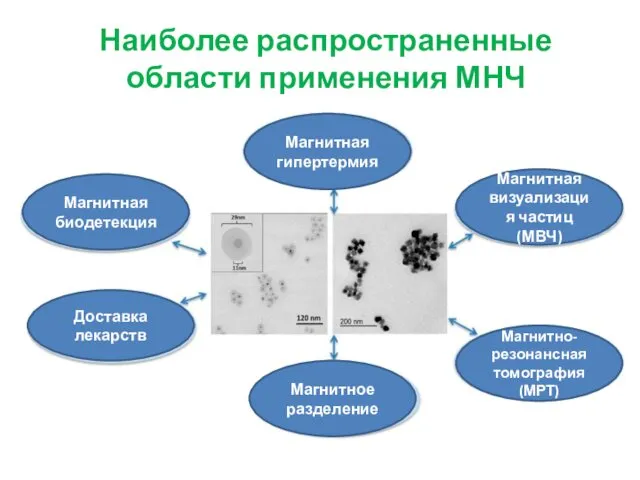
- 9. Наиболее распространенные области применения МНЧ
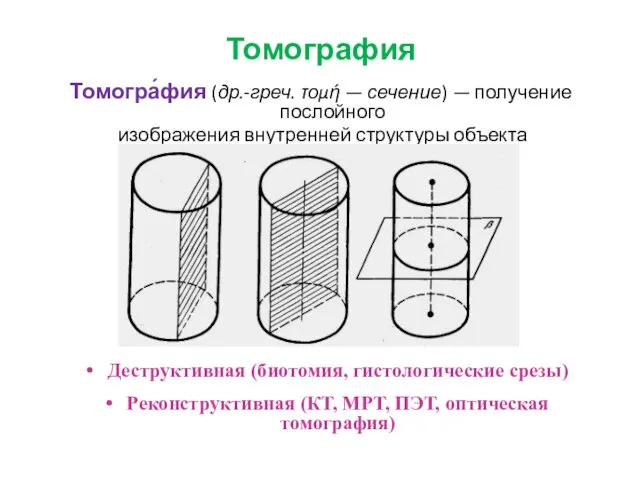
- 10. Томография Томогра́фия (др.-греч. τομή — сечение) — получение послойного изображения внутренней структуры объекта Деструктивная (биотомия, гистологические
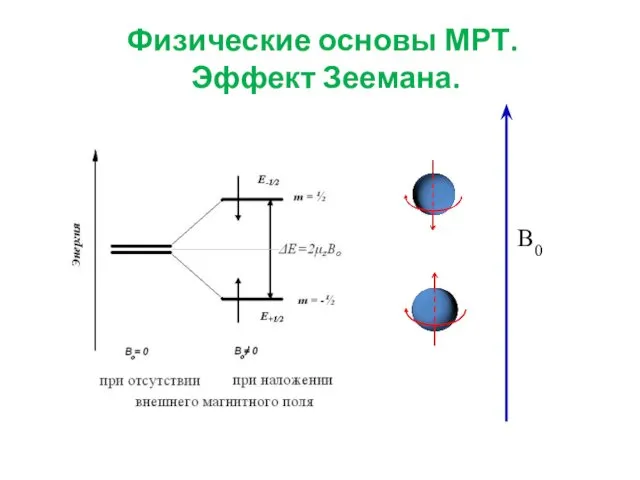
- 11. Физические основы МРТ. Эффект Зеемана. B0
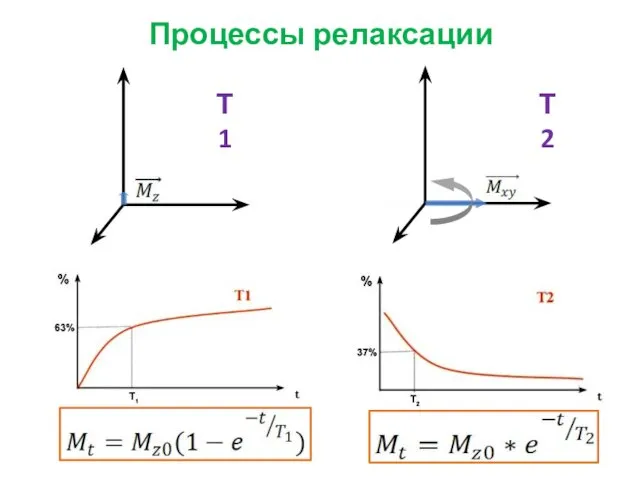
- 12. Т1 Т2 Процессы релаксации
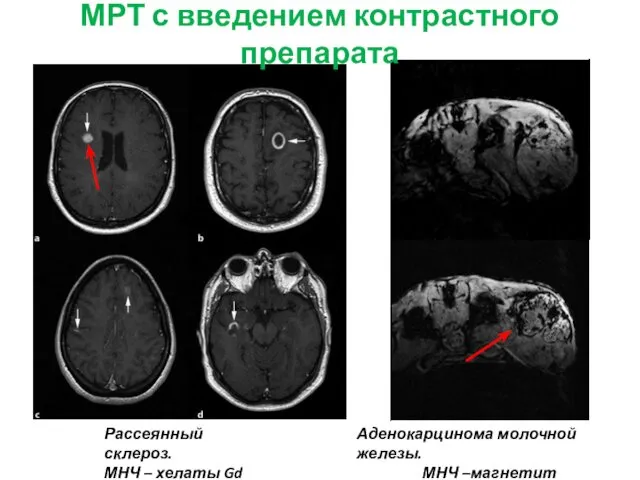
- 13. МРТ с введением контрастного препарата Рассеянный склероз. МНЧ – хелаты Gd Аденокарцинома молочной железы. МНЧ –магнетит
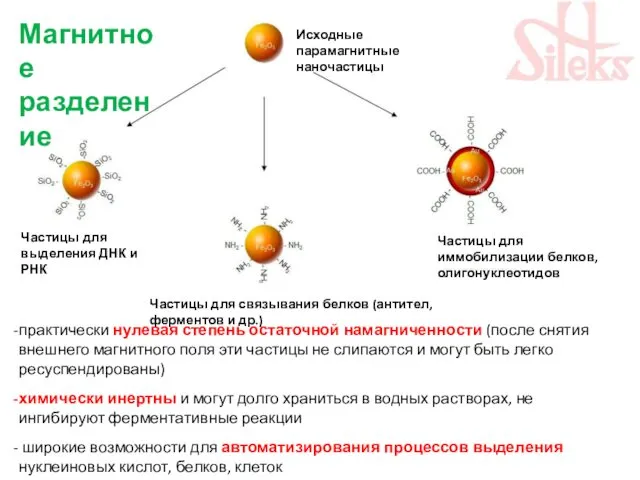
- 14. практически нулевая степень остаточной намагниченности (после снятия внешнего магнитного поля эти частицы не слипаются и могут
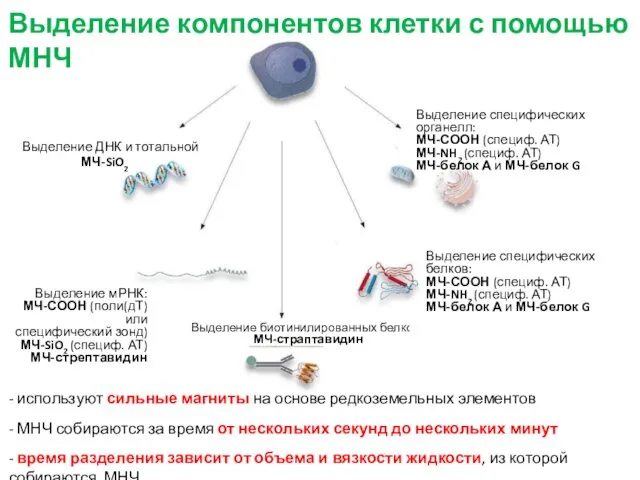
- 15. Выделение компонентов клетки с помощью МНЧ - используют сильные магниты на основе редкоземельных элементов - МНЧ
- 16. Преимущества магнитных наночастиц оксида железа Низкая токсичность Биосовместимость Высокая стабильность в водных растворах Низкая стоимость Простота
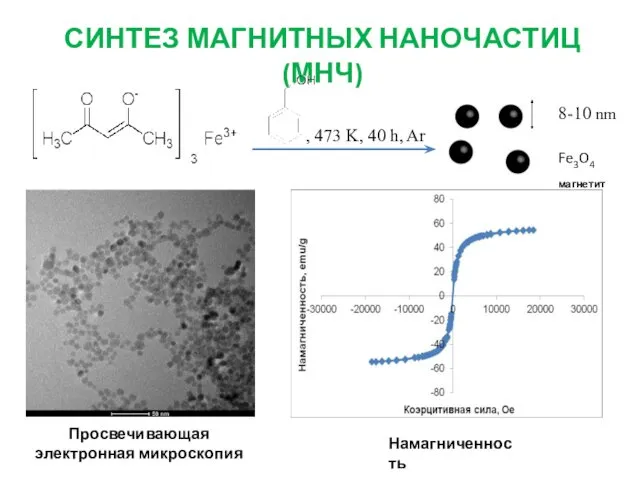
- 17. СИНТЕЗ МАГНИТНЫХ НАНОЧАСТИЦ (МНЧ) , 473 K, 40 h, Ar Просвечивающая электронная микроскопия Намагниченность Fe3O4 магнетит
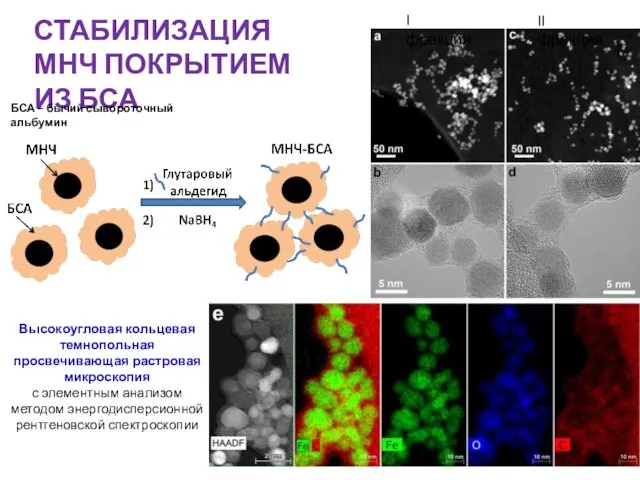
- 18. СТАБИЛИЗАЦИЯ МНЧ ПОКРЫТИЕМ ИЗ БСА I фракция II фракция Высокоугловая кольцевая темнопольная просвечивающая растровая микроскопия с
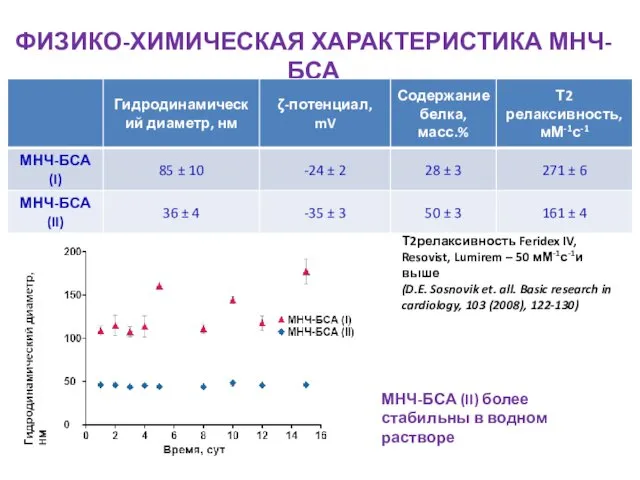
- 19. ФИЗИКО-ХИМИЧЕСКАЯ ХАРАКТЕРИСТИКА МНЧ-БСА МНЧ-БСА (II) более стабильны в водном растворе Т2релаксивность Feridex IV, Resovist, Lumirem –
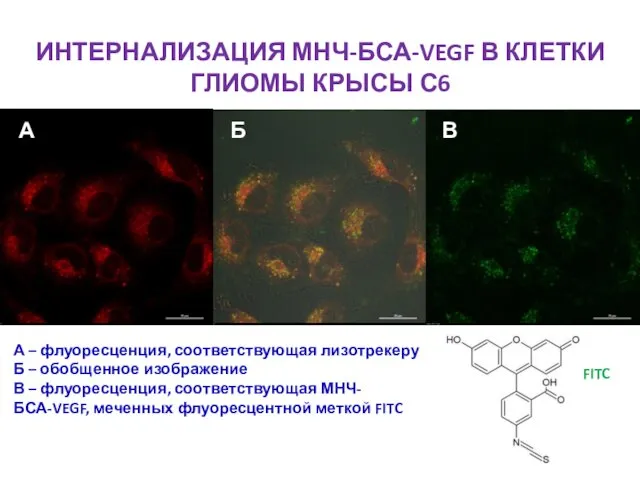
- 20. ИНТЕРНАЛИЗАЦИЯ МНЧ-БСА-VEGF В КЛЕТКИ ГЛИОМЫ КРЫСЫ С6 А Б В А – флуоресценция, соответствующая лизотрекеру Б
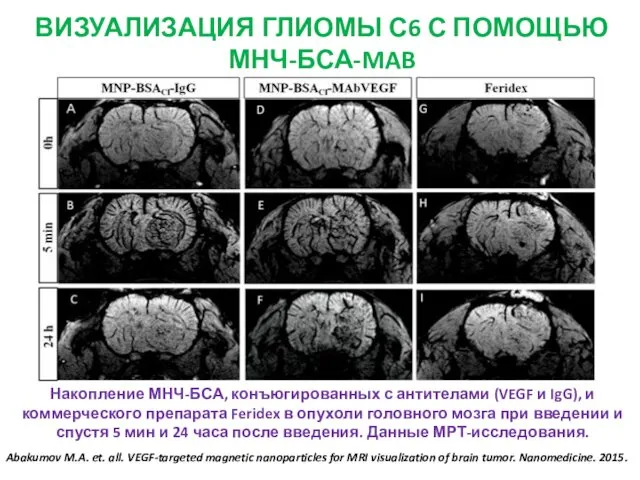
- 21. ВИЗУАЛИЗАЦИЯ ГЛИОМЫ С6 С ПОМОЩЬЮ МНЧ-БСА-MAB Накопление МНЧ-БСА, конъюгированных с антителами (VEGF и IgG), и коммерческого
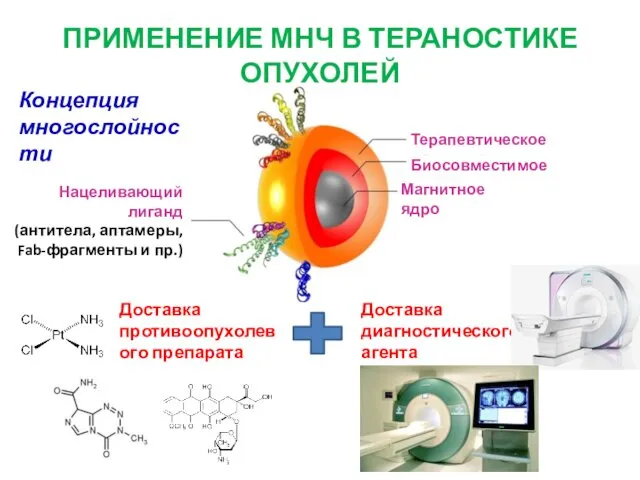
- 22. ПРИМЕНЕНИЕ МНЧ В ТЕРАНОСТИКЕ ОПУХОЛЕЙ Доставка противоопухолевого препарата Доставка диагностического агента Нацеливающий лиганд (антитела, аптамеры, Fab-фрагменты
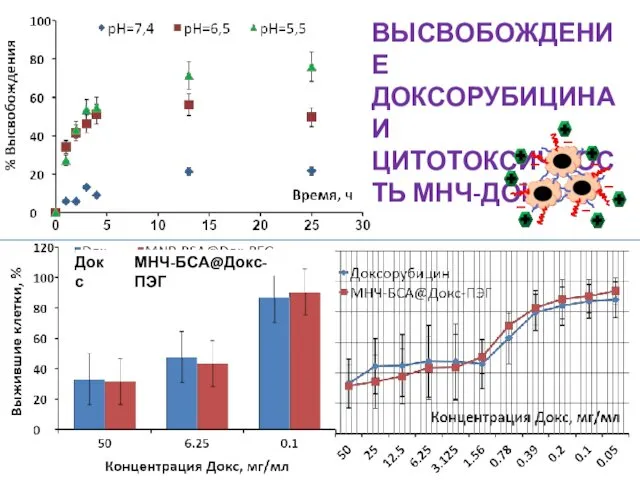
- 23. ВЫСВОБОЖДЕНИЕ ДОКСОРУБИЦИНА И ЦИТОТОКСИЧНОСТЬ МНЧ-ДОКС
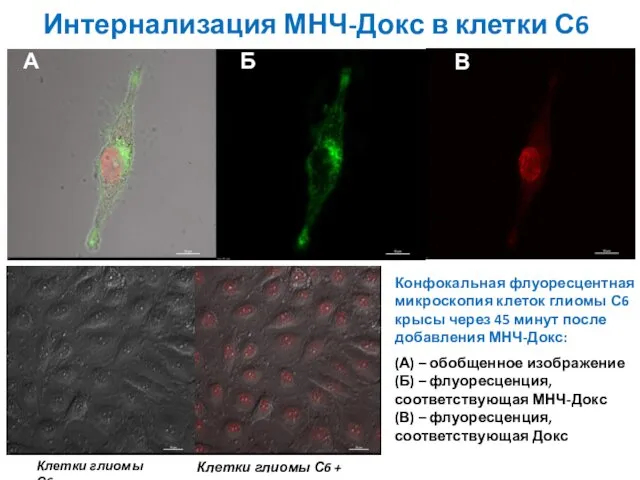
- 24. А Б В Конфокальная флуоресцентная микроскопия клеток глиомы С6 крысы через 45 минут после добавления МНЧ-Докс:
- 25. Терапия с применением МНЧ-БСА@Докс-ПЭГ-VEGF позволила значительно повысить значение медианы выживаемости животных по сравнению с контрольной группой,
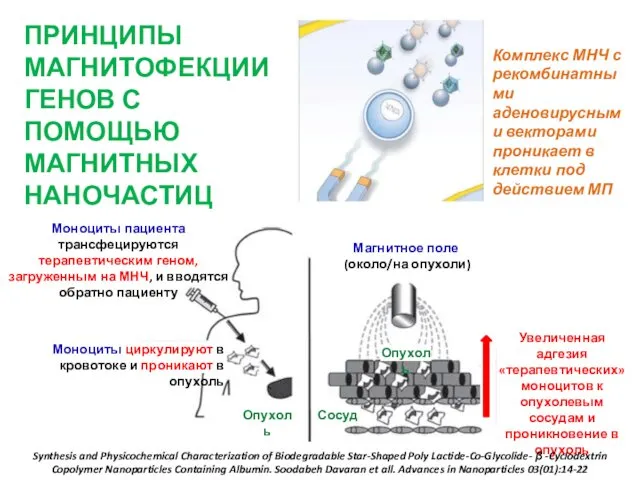
- 26. Комплекс МНЧ с рекомбинатными аденовирусными векторами проникает в клетки под действием МП Моноциты пациента трансфецируются терапевтическим
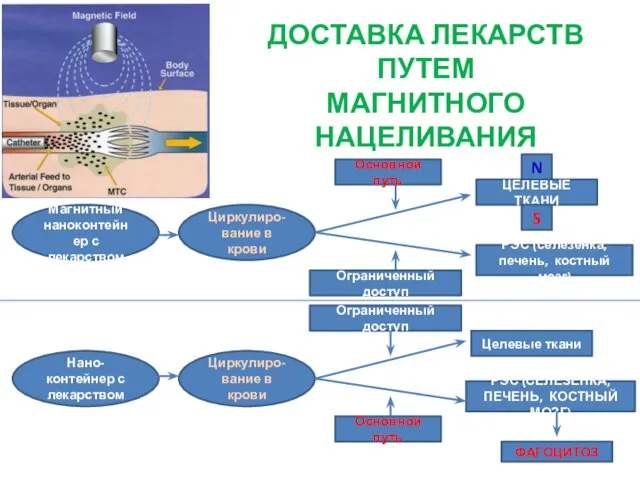
- 27. Нано-контейнер с лекарством Циркулиро-вание в крови Магнитный наноконтейнер с лекарством Циркулиро-вание в крови Целевые ткани РЭС
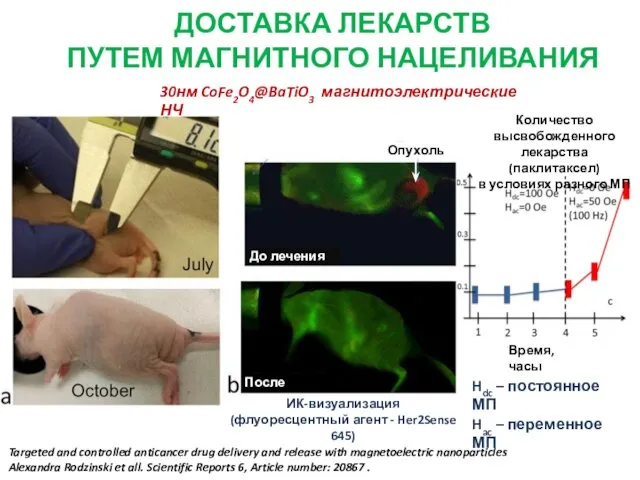
- 28. Targeted and controlled anticancer drug delivery and release with magnetoelectric nanoparticles Alexandra Rodzinski et all. Scientific
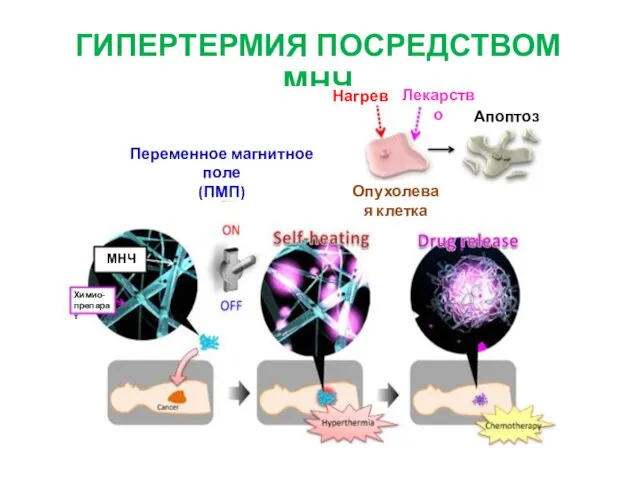
- 29. ГИПЕРТЕРМИЯ ПОСРЕДСТВОМ МНЧ Переменное магнитное поле (ПМП) Нагрев Лекарство Апоптоз Опухолевая клетка
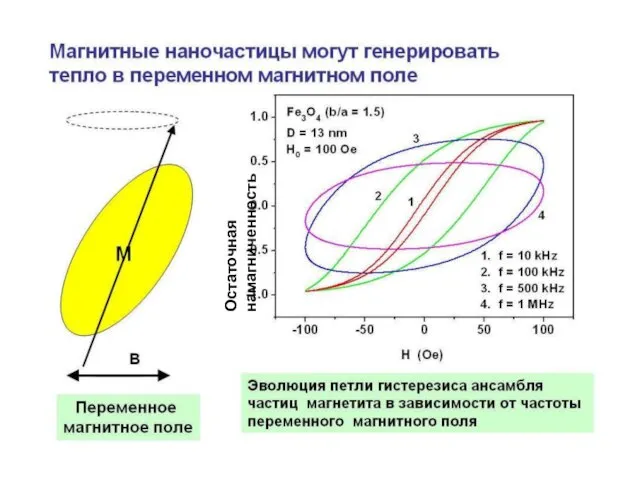
- 30. Остаточная намагниченность
- 31. Гипертермия с помощью магнитолипосом МЛ Опухоль Температура, °С Время нахождения в ПМП (мин) Температура в левой
- 32. ПРИМЕНЕНИЕ МНЧ ДЛЯ ГИПЕРТЕРМИИ ОПУХОЛЕЙ (ДОКЛИНИЧЕСКИЕ ИСПЫТАНИЯ ЗА ПОСЛЕДНИЕ 5 ЛЕТ) An arsenal of magnetic nanoparticles;
- 34. Скачать презентацию







 Безопасный локомотивный объединенный комплекс БЛОК-М. Эксплуатация
Безопасный локомотивный объединенный комплекс БЛОК-М. Эксплуатация Моя будущая профессия - учитель
Моя будущая профессия - учитель Анализ системы образования и научной деятельности Технологического института Массачусетса
Анализ системы образования и научной деятельности Технологического института Массачусетса Маркерные радиомаяки
Маркерные радиомаяки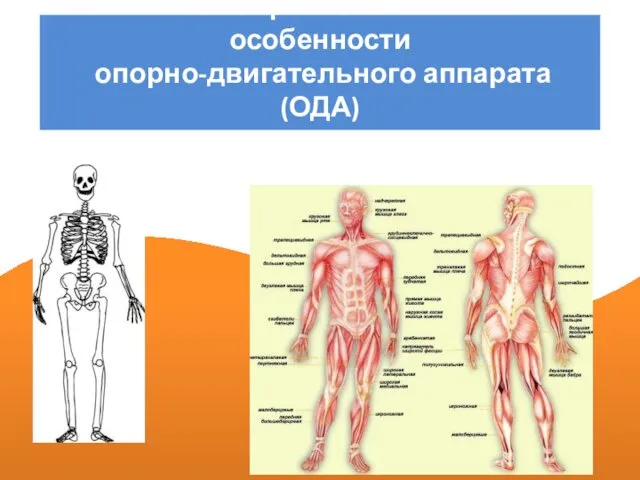 Анатомо-физиологические особенности опорно-двигательного аппарата (ОДА) у подростков
Анатомо-физиологические особенности опорно-двигательного аппарата (ОДА) у подростков Избирательная система
Избирательная система математика 6 класс
математика 6 класс Создание своими руками скворечника и кормушки, для замерзших птиц. (5 класс)
Создание своими руками скворечника и кормушки, для замерзших птиц. (5 класс) Планеты гиганты
Планеты гиганты Чековая книжка желаний
Чековая книжка желаний презентация к классному часу
презентация к классному часу Порядок слов в английском предложении
Порядок слов в английском предложении Ғимараттарды қайтадан құру жобалау жұмыстарының технологиясы
Ғимараттарды қайтадан құру жобалау жұмыстарының технологиясы Математика әлеміне саяхат
Математика әлеміне саяхат презентация опыта
презентация опыта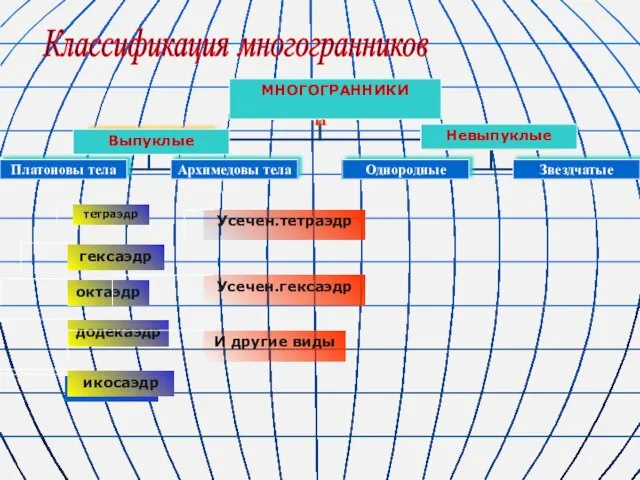 Классификация многогранников
Классификация многогранников Проектирование предприятий общественного питания
Проектирование предприятий общественного питания Формы размножения организмов
Формы размножения организмов Религия, её виды, функции, структура
Религия, её виды, функции, структура Педагогический Проект Коррекция речевых нарушений у детей старшего дошкольного возраста посредством развития мелкой моторики
Педагогический Проект Коррекция речевых нарушений у детей старшего дошкольного возраста посредством развития мелкой моторики Регистрация религиозных объединений
Регистрация религиозных объединений Етеккір циклының бұзылуы. Этиопатогенезі, клиникасы. Диагностикасы
Етеккір циклының бұзылуы. Этиопатогенезі, клиникасы. Диагностикасы Повторение 8 класса. Основные понятия химии
Повторение 8 класса. Основные понятия химии Жону мен өңдеу сипаттамасы және технологиялық мүмкіндіктері
Жону мен өңдеу сипаттамасы және технологиялық мүмкіндіктері Родительское собрание Эти домашние задания
Родительское собрание Эти домашние задания Презентация Использование камушков Марблс для развития познавательной активности у детей старшего дошкольного возраста с нарушением зрения.
Презентация Использование камушков Марблс для развития познавательной активности у детей старшего дошкольного возраста с нарушением зрения. Общая характеристика ОАО НК Роснефть
Общая характеристика ОАО НК Роснефть Деньги и их эволюция
Деньги и их эволюция