Содержание
- 2. Простые вещества, и основные степени окисления ns2np3 N2 N≡N Химия азота богата на количество соединений с
- 3. Простые вещества, и основные степени окисления ns2np3 +5 H3PO4, PF5 +3 Na2HPO3, PCl3 +1 KH2PO2 0
- 4. Простые вещества, и основные степени окисления ns2np3 As – мышьяк, arsenicum Соли – арсениды, арсениты, арсенаты.
- 5. Простые вещества, и основные степени окисления ns2np3 Bi – висмут, bismuthum. Самый «тяжелый» нерадиоактивый металл. +5
- 6. Распространение на Земле
- 7. Азот получение Промышленное Фракционная перегонка жидкого воздуха Применение Черный порох: 2KNO3 + 3C + S =
- 8. Азот получение Лабораторное NH4NO2 → N2↑ + 2H2O + Q K2Cr2O7 + (NH4)2SO4 = (NH4)2Cr2O7 +
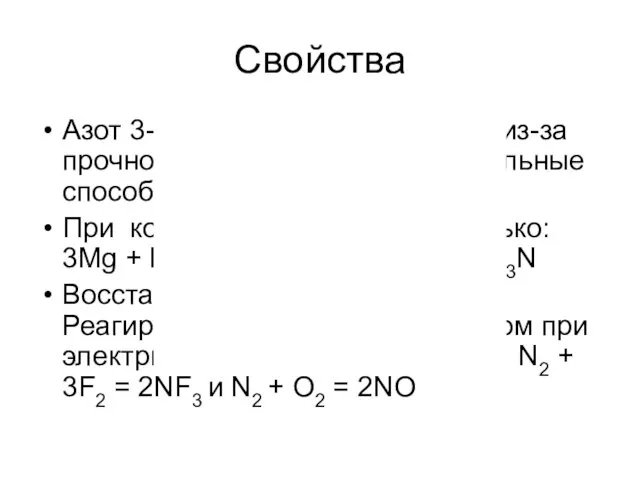
- 9. Свойства Азот 3-ий по ЭО после F и О! Но из-за прочности молекулы N2 окислительные способности
- 10. Бинарные соединения – нитириды. Делятся на ионные и ковалентные. Свойства Примеры: TiN (ковалентный, куб. алмазоподоб.) AlN
- 11. Свойства
- 12. Свойства 6Ti + N2 → 2TiN, 2B + N2 →2BN, CaC2 + N2 → CaCN2 +
- 13. Аммиак NH3 + H2O → NH4+ + OH−; Kb=1,8·10−5 Аммиа́к — NH3, нитрид водорода, при нормальных
- 14. Аммиак Комплексообразование CuSO4 + 4NH3 → [Cu(NH3)4]SO4 Ni(NO3)2 + 6NH3 → [Ni(NH3)6](NO3)2 Соли аммония – б.ц.,
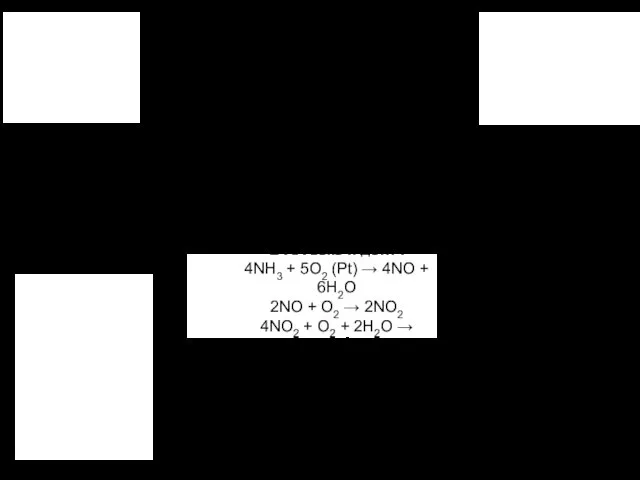
- 15. Азотная кислота Производство: В XX веке и до… : 4NH3 + 5O2 (Pt) → 4NO +
- 16. Применение в производстве минеральных удобрений; в производстве красителей и лекарств (нитроглицерин) в военной промышленности (дымящая —
- 17. Азотная кислота Различные азотсодержащие продукты при взаимодействии азотной кислоты с различными веществами: увеличение концентрации кислоты увеличение
- 18. Азотная кислота Различные азотсодержащие продукты при взаимодействии азотной кислоты с различными веществами: увеличение концентрации кислоты увеличение
- 19. Оксида азота N2O – несолеобразующий NO – несолеобразующий N2O3 – кислый NO2 – несолеобразующий N2O5 –
- 20. Хим. свойства P, As, Sb, Bi Степень окисления (– 3). PH3, AsH3, SbH3, BiH3. 3Mg +
- 21. Степень окисление = 0. Горение на воздухе: 4P + 5O2 → P4O10 2As(и др.) + 3O2
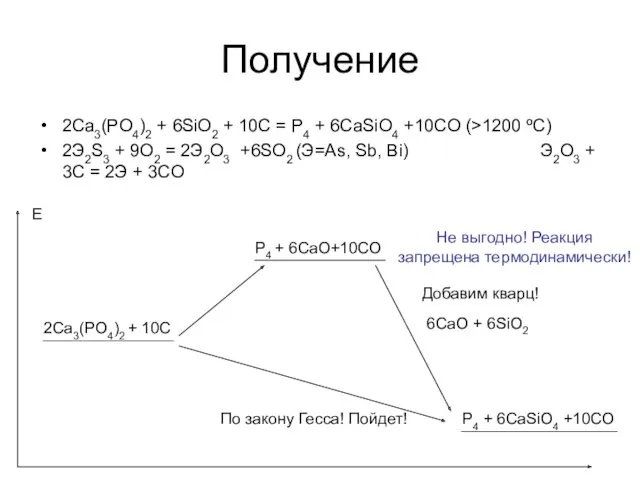
- 22. Получение 2Ca3(PO4)2 + 6SiO2 + 10C = P4 + 6CaSiO4 +10CO (>1200 ºC) 2Э2S3 + 9O2
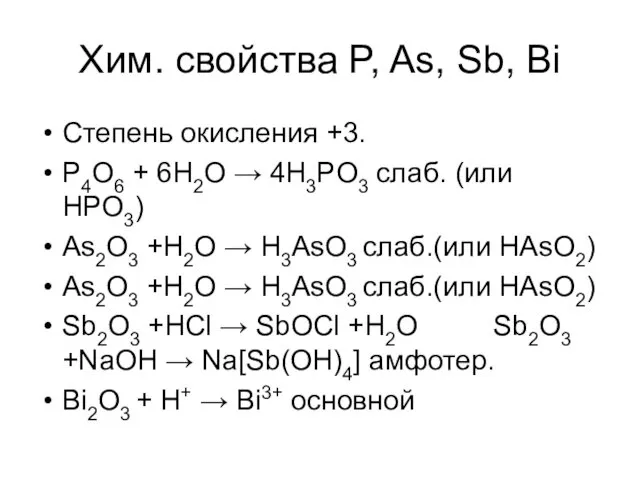
- 23. Степень окисления +3. P4O6 + 6H2O → 4H3PO3 слаб. (или HPO3) As2O3 +H2O → H3AsO3 слаб.(или
- 24. Степень окисления +5 P4O10 + 6H2O → 4H3PO4 (или HPO3) As2O5 + H2O → H3AsO3 (или
- 26. Скачать презентацию











![Аммиак Комплексообразование CuSO4 + 4NH3 → [Cu(NH3)4]SO4 Ni(NO3)2 + 6NH3](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/42353/slide-13.jpg)







 Шарль Пьер Бодлер (1821-1867)
Шарль Пьер Бодлер (1821-1867) Презентация Знаменитые деятели науки и культуры Тамбовского края
Презентация Знаменитые деятели науки и культуры Тамбовского края В бизнесе всё решают связью. Коммерческое предложение ПАО Ростелеком
В бизнесе всё решают связью. Коммерческое предложение ПАО Ростелеком Западная Сибирь. Население и хозяйство
Западная Сибирь. Население и хозяйство Эбру - искусство обработки бумаги
Эбру - искусство обработки бумаги 20230228_nalogi
20230228_nalogi Размножение фуксии черенками
Размножение фуксии черенками Синдром дефицита внимания и гиперактивность
Синдром дефицита внимания и гиперактивность Правописание безударных гласных в корне слова
Правописание безударных гласных в корне слова Умный дом
Умный дом Порядок оформления и ведения эксплуатационной и технической документации. Руководство по эксплуатации машины
Порядок оформления и ведения эксплуатационной и технической документации. Руководство по эксплуатации машины Малярия. Возбудитель малярии
Малярия. Возбудитель малярии В гостях у С.Я.Маршака
В гостях у С.Я.Маршака Азотування та ціанування сталі. Дифузійна металізація. Види, призначення, застосування
Азотування та ціанування сталі. Дифузійна металізація. Види, призначення, застосування Устный журнал России верные сыны
Устный журнал России верные сыны неделя начальной школы, посвященная Г.Х.Андерсену
неделя начальной школы, посвященная Г.Х.Андерсену Выделение. Выделение у растений
Выделение. Выделение у растений Технология обработки продукта убоя для производства мясных изделий
Технология обработки продукта убоя для производства мясных изделий Презентация Музыкальная предметно-развивающая среда как средство эмоционального развития ребенка
Презентация Музыкальная предметно-развивающая среда как средство эмоционального развития ребенка Силикатная промышленность. Керамика
Силикатная промышленность. Керамика Социо-игровые технологии по В.М.Букатову
Социо-игровые технологии по В.М.Букатову Выпускная квалификационная работа. Механизированная технология заготовки высокопитательного корма
Выпускная квалификационная работа. Механизированная технология заготовки высокопитательного корма Презентация из опыта работы по теме: Развитие творческого воображения у детей дошкольного возраста посредством изобразительной деятельности
Презентация из опыта работы по теме: Развитие творческого воображения у детей дошкольного возраста посредством изобразительной деятельности Этика сетевого общения
Этика сетевого общения Открытка ко Дню Святого Валентин
Открытка ко Дню Святого Валентин Основы самоменеджмента. Лекция 2
Основы самоменеджмента. Лекция 2 Игра, как основа социального развития детей
Игра, как основа социального развития детей Моя концепция классного руководителя
Моя концепция классного руководителя