Слайд 2
Основания-
электролиты, при диссоциации которых образуются катионы металла и анионы гидроксогрупп
NaOH —> Na+ + OH -
3+ -
Fe(OH)3 —> Fe + 3OH
Слайд 3
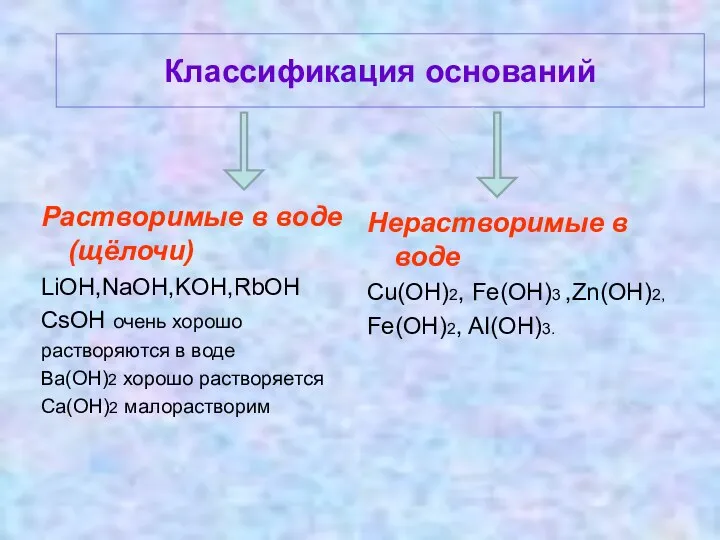
Классификация оснований
Растворимые в воде (щёлочи)
LiOH,NaOH,KOH,RbOH
CsOH очень хорошо
растворяются в воде
Ba(OH)2 хорошо растворяется
Ca(OH)2
малорастворим
Нерастворимые в воде
Cu(OH)2, Fe(OH)3 ,Zn(OH)2,
Fe(OH)2, AI(OH)3.
Слайд 4

Название оснований
Гидроксид
+
Название металла в родительном падеже
+
Валентность римскими цифрами
Слайд 5

Степень окисления гидроксогруппы –
Количество гидроксогрупп определяется валентностью металла, образующего
основание.
Например:
+1 +2 +3
Na OH, Ca (OH)2 , Fe (OH)3
Слайд 6

Изменение окраски индикатора в щелочной среде
Бесцветный фенолфталеин—малиновый
Метиловый оранжевый—желтый
лакмус—синий
Слайд 7
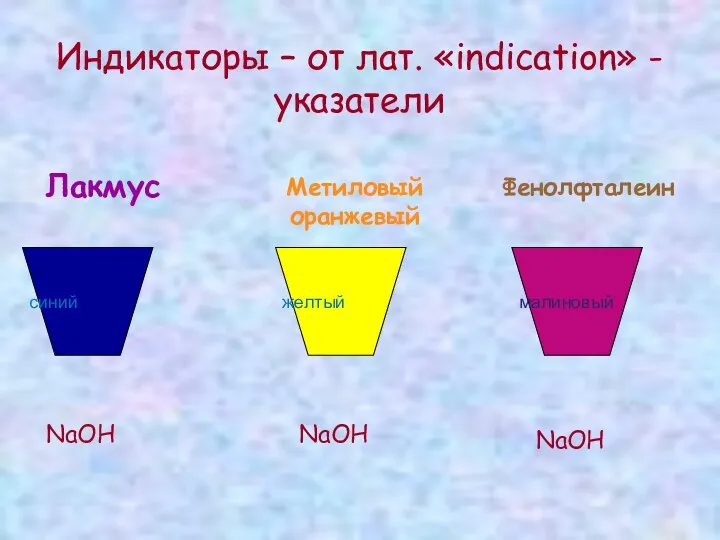
Индикаторы – от лат. «indication» - указатели
Лакмус
синий
NaOH
Метиловый оранжевый
желтый
NaOH
Фенолфталеин
малиновый
NaOH
Слайд 8

Типичные реакции растворимых оснований
РЕАГИРУЮТ С КИСЛОТАМИ
2KOH + H2SO4 —> K2SO4 +
2H2O
РЕАГИРУЮТ С РАСТВОРАМИ СОЛЕЙ
CuCI2 + 2KOH = Cu(OH)2 + 2KCI
РЕАГИРУЮТ С КИСЛОТНЫМИ ОКСИДАМИ
2KOH + CO2 —> K2CO3 + H2O
Слайд 9

Типичные реакции нерастворимых оснований
РЕАГИРУЮТ С КИСЛОТАМИ
2Fe(OH)3 + 3H2SO4—>Fe2(SO4)3+6H2O
ПРИ НАГРЕВАНИИ
РАЗЛАГАЮТСЯ
2Fe(OH)3 —> Fe2O3 + 3H2O
Слайд 10

ПРОВЕРЬ СЕБЯ
1.Формула основания это:
а) NaOH в) CuCL2
б) HCL г)
SO3
2. Лакмус в растворе, полученном при взаимодействии оксида кальция с водой:
а) синий в) фиолетовый
б) красный г) малиновый
3. С раствором гидроксида натрия взаимодействует:
а) оксид магния в) оксид цинка
б) оксид углерода г) сера
4. Нерастворимое основание при нагревании разлагаются:
а) Fe(OH)3 в) NaOH
б) Ba(OH)2 г) НСL
5. Пара ионов, которая может одновременно находится в растворе:
а) H+ и SiO3 в) Н+ и SO42-
б) Cu 2+ и ОН- г) Ag+ и CL-
6. Пара веществ взаимодействующих друг с другом:
а) H2SO4 u SiO2 в) Сu u H3PO4
б) CuO u Na2O г) НСl u NaOH









 технологическая карта урока
технологическая карта урока Первобытная магия и ритуалы
Первобытная магия и ритуалы Фенилалкиламины: источники, свойства и методы анализа
Фенилалкиламины: источники, свойства и методы анализа Создание агропромышленного комплекса по выращиванию, хранению, переработке и реализации картофеля. Бизнес-проект
Создание агропромышленного комплекса по выращиванию, хранению, переработке и реализации картофеля. Бизнес-проект Особенности управления персоналом в проектной деятельности
Особенности управления персоналом в проектной деятельности Подготовка сырьевых материалов по мокрому способу
Подготовка сырьевых материалов по мокрому способу Тест-тренажёр для 2 класса по теме: Устное сложение и вычитание в пределах 100
Тест-тренажёр для 2 класса по теме: Устное сложение и вычитание в пределах 100 Получение продукции животноводства. Разведение животных, их породы и продуктивность. 8 класс
Получение продукции животноводства. Разведение животных, их породы и продуктивность. 8 класс презентация День смеха.
презентация День смеха. развитие дыхания
развитие дыхания Гуманность, интеллект. Сочинение на ОГЭ. (Задание 15.3)
Гуманность, интеллект. Сочинение на ОГЭ. (Задание 15.3) Сумма углов треугольника
Сумма углов треугольника Организационное и правовое обеспечение информационной безопасности (ОПОИБ, лекция 1)
Организационное и правовое обеспечение информационной безопасности (ОПОИБ, лекция 1) Арены. Бензол.
Арены. Бензол. Методы искусственного прерывания беременности в ранние и поздние сроки
Методы искусственного прерывания беременности в ранние и поздние сроки Эксплуатация трансформаторов
Эксплуатация трансформаторов Роговица. Свойства и функции роговицы
Роговица. Свойства и функции роговицы Лукьянова О. СОШ 30Scientists and their discoveries that changed the world
Лукьянова О. СОШ 30Scientists and their discoveries that changed the world Презентация по теме: Двойные согласные
Презентация по теме: Двойные согласные Расчет точности технологической оснастки станков
Расчет точности технологической оснастки станков Материк Африка
Материк Африка презентация Наш 9 класс
презентация Наш 9 класс Презентация 9 мая - День Победы
Презентация 9 мая - День Победы Детский катехизис. Ответы на вопросы детей о Боге
Детский катехизис. Ответы на вопросы детей о Боге Презентация Я и моя память
Презентация Я и моя память Цифровые автоматы – общие сведения
Цифровые автоматы – общие сведения Транспарантное вырезание. Мастер-класс (ИЗО)
Транспарантное вырезание. Мастер-класс (ИЗО) Вред употребления: снюс, насвай
Вред употребления: снюс, насвай