Содержание
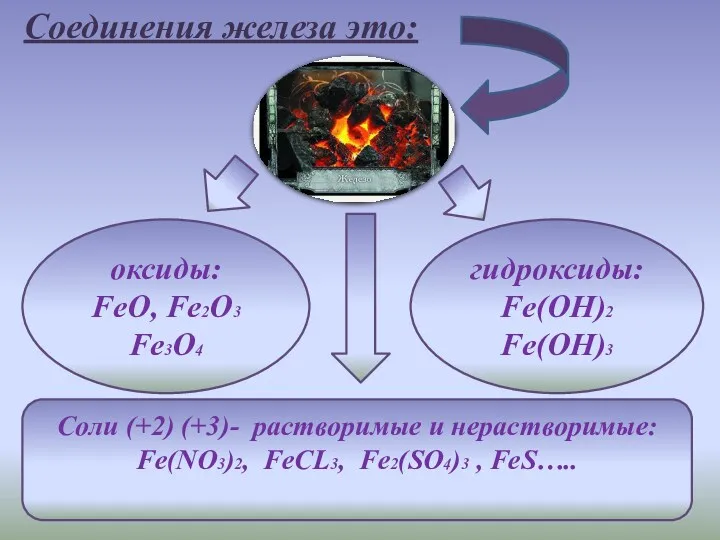
- 2. Соли (+2) (+3)- растворимые и нерастворимые: Fe(NO3)2, FeCL3, Fe2(SO4)3 , FeS….. оксиды: FeO, Fe2O3 Fe3O4 гидроксиды:
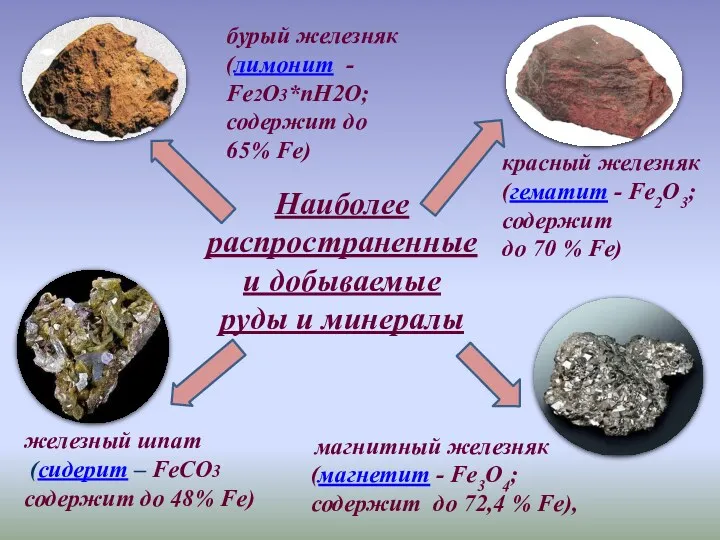
- 3. магнитный железняк (магнетит - Fe3O4; содержит до 72,4 % Fe), бурый железняк (лимонит - Fe2О3*пН2О; содержит
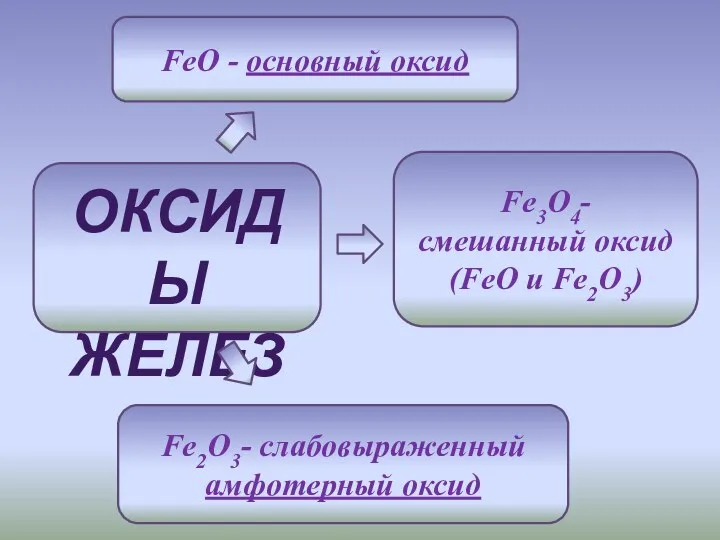
- 4. ОКСИДЫ ЖЕЛЕЗА FeO - основный оксид Fe2O3- слабовыраженный амфотерный оксид Fe3O4- смешанный оксид (FeO и Fe2O3)
- 5. Химические свойства FeO с кислотами: FeO + 2HCL=FeCL2 + H2O 2) с более активными металлами: 3FeO
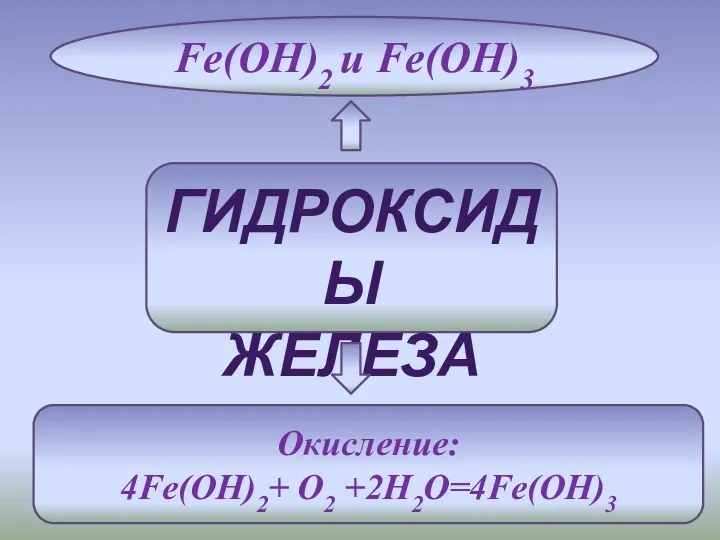
- 6. ГИДРОКСИДЫ ЖЕЛЕЗА Fe(OH)2 и Fe(OH)3 Окисление: 4Fe(OH)2+ O2 +2H2O=4Fe(OH)3
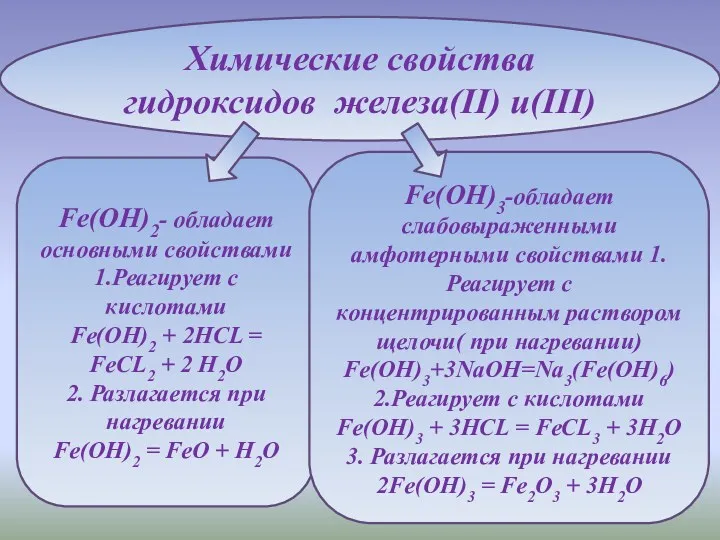
- 7. Химические свойства гидроксидов железа(II) и(III) Fe(OH)2- обладает основными свойствами 1.Реагирует с кислотами Fe(OH)2 + 2HCL =
- 8. Соли железа Реагируют с щелочами: FeCL2 + 2NaOH= Fe(OH)2 + 2 NaCL Реагируют с более активными
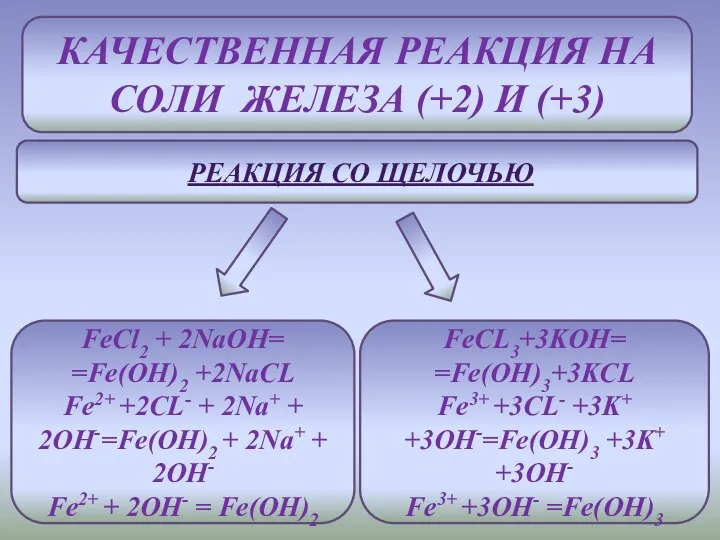
- 9. КАЧЕСТВЕННАЯ РЕАКЦИЯ НА Соли железа (+2) и (+3) Реакция со щелочью FeCl2 + 2NaOH= =Fe(OH)2 +2NaCL
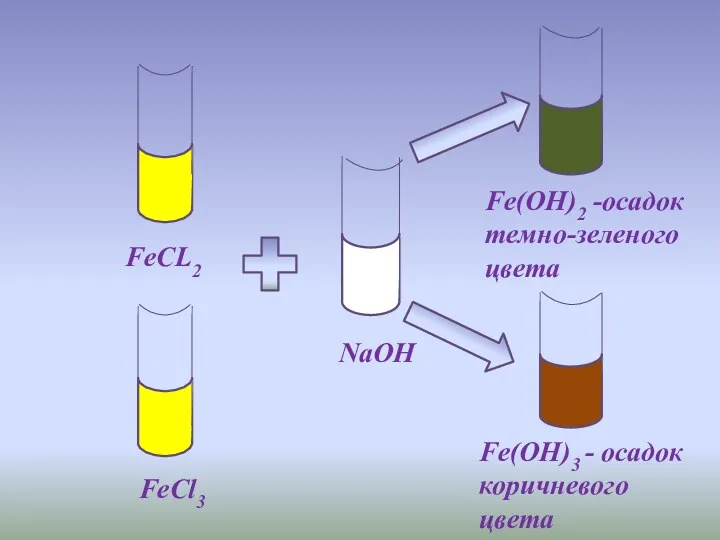
- 10. FeCL2 FeCl3 NaOH Fe(OH)2 -осадок темно-зеленого цвета Fe(OH)3 - осадок коричневого цвета
- 11. Находят широкое применение многие соединения железа. Например, сульфат железа (III) используют при водоподготовке, оксиды и цианид
- 12. Соли железа нужны для пополнения запасов железа в организме при лечении железистой анемии т.е. нехватки содержания
- 13. П Р О В Е Р Ь Т Е С Е Б Я С какими веществами
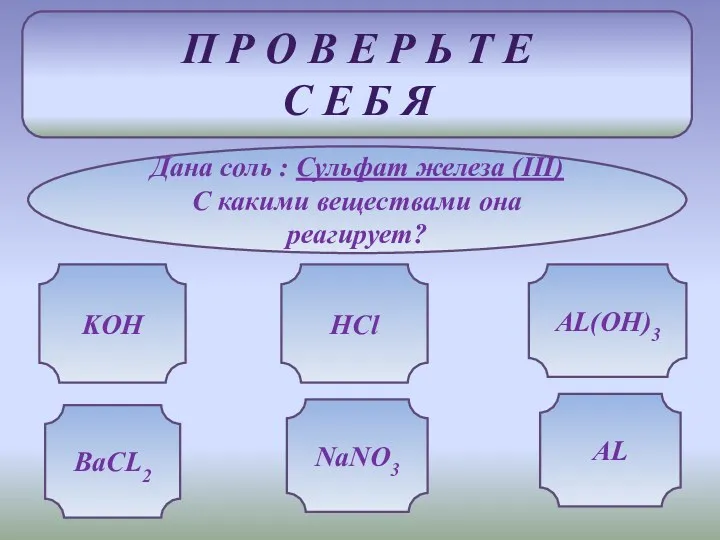
- 14. П Р О В Е Р Ь Т Е С Е Б Я Дана соль :
- 16. Скачать презентацию




 Врожденные пороки сердца
Врожденные пороки сердца Петербургские повести Н. В. Гоголя. Образ маленького человека
Петербургские повести Н. В. Гоголя. Образ маленького человека Історичні пам’ятки архітектури України
Історичні пам’ятки архітектури України ruslachik
ruslachik Проектирование разработки сеноманских отложений на Заполярном месторождении
Проектирование разработки сеноманских отложений на Заполярном месторождении День России. Викторина
День России. Викторина Предметно-пространственная среда средняя группа. Презентация
Предметно-пространственная среда средняя группа. Презентация Here we are! module 2
Here we are! module 2 Студийная фотосъемка. Тень и контраст в фотографии
Студийная фотосъемка. Тень и контраст в фотографии Показатели готовности детей с ОВЗ к обучению в условиях интегрированного образования.
Показатели готовности детей с ОВЗ к обучению в условиях интегрированного образования. Подготовительные работы при устройстве асфальтобетонных покрытий. Розлив вяжущих материалов
Подготовительные работы при устройстве асфальтобетонных покрытий. Розлив вяжущих материалов Организация и методика ветеринарно-санитарного осмотра продуктов убоя животных
Организация и методика ветеринарно-санитарного осмотра продуктов убоя животных деление суммы на число
деление суммы на число Викторина – путешествие по произведениям С.Я. Маршака
Викторина – путешествие по произведениям С.Я. Маршака Контроль качества отливок
Контроль качества отливок Презентация Конец слова за тобой (1 тип слоговой структуры слова)
Презентация Конец слова за тобой (1 тип слоговой структуры слова) Сосуды, работающие под избыточным давлением
Сосуды, работающие под избыточным давлением Descuentos en SeguroYo.Mx
Descuentos en SeguroYo.Mx Посвящение в пятиклассники
Посвящение в пятиклассники Алмашлыкларның төркемчәләрен кабатлау дәресе
Алмашлыкларның төркемчәләрен кабатлау дәресе Иррациональные уравнения
Иррациональные уравнения Петербурговедение , мосты Санкт-Петербурга
Петербурговедение , мосты Санкт-Петербурга Коллекционные карточные игры для гейм-дизайнеров
Коллекционные карточные игры для гейм-дизайнеров Общие сведения по проектированию механосборочного производства. (Тема 1)
Общие сведения по проектированию механосборочного производства. (Тема 1) электронное портфолио
электронное портфолио Диагностические карты для определения изобразительных, технических навыков и умений у детей дошкольного возраста
Диагностические карты для определения изобразительных, технических навыков и умений у детей дошкольного возраста Методическая разработка Тест-игра Литературные доктора
Методическая разработка Тест-игра Литературные доктора А. Блок, поэма Двенадцать (1918)
А. Блок, поэма Двенадцать (1918)