Слайд 2

Стандарты GMP базируются на необходимости устранения негативных моментов в производственном процессе,
в результате учета тех факторов, которые могут нанести ущерб готовой продукции. Так как, наше государство динамично интегририруется в мировую систему, то и производственники вынуждены переходить на международные правила и принципы.
Слайд 3

Каждое фармпроизводство имеет свои отличительные особенности. Это связано с выпускаемой номенклатурой
лекарственных препаратов, особенностью проекта производства, Устава и Политики предприятия, его структуры, специфических особенностей выпускаемой продукции
Слайд 4

В РГП «Научном центре противоинфекционных препаратов» идет активная работа по внедрению
международных требовании GMP, на базе опытного производства разработаны такие методические рекомендации, как:
– Проведение валидационных процессов в производстве лекарственных средств по системе GMP;
-Совершенствование нормативной базы, видов и процессов производства лекарственных средств при внедрении систем GMP и GLP;
-Интеграция систем СТ РК ИСО 9001-2009, 13485:2003, ИСО/МЭК 17025-2007 в стандарты GMP, GLP, GСP, GDP, GРP;
-Разработка документов по стандартам GMP для производства лекарственных средств;
-Особенности складской зоны производства согласно требованиям GMP.
Слайд 5

При составлении данных рекомендации, были учтены и отражены все позитивные моменты
наработанные в научном центре. Кроме того, составлены СОПы, идут валидационные процессы, разрабатываются необходимые другие документы и т.д.
Разработанные рекомендации, которые можно использовать как вспомогательную литературу, доступны для всех желающих субъектов фармацевтического рынка.




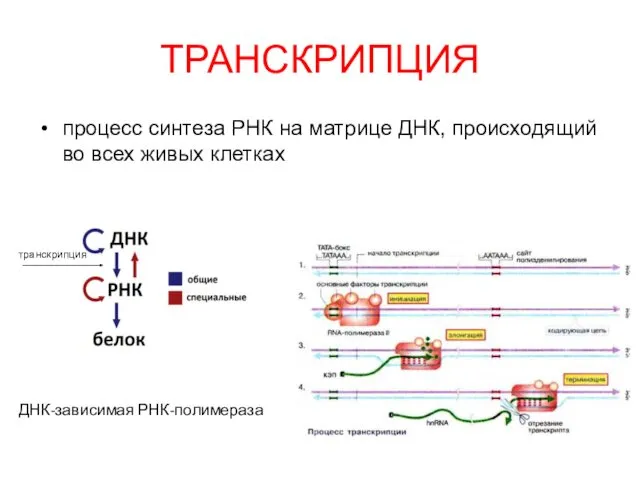 Транскрипция, процессинг
Транскрипция, процессинг Рефлексия на уроке
Рефлексия на уроке Просветительская деятельность учителя-логопеда в МДОУ Детский сад №3 Дюймовочка
Просветительская деятельность учителя-логопеда в МДОУ Детский сад №3 Дюймовочка Работа. Мехническая энергия. Кинетическая и потенциальная энергия. Закон сохранения механической энергии
Работа. Мехническая энергия. Кинетическая и потенциальная энергия. Закон сохранения механической энергии Анализ работы городского методического объединения учителей-логопедов г. Троицка за 2013-2014 учебный год
Анализ работы городского методического объединения учителей-логопедов г. Троицка за 2013-2014 учебный год Формы глагола Be в настоящем простом времени. GRAMMAR
Формы глагола Be в настоящем простом времени. GRAMMAR Геометрические приложения определенного интеграла
Геометрические приложения определенного интеграла Презентация к занятию Я люблю шоколад, а полезен ли он
Презентация к занятию Я люблю шоколад, а полезен ли он Семинар по неорганической химии: Комплексные соединения. Качественный анализ
Семинар по неорганической химии: Комплексные соединения. Качественный анализ Обережно - сказ
Обережно - сказ Компьютерная графика
Компьютерная графика Экономическое развитие России при Петре I
Экономическое развитие России при Петре I Страна вежливости и доброты
Страна вежливости и доброты Эпоха Возрождения - позднее европейское средневековье
Эпоха Возрождения - позднее европейское средневековье Места названые в честь В.Шекспира
Места названые в честь В.Шекспира Основы электроники
Основы электроники Золотодобывающая промышленность
Золотодобывающая промышленность Эксплуатация штатных образцов ВВСТ (артиллерийского вооружения)
Эксплуатация штатных образцов ВВСТ (артиллерийского вооружения) Экологическое право
Экологическое право Мировая религия пастафарианство
Мировая религия пастафарианство Muhammad and the sources
Muhammad and the sources Социальное партнёрство с родителями, как условие развития творческих способностей обучающихся
Социальное партнёрство с родителями, как условие развития творческих способностей обучающихся  Программа классного руководителя Мир начинается с меня
Программа классного руководителя Мир начинается с меня Названия чисел в записях действий. числовые выражения
Названия чисел в записях действий. числовые выражения Виды торговых помещений
Виды торговых помещений Уравнение. 5 класс
Уравнение. 5 класс Натрий (Na)
Натрий (Na) О рассмотрении паспорта проекта Модернизация ТГ-6 с заменой проточной части цилиндра среднего давления (ЦСД)
О рассмотрении паспорта проекта Модернизация ТГ-6 с заменой проточной части цилиндра среднего давления (ЦСД)