Содержание
- 2. План лекции Жидкометаллические аккумуляторы Натрий-серный Натрий-хлоридный Магний-сурьмяной Проточные аккумуляторы Редокс-аккумуляторы Гибридные аккумуляторы Козадеров О.А. 2015
- 3. Проблема стабильности энергообеспечения Козадеров О.А. 2015
- 4. 8.1. Жидкометаллические аккумуляторы Козадеров О.А. 2015
- 5. Натрий-серный аккумулятор Схема Электрохимическая ячейка (–) Na | β-Al2O3 | S (+) Анод: расплав натрия (tпл
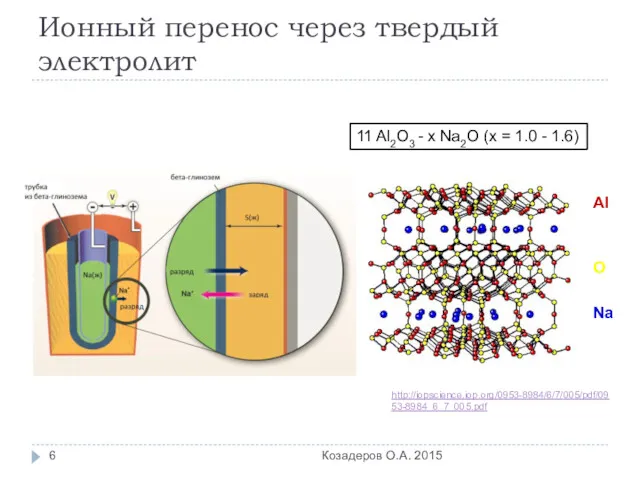
- 6. Ионный перенос через твердый электролит Козадеров О.А. 2015 11 Al2O3 - x Na2O (x = 1.0
- 7. Электродные процессы (–) Na (ж) = Na+ (сепаратор) + e– (+) 2Na+ (сепаратор) + 5S (ж)
- 8. Дополнительная токообразующая реакция Козадеров О.А. 2015 После формирования Na2S3 разряд аккумулятора следует прекратить, так как если
- 9. Аккумулятор ZEBRA (ZEolite Battery Research Africa) Устройство Электрохимическая ячейка (–) Na | β-Al2O3 | NaAlCl4, NiCl2,
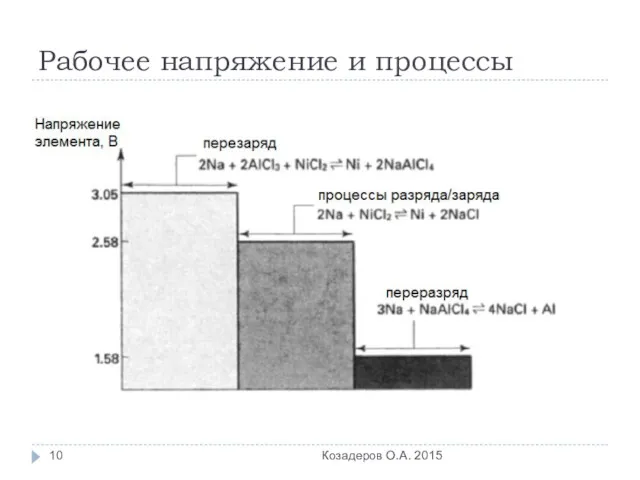
- 10. Рабочее напряжение и процессы Козадеров О.А. 2015
- 11. Жидкометаллический магний-сурьмяной аккумулятор Видео http://www.ted.com/talks/donald_sadoway_the_missing_link_to_renewable_energy?language=ru Козадеров О.А. 2015
- 12. Жидкометаллический магний-сурьмяной аккумулятор: опытный образец Козадеров О.А. 2015 dx.doi.org/10.1021/ja209759s | J. Am. Chem.Soc. 2012, 134, 1895−1897
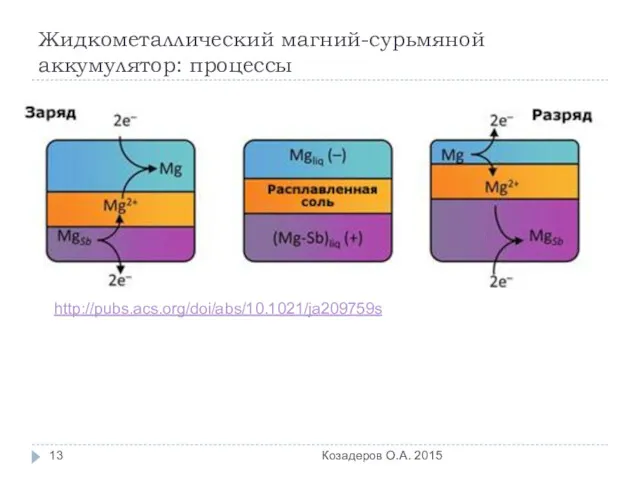
- 13. Жидкометаллический магний-сурьмяной аккумулятор: процессы Козадеров О.А. 2015 http://pubs.acs.org/doi/abs/10.1021/ja209759s
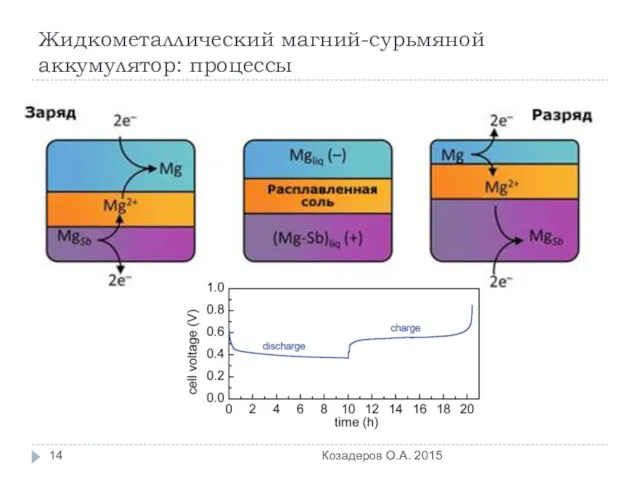
- 14. Жидкометаллический магний-сурьмяной аккумулятор: процессы Козадеров О.А. 2015
- 15. 8.2. Проточные аккумуляторы Козадеров О.А. 2015
- 16. Проточный аккумулятор это электрохимическое устройство, которое преобразует химическую энергию электрохимически активных веществ непосредственно в электрическую энергию,
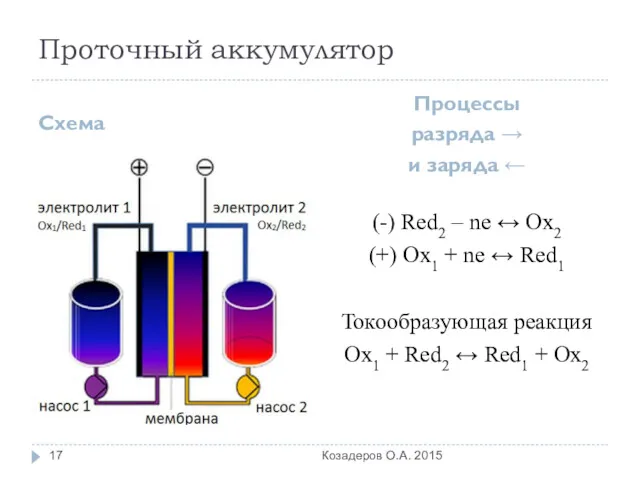
- 17. Проточный аккумулятор Схема Процессы разряда → и заряда ← (-) Red2 – ne ↔ Ox2 (+)
- 18. Типы проточных аккумуляторов Редокс-аккумулятор Гибридный аккумулятор система, в которой все электрохимически активные вещества растворены в жидком
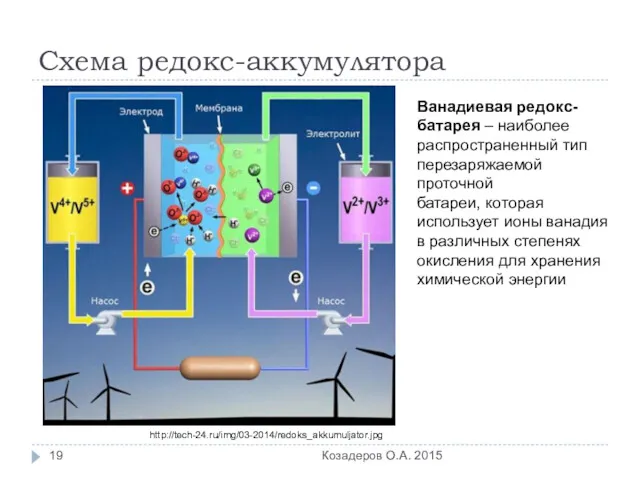
- 19. Схема редокс-аккумулятора Козадеров О.А. 2015 http://tech-24.ru/img/03-2014/redoks_akkumuljator.jpg Ванадиевая редокс-батарея – наиболее распространенный тип перезаряжаемой проточной батареи, которая
- 20. Ванадиевый редокс-аккумулятор: процессы Козадеров О.А. 2015
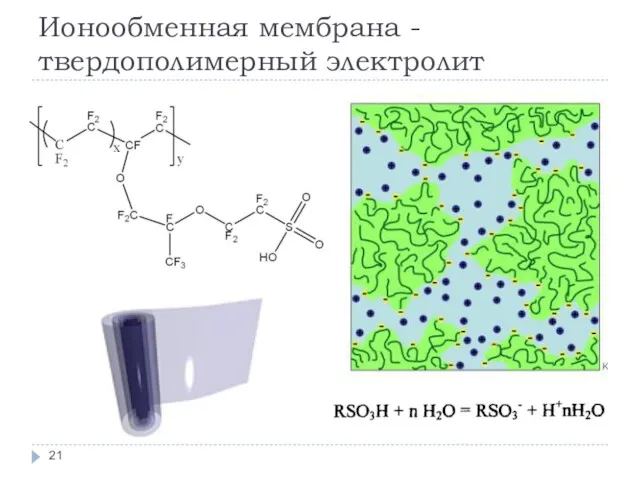
- 21. Ионообменная мембрана - твердополимерный электролит
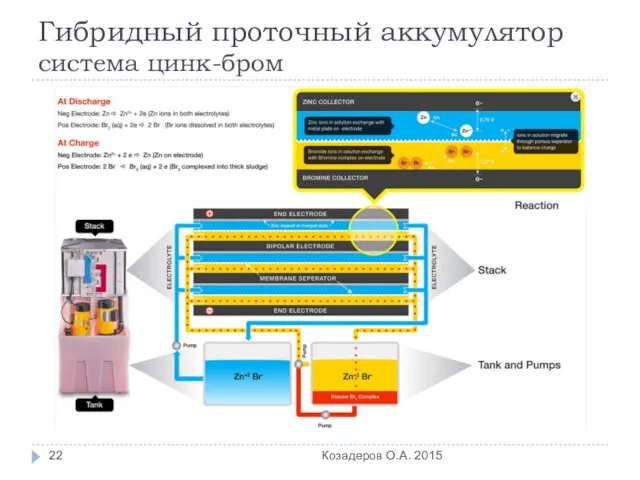
- 22. Гибридный проточный аккумулятор система цинк-бром Козадеров О.А. 2015
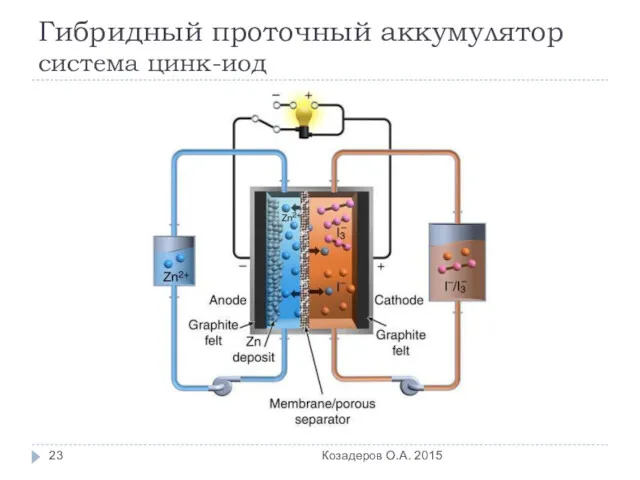
- 23. Гибридный проточный аккумулятор система цинк-иод Козадеров О.А. 2015
- 25. Скачать презентацию













 Построение теней при центральном проецировании
Построение теней при центральном проецировании Презентация-отчет по учебной практике
Презентация-отчет по учебной практике Развитие средств связи
Развитие средств связи Ракетные двигатели, их значимость, устройство и принцип работы
Ракетные двигатели, их значимость, устройство и принцип работы Реле направления мощности
Реле направления мощности Колебания-1. Гармоническое колебание и его характеристики. Модель гармонического осциллятора
Колебания-1. Гармоническое колебание и его характеристики. Модель гармонического осциллятора Строение ядра атома. Изотопы
Строение ядра атома. Изотопы Конвективный теплообмен в однофазных средах
Конвективный теплообмен в однофазных средах 9 кл - Физический диктант Механические колебания
9 кл - Физический диктант Механические колебания Глицерин
Глицерин Организация технического обслуживания и ремонт автомобиля Iveco Stralis AT440S40 T/P
Организация технического обслуживания и ремонт автомобиля Iveco Stralis AT440S40 T/P Захватные устройства
Захватные устройства Физика мультфильмов
Физика мультфильмов Electrical Communication ELC318
Electrical Communication ELC318 Кристалдану үдерісі
Кристалдану үдерісі Лабораторная работа Наблюдение сплошного и линейчатых спектров. 11 класс
Лабораторная работа Наблюдение сплошного и линейчатых спектров. 11 класс Инфракрасная спектроскопия
Инфракрасная спектроскопия Почему корабль может плавать а камень тонет?
Почему корабль может плавать а камень тонет? Властивості електромагнітних хвиль
Властивості електромагнітних хвиль презентация Обнаружение магнитного поля по его действию на электрический ток
презентация Обнаружение магнитного поля по его действию на электрический ток Электромагнитная обстановка на объектах электроэнергетики
Электромагнитная обстановка на объектах электроэнергетики Sensors and actuators
Sensors and actuators Потенциал. Работа электростатического поля
Потенциал. Работа электростатического поля Кинематические характеристики движения точки
Кинематические характеристики движения точки ТО и ТР приборов облегчения пуска двигателя
ТО и ТР приборов облегчения пуска двигателя Измерение атмосферного давления. 7 класс
Измерение атмосферного давления. 7 класс Тепловые двигатели
Тепловые двигатели Основные законы магнитного поля: теорема Гаусса и теорема о циркуляции индукции магнитного поля
Основные законы магнитного поля: теорема Гаусса и теорема о циркуляции индукции магнитного поля