Содержание
- 2. Электрический аккумулятор — источник тока многоразового действия, основная специфика которого заключается в обратимости внутренних химических процессов,
- 3. Температурный режим- берегите аккумуляторы от огня и воды, чрезмерного нагревания (охлаждения), резких перепадов температур. Не используйте
- 4. Принцип действия Основные принципы действия химических источников электрического тока были открыты еще в конце 18 века,
- 5. Типы аккумуляторов Электрические и эксплуатационные характеристики аккумулятора зависят от материала электродов и состава электролита. Сейчас наиболее
- 9. Скачать презентацию
Электрический аккумулятор — источник тока многоразового действия, основная специфика которого заключается в обратимости
Электрический аккумулятор — источник тока многоразового действия, основная специфика которого заключается в обратимости
Характеристики
Ёмкость аккумулятора- максимально возможный полезный заряд аккумулятора называется зарядной ёмкостью, или просто ёмкостью. Ёмкость аккумулятора — это заряд, отдаваемый полностью заряженным аккумулятором при разряде до наименьшего допустимого напряжения. В системе СИ ёмкость аккумуляторов измеряют в кулонах, на практике часто используется внесистемная единица — ампер-час. 1 А⋅ч = 3600 Кл.
Плотность энергии — количество энергии на единицу объёма или единицу веса аккумулятора.
Саморазряд- это потеря аккумулятором ёмкости после полной зарядки при отсутствии нагрузки. Саморазряд проявляется по-разному у разных типов аккумуляторов, но всегда максимален в первые часы после заряда, а после замедляется.
Температурный режим- берегите аккумуляторы от огня и воды, чрезмерного нагревания (охлаждения),
Температурный режим- берегите аккумуляторы от огня и воды, чрезмерного нагревания (охлаждения),
Срок службы аккумуляторов - неправильно определять срок службы аккумуляторов в годах или месяцах. Срок службы батареи определяется числом циклов заряд-разряд и значительно зависит от условий ее эксплуатации. Чем глубже разряжается батарея, чем большее время она находится в разряженном состоянии, тем меньшее число возможных циклов работы.
Срок хранения - максимальный период времени, в течение которого батарея может храниться при оговоренных условиях, не требуя дополнительной зарядки.
Принцип действия
Основные принципы действия химических источников электрического тока были открыты
Принцип действия
Основные принципы действия химических источников электрического тока были открыты
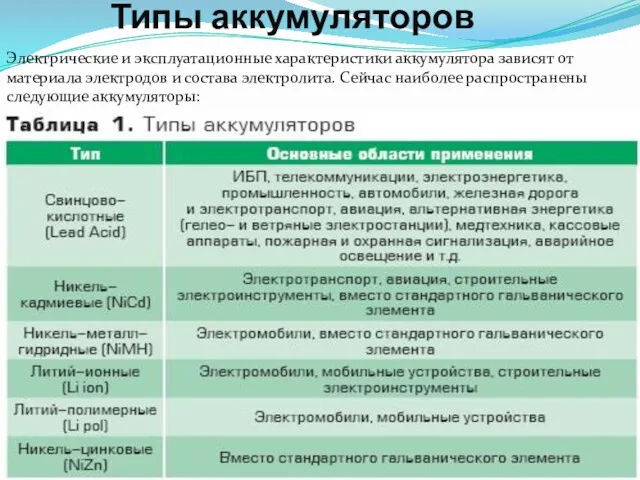
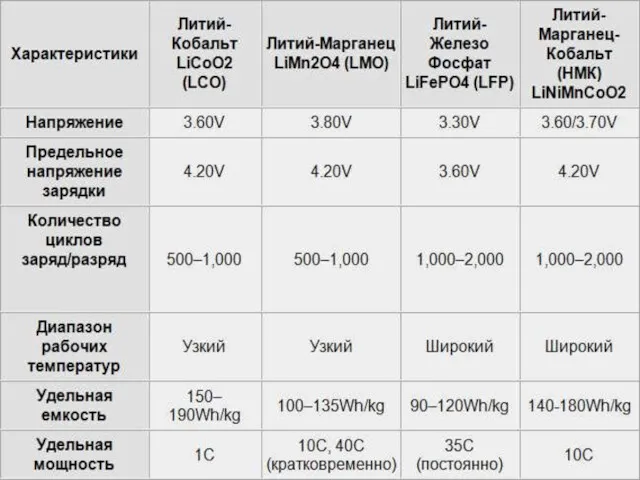
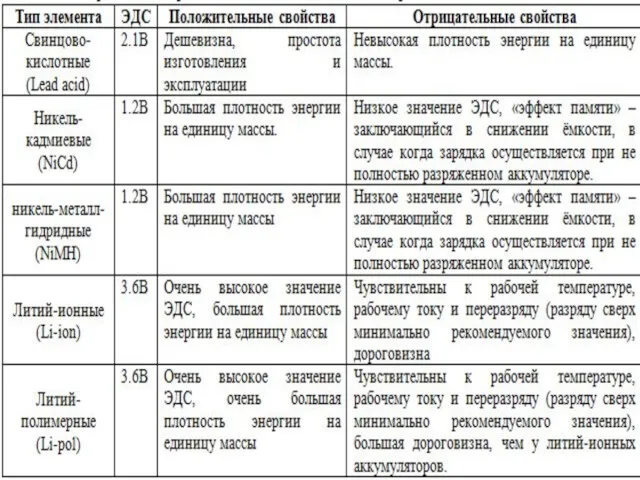
Типы аккумуляторов
Электрические и эксплуатационные характеристики аккумулятора зависят от материала электродов
Типы аккумуляторов
Электрические и эксплуатационные характеристики аккумулятора зависят от материала электродов



 Условия плавания тел
Условия плавания тел презентация Генератор переменного тока
презентация Генератор переменного тока Теплопередача, или теплообмен
Теплопередача, или теплообмен КВН по физике
КВН по физике Как составить программу элективного курса
Как составить программу элективного курса Работа и мощность электрического тока. Решение задач. Физика. 8 класс
Работа и мощность электрического тока. Решение задач. Физика. 8 класс Коррозия металлов
Коррозия металлов Звук. Автор Максимова Наталья Сергеевна
Звук. Автор Максимова Наталья Сергеевна Кинетическая теория равновесного идеального газа. Термодинамика идеального газа. Лекция 2
Кинетическая теория равновесного идеального газа. Термодинамика идеального газа. Лекция 2 Експлуатація навчального вертольота. Експлуатація гідравлічної і пневматичної систем в польоті
Експлуатація навчального вертольота. Експлуатація гідравлічної і пневматичної систем в польоті Динамика. Задачи
Динамика. Задачи Выбор оборудования для участка подготовки, кузовного ремонта и покраски легковых автомобилей
Выбор оборудования для участка подготовки, кузовного ремонта и покраски легковых автомобилей Вспомогательные устройства гидросистем. (Лекция 13-14)
Вспомогательные устройства гидросистем. (Лекция 13-14) Сұйық біртексіз жүйелерді бөлу
Сұйық біртексіз жүйелерді бөлу Электрический ток в металлах и электролитах. Законы Фарадея
Электрический ток в металлах и электролитах. Законы Фарадея Презентация к уроку физики в 8 классе на тему: Кипение
Презентация к уроку физики в 8 классе на тему: Кипение Створення телеграфу та винайдення телефону
Створення телеграфу та винайдення телефону Масса өтудің модифицирленген теңдеуі
Масса өтудің модифицирленген теңдеуі Частотные характеристики линейных стационарных автоматических систем. Тема 4
Частотные характеристики линейных стационарных автоматических систем. Тема 4 Экологическое воспитание на уроках физики
Экологическое воспитание на уроках физики Электромагнитные колебания. Закрытый колебательный контур
Электромагнитные колебания. Закрытый колебательный контур КПД двигателя внутреннего сгорания
КПД двигателя внутреннего сгорания Параллельное и последовательное соединение проводников
Параллельное и последовательное соединение проводников Преломление света
Преломление света Электор жабдықтау жүиесі,оталдыру және іске қосу жүиесі
Электор жабдықтау жүиесі,оталдыру және іске қосу жүиесі Робот-исследователь, способный измерять некоторые физические факторы среды
Робот-исследователь, способный измерять некоторые физические факторы среды Высота. Тембр и громкость звука
Высота. Тембр и громкость звука Импульс тела, импульс силы, теорема об изменении импульса
Импульс тела, импульс силы, теорема об изменении импульса