Содержание
- 2. Изопроцессы в газах Процессы, протекающие при неизменном значении одного из параметров, называют изопроцессами. Рассмотрим следующие изопроцессы:
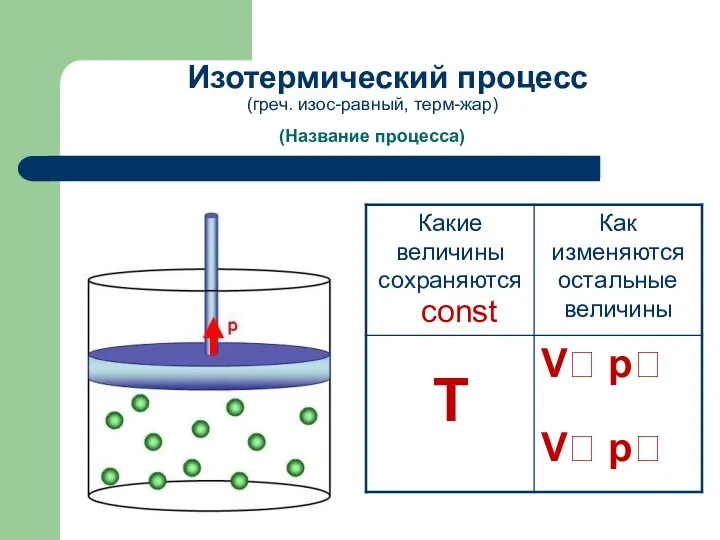
- 3. (Название процесса) Изотермический процесс T const V? p? V? p? (греч. изос-равный, терм-жар)
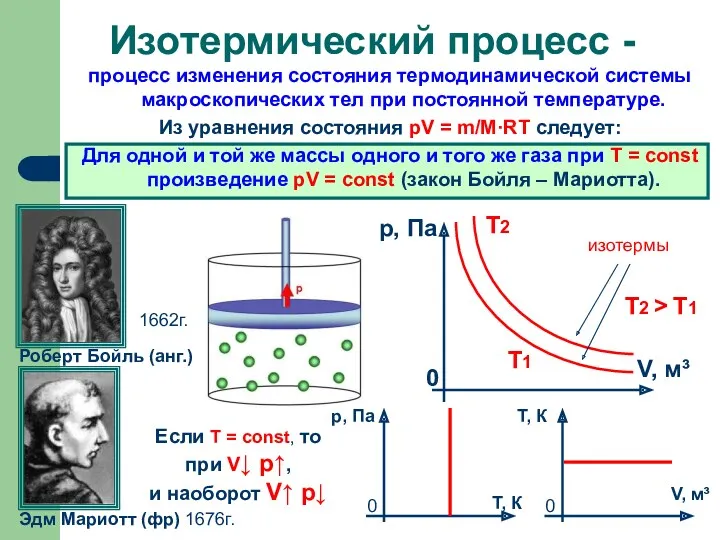
- 4. процесс изменения состояния термодинамической системы макроскопических тел при постоянной температуре. Из уравнения состояния pV = m/M·RT
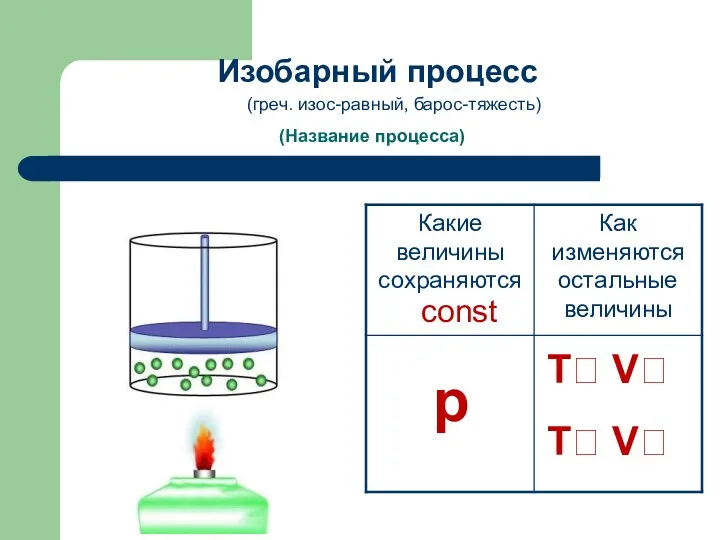
- 5. (Название процесса) Изобарный процесс const p T? V? T? V? (греч. изос-равный, барос-тяжесть)
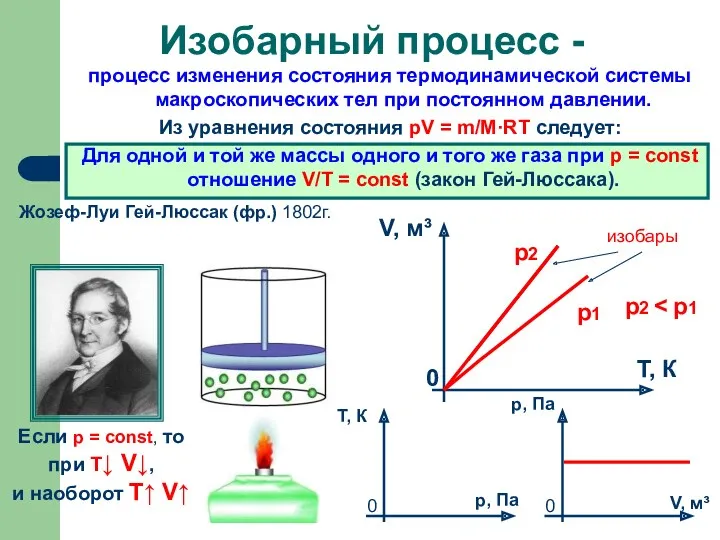
- 6. процесс изменения состояния термодинамической системы макроскопических тел при постоянном давлении. Из уравнения состояния pV = m/M·RT
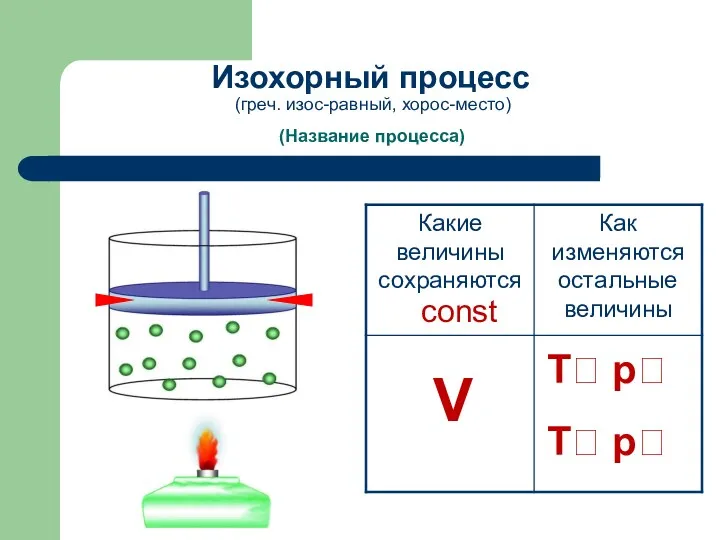
- 7. (Название процесса) Изохорный процесс (греч. изос-равный, хорос-место) const V T? p? T? p?
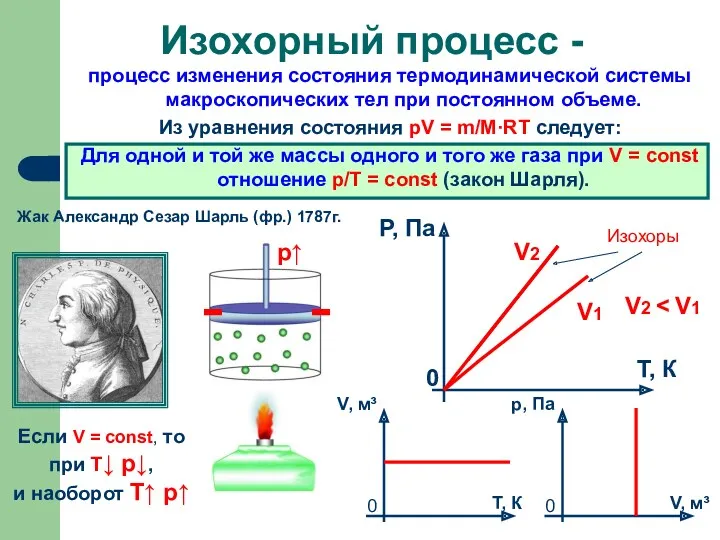
- 8. процесс изменения состояния термодинамической системы макроскопических тел при постоянном объеме. Из уравнения состояния pV = m/M·RT
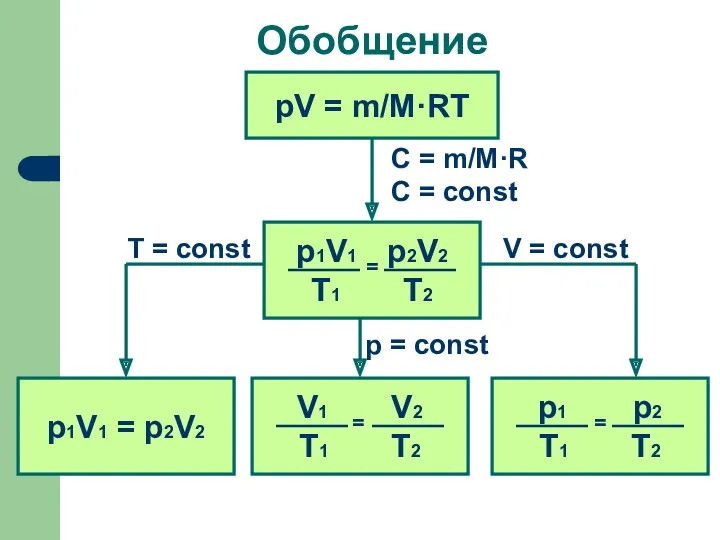
- 9. Обобщение pV = m/M·RT C = m/M·R C = const p1V1 = p2V2 V = const
- 10. Повторение Перечислите основные положения МКТ. Дайте определение относительной молекулярной массы. Что такое количество вещества? Что такое
- 11. ДЕМО_2016_9 1
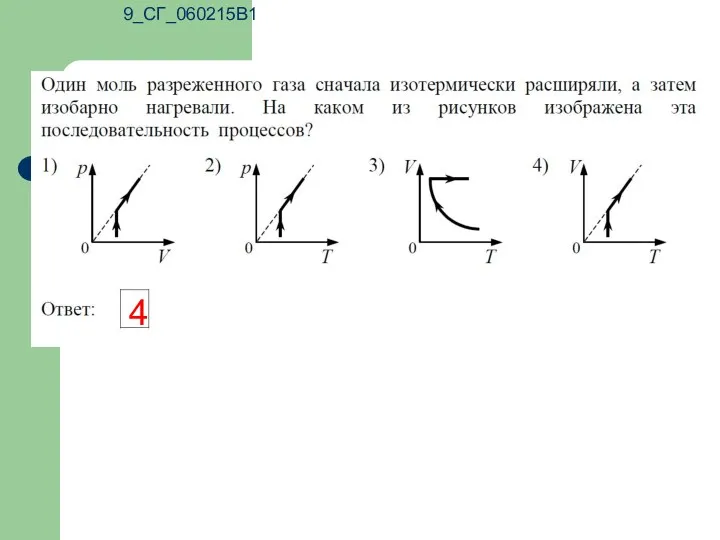
- 12. 9_СГ_060215В1 4
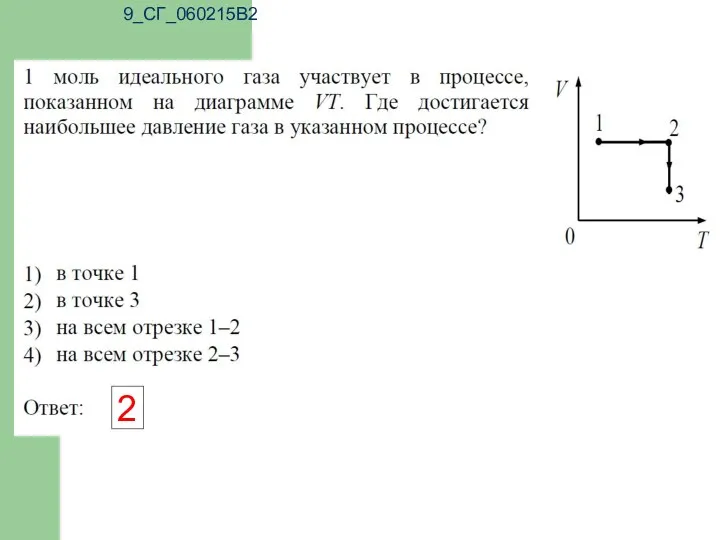
- 13. 9_СГ_060215В2 2
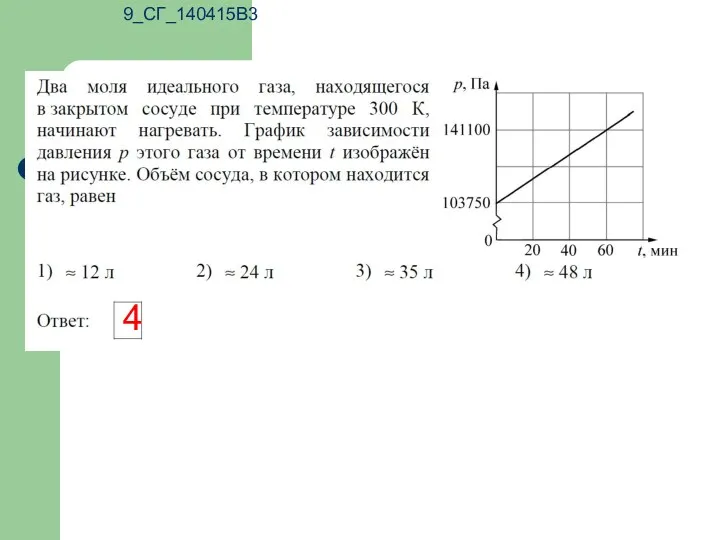
- 14. 9_СГ_140415В3 4
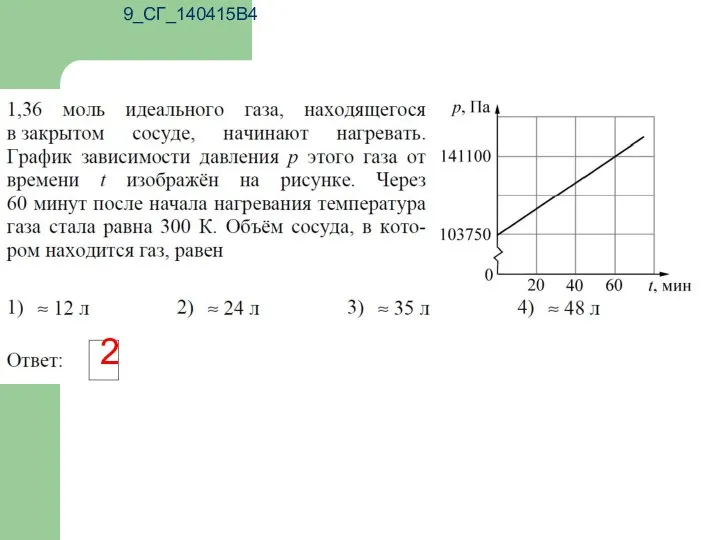
- 15. 9_СГ_140415В4 2
- 16. 12_СГ_120515В1 1 3
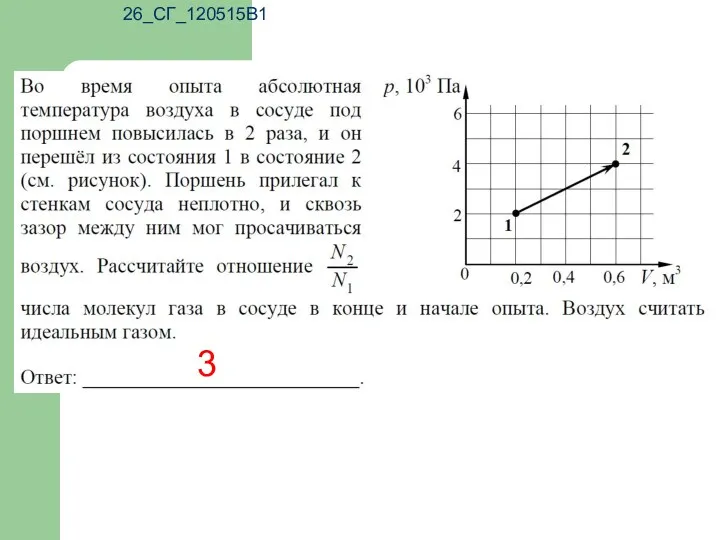
- 17. 26_СГ_120515В1 3
- 18. 9_СГ_120515В2 1
- 19. 11_СГ_211215В3 2 3
- 20. 11_СГ_211215В4 3 3
- 21. 28_СГ_060215В1
- 22. 30_СГ_211215В3 30_СГ_211215В4
- 25. Скачать презентацию










 Основные параметры эхо-метода
Основные параметры эхо-метода Физические основы механики. Кинематика материальной точки
Физические основы механики. Кинематика материальной точки Современные автомобили и двигатели
Современные автомобили и двигатели Машина и ее основные части
Машина и ее основные части Лекция №7 (7). Электромагнитные волны в различных средах
Лекция №7 (7). Электромагнитные волны в различных средах yadernaya_fizika (1)
yadernaya_fizika (1) Средства измерения уровня
Средства измерения уровня Законы сохранения
Законы сохранения Basic principles of ultrasonic testing
Basic principles of ultrasonic testing Жаңбырлатқыш машиналар қондырғылар
Жаңбырлатқыш машиналар қондырғылар Определение твёрдости металлов и сплавов
Определение твёрдости металлов и сплавов Открытие нейтрона
Открытие нейтрона Презентация к уроку по теме Сила тяжести
Презентация к уроку по теме Сила тяжести Магнитное поле
Магнитное поле Напряженность электрического поля. Принцип суперпозиции полей
Напряженность электрического поля. Принцип суперпозиции полей Звуковые явления. Эхо
Звуковые явления. Эхо Электрическое напряжение. Единицы напряжения. Вольтметр
Электрическое напряжение. Единицы напряжения. Вольтметр Магнитное поле в веществе. Система уравнений Максвелла. Тема 18
Магнитное поле в веществе. Система уравнений Максвелла. Тема 18 Презентация Современный урок
Презентация Современный урок Урок физики в 9 классе Колебательное движение.
Урок физики в 9 классе Колебательное движение. Модуляция и детектирование
Модуляция и детектирование Фізичні та хімічні властивості води
Фізичні та хімічні властивості води Intelligent energy storage
Intelligent energy storage Ультразвуковой контроль
Ультразвуковой контроль Renewable power
Renewable power Звуковая волна
Звуковая волна Направление тока и направление линий его магнитного поля. (Урок 40)
Направление тока и направление линий его магнитного поля. (Урок 40) Механика и свойства жидкостей. (Лекция 3)
Механика и свойства жидкостей. (Лекция 3)