Содержание
- 2. Фредерик Содди 1877 - 1956 Эрнест Резерфорд 1871–1937 В 1903 г. обнаружили, что радий превращается в
- 3. Обозначение ядер химических элементов - Зарядовое число - Номер химического элемента - Заряд ядра в элементарных
- 4. Обозначение ядер химических элементов и частиц Ядра химических элементов: Частицы:
- 5. Правила смещения А) Альфа – распад: зарядовое число (порядковый номер) элемента уменьшается на две единицы, а
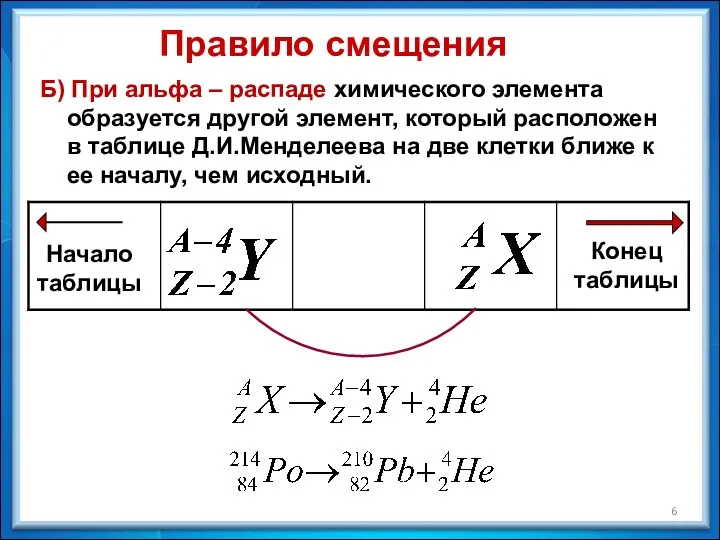
- 6. Б) При альфа – распаде химического элемента образуется другой элемент, который расположен в таблице Д.И.Менделеева на
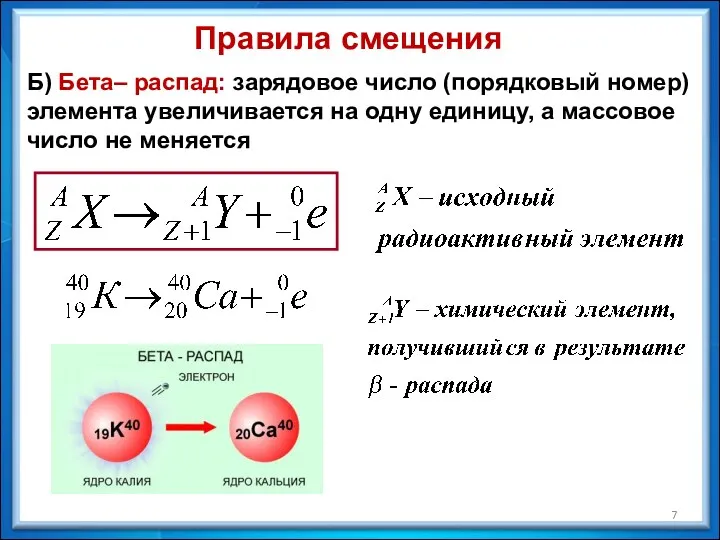
- 7. Правила смещения Б) Бета– распад: зарядовое число (порядковый номер) элемента увеличивается на одну единицу, а массовое
- 8. Правило смещения Б) При бета – распаде одного химического элемента образуется другой элемент, который расположен в
- 9. Законы сохранения массового числа и заряда при радиоактивных превращениях
- 10. Фредерик Содди 1877 - 1956 Эрнест Резерфорд 1871–1937 Открытие радиоактивных превращений атомных ядер 5. Вывод: ядра
- 11. Упражнения 1) Пользуясь законами сохранения массового числа и заряда, определить массовое число и зарядовое число химического
- 12. Упражнения 2. В результате какого радиоактивного распада натрий-22 превращается в магний – 22?
- 13. 3. Кобальт-60 используется в медицине для лечения и терапии злокачественных образований и воспалительных процессов. Кобальт-60 бета-радиоактивен.
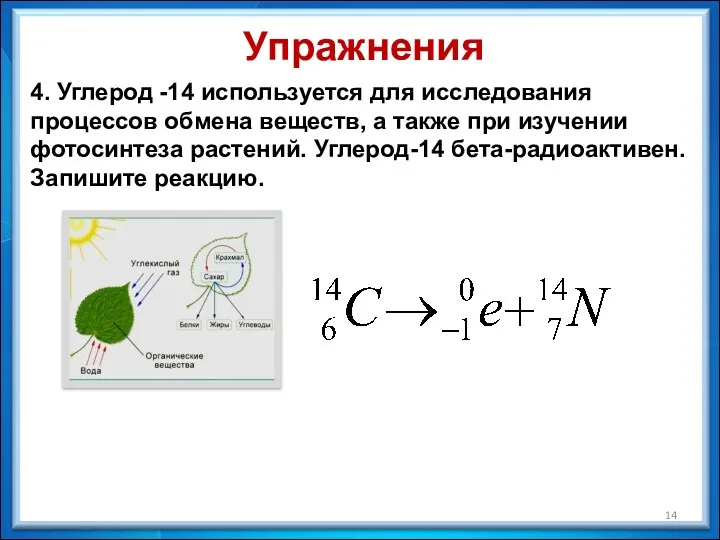
- 14. 4. Углерод -14 используется для исследования процессов обмена веществ, а также при изучении фотосинтеза растений. Углерод-14
- 15. 5. Какие заряд Z и массовое число А будет иметь ядро элемента, получившегося из ядра изотопа
- 16. Д.з. § 67, Упр. 51(письм), Р. № 1198 Радиоактивные превращения атомных ядер
- 18. Скачать презентацию











 Дослідження режимів роботи рентгенівських апаратів
Дослідження режимів роботи рентгенівських апаратів Презентация к уроку физики в 8 классе на тему Звуковые волны в различных средах
Презентация к уроку физики в 8 классе на тему Звуковые волны в различных средах Maintenance Level Training. TA 400 Tier 2/4 – Scania Engine
Maintenance Level Training. TA 400 Tier 2/4 – Scania Engine Презентация к уроку развивающего обучения Простые механизмы часть 2
Презентация к уроку развивающего обучения Простые механизмы часть 2 Термиялық өңдеу. Термиялық өңдеудің түрлері. Термиялық өңдеудің фазалық өзгерістері. Болаттын термиялық өңдеу
Термиялық өңдеу. Термиялық өңдеудің түрлері. Термиялық өңдеудің фазалық өзгерістері. Болаттын термиялық өңдеу Электр тоғы. Ток көздері. Ток күші. Амперметр
Электр тоғы. Ток көздері. Ток күші. Амперметр Электрический ток
Электрический ток Буксы. Общие сведения
Буксы. Общие сведения Разработка диаграмм управления пневматическими приводами
Разработка диаграмм управления пневматическими приводами Закон Паскаля, объясняющий процесс передачи давления жидкостями и газами
Закон Паскаля, объясняющий процесс передачи давления жидкостями и газами Кинематика роботов. Кинематические схемы. (Лекция 2.1)
Кинематика роботов. Кинематические схемы. (Лекция 2.1) Биохимические методы исследования в КДЛ
Биохимические методы исследования в КДЛ Термоэлектрический генератор на основе эффекта Зеебека
Термоэлектрический генератор на основе эффекта Зеебека Исследовательская работа по теме: Физика вокруг нас
Исследовательская работа по теме: Физика вокруг нас Плавание тел. Понятия о силе Архимеда
Плавание тел. Понятия о силе Архимеда Плотность. Формула измерения плотности
Плотность. Формула измерения плотности Презентация Свет,цвет и здоровье человека
Презентация Свет,цвет и здоровье человека Атомно-силовая микроскопия
Атомно-силовая микроскопия Что изучает физика? Урок в 7 классе
Что изучает физика? Урок в 7 классе Расчетный напор НС-2 при расположении башни в начале сети
Расчетный напор НС-2 при расположении башни в начале сети Система подготовки учащихся к ОГЭ по физике
Система подготовки учащихся к ОГЭ по физике Силы в природе. Понятие силы
Силы в природе. Понятие силы Сверлильный станок
Сверлильный станок Метрология. Шероховатость поверхности деталей
Метрология. Шероховатость поверхности деталей Колебания и волны
Колебания и волны Базирование по отверстиям под стыковые болты
Базирование по отверстиям под стыковые болты Явления переноса. Лекция № 16
Явления переноса. Лекция № 16 Ядерная гамма-резонансная спектроскопия
Ядерная гамма-резонансная спектроскопия