Содержание
- 2. Джозеф Джон ТОМСОН (1856-1940) выдающийся ученый, директор знаменитой Кавендишской лаборатории лауреат Нобелевской премии по физике (1906)
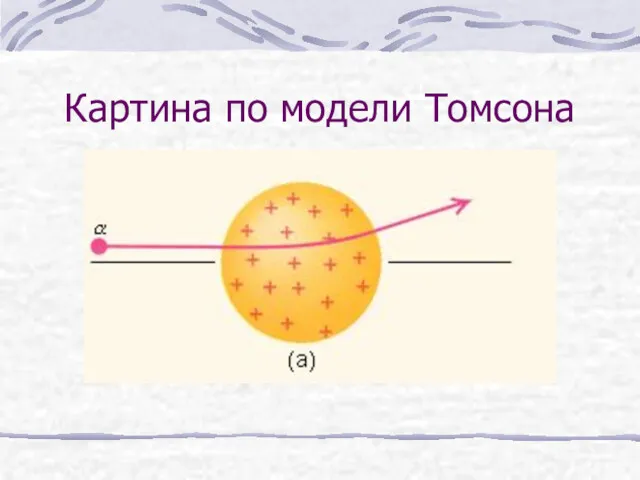
- 3. Картина по модели Томсона
- 4. Эрнест РЕЗЕРФОРД (1871-1937) выдающийся ученый, директор знаменитой Кавендишской лаборатории лауреат Нобелевской премии по химии (1908) в
- 5. Опыт Резерфорда Цель эксперимента: проверить гипотезу Дж. Томсона на опыте. 1911
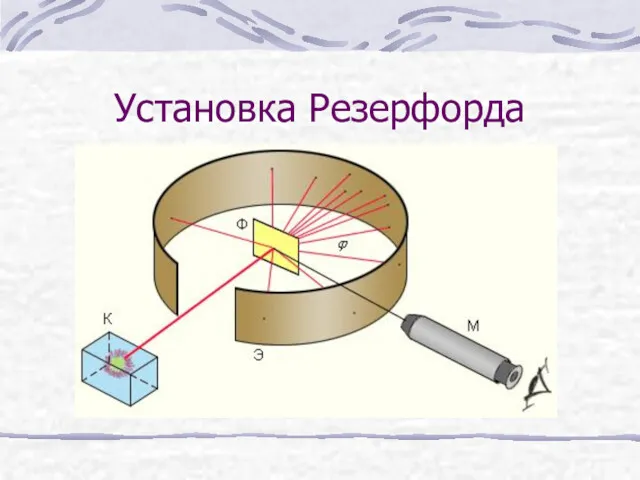
- 6. Установка Резерфорда
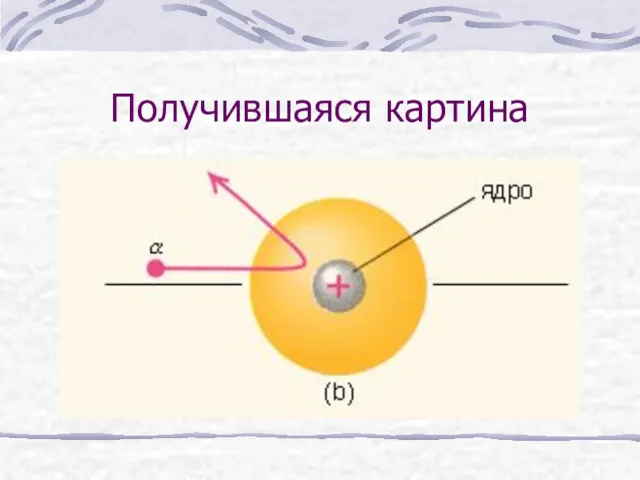
- 7. Получившаяся картина
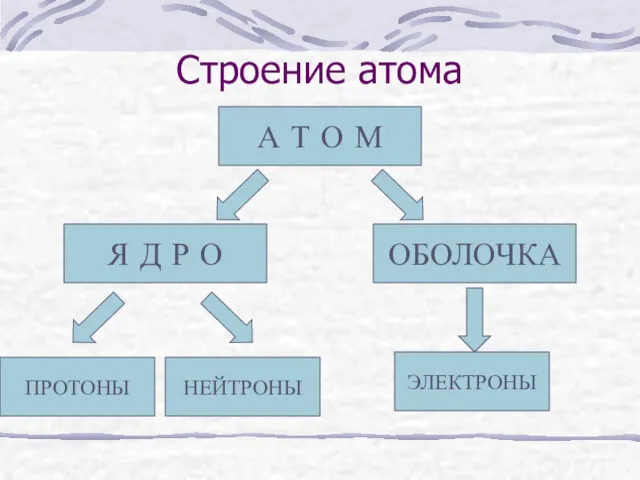
- 8. Строение атома А Т О М Я Д Р О ОБОЛОЧКА ПРОТОНЫ НЕЙТРОНЫ ЭЛЕКТРОНЫ
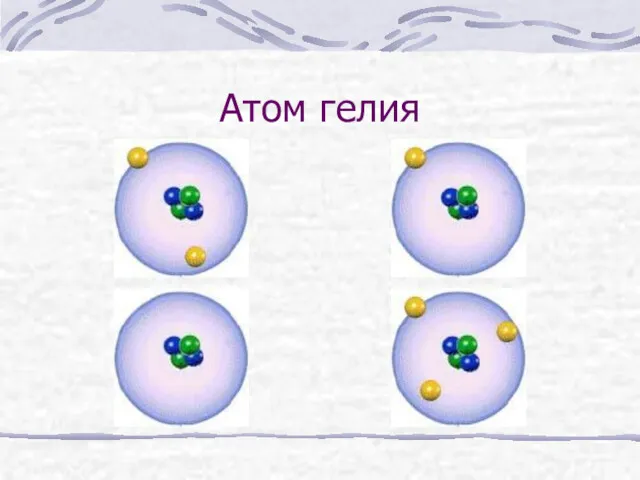
- 9. Атом гелия
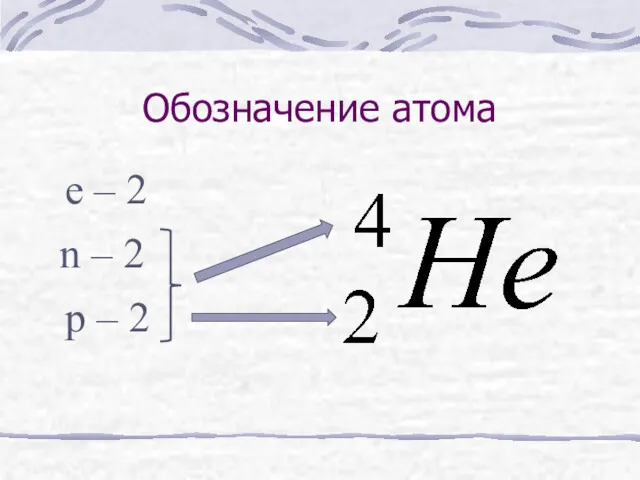
- 10. Обозначение атома e – 2 n – 2 p – 2
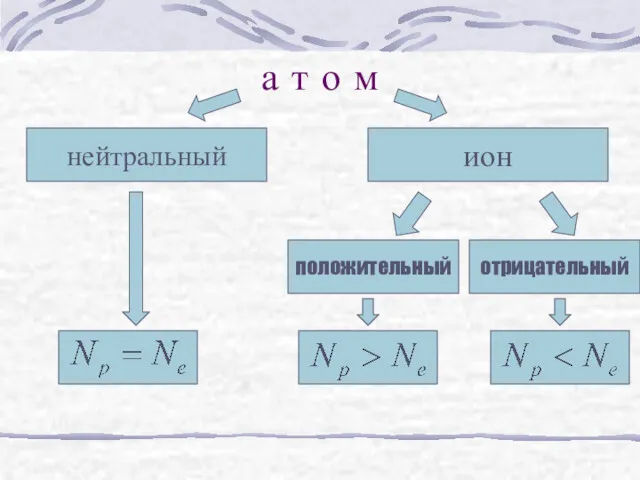
- 11. а т о м нейтральный ион положительный отрицательный
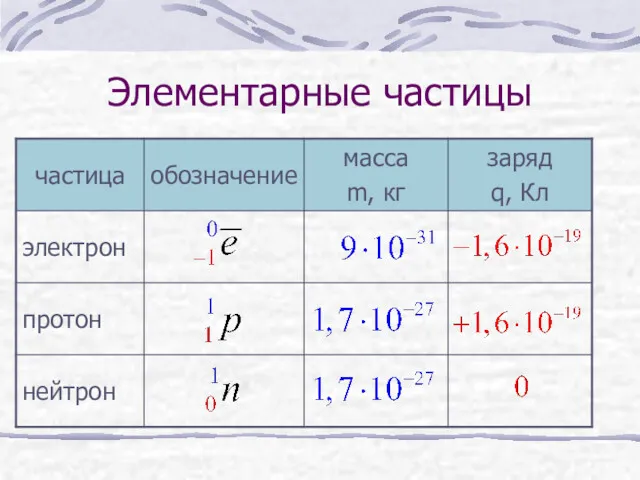
- 12. Элементарные частицы
- 13. Может ли атом водорода лишиться заряда равного 1,5 заряда электрона? 1. Да 2. Нет
- 14. 2. Существуют ли атомные ядра с зарядом меньшим, чем у протона? 1. Да 2. Нет
- 15. 3. Какой заряд приобретает атом железа, если он потеряет один электрон? 1. Положительный 2. Отрицательный 3.
- 16. 4. Вокруг ядра атома кислорода движется 8 электронов. Сколько протонов в ядре? 1. 8 2. 4
- 17. 5. В ядре атома азота 14 частиц, из них 7 нейтронов. Сколько протонов и электронов в
- 19. Скачать презентацию








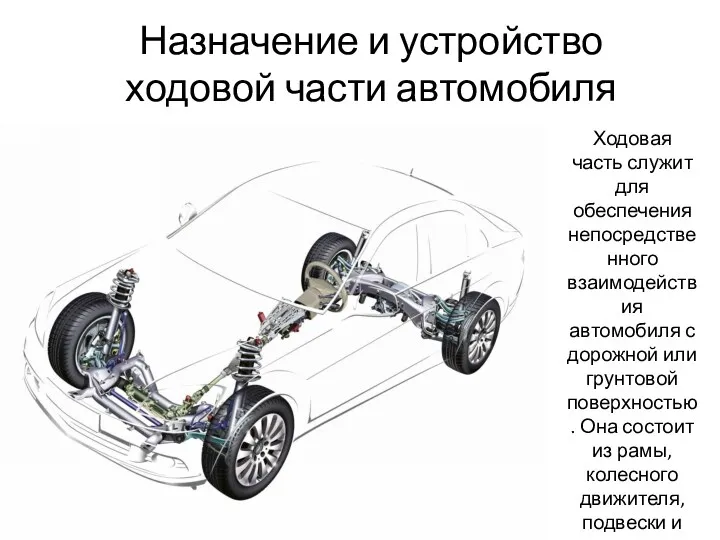 Назначение и устройство ходовой части автомобиля
Назначение и устройство ходовой части автомобиля Принцип неопределённости Гейзенберга 1927
Принцип неопределённости Гейзенберга 1927 Детали машин. Выполнение рабочих чертежей
Детали машин. Выполнение рабочих чертежей Обобщающий урок-игра по физике, 9 класс
Обобщающий урок-игра по физике, 9 класс Колебательное движение.
Колебательное движение. Переменный ток. Итоговый тест
Переменный ток. Итоговый тест Бытовая швейная машина
Бытовая швейная машина Танцующая монета
Танцующая монета Магнитное поле и его графическое изображение. Направление тока и направление линий его магнитного поля
Магнитное поле и его графическое изображение. Направление тока и направление линий его магнитного поля Темір жол жылжымалы құрам тежеуішінің принципиалды сұлбасы және тағайындалуы
Темір жол жылжымалы құрам тежеуішінің принципиалды сұлбасы және тағайындалуы Решение задач на ускорение (9 класс)
Решение задач на ускорение (9 класс) Аэродинамика и летно-технические данные вертолёта. Тема №1. Аэродинамические силы и их коэффициенты. Лекция №3
Аэродинамика и летно-технические данные вертолёта. Тема №1. Аэродинамические силы и их коэффициенты. Лекция №3 Идеальный газ. Основное уравнение МКТ идеального газа
Идеальный газ. Основное уравнение МКТ идеального газа Роз'ємні та нероз'ємні з'єднання
Роз'ємні та нероз'ємні з'єднання Bernoulli’s equation
Bernoulli’s equation Превращение энергии в колебательном движении. Гармонические колебания
Превращение энергии в колебательном движении. Гармонические колебания Квантова фізика
Квантова фізика Сила трения
Сила трения Gas Dynamics (Introduction to Compressible Flow) Lecture 6a and 6b
Gas Dynamics (Introduction to Compressible Flow) Lecture 6a and 6b Температура. Шкала Реомюра
Температура. Шкала Реомюра презентация Масса
презентация Масса Вплив теплових двигунів на навколишнє середовище
Вплив теплових двигунів на навколишнє середовище Рентгеновское излучение. Открытие рентгеновских лучей
Рентгеновское излучение. Открытие рентгеновских лучей Уравнения строительной механики. Вариационные принципы строительной механики
Уравнения строительной механики. Вариационные принципы строительной механики Презентация по физике 8 класс Зависимость силы тока от напряжения. Электрическое сопротивление
Презентация по физике 8 класс Зависимость силы тока от напряжения. Электрическое сопротивление Дисперсия света
Дисперсия света Нанотехнології в нашому житті. Загроза цивілізації, або стрибок у майбутнє
Нанотехнології в нашому житті. Загроза цивілізації, або стрибок у майбутнє Закон сохранения энергии. Работа и кинетическая энергия
Закон сохранения энергии. Работа и кинетическая энергия