Содержание
- 2. Пли́ний Ста́рший — древнеримский писатель – эрудит. Существует легенда о том, как к римскому императору Тиберию
- 3. Наполеон ІІІ В XIX веке на императорских приёмах -------- посуда была самой престижной. Наполеон III устроил
- 4. Д.И Менделеев В период открытия этого металла он был дороже золота. Англичане, решив почтить богатым подарком
- 5. Из глины я обыкновенной, Но я на редкость современный. Я не боюсь электротока, Бесстрашно в воздухе
- 6. «Этому металлу суждено великое будущее». Чернышевский Н. Г. Он важен, это - несомненно. Он нужен нам
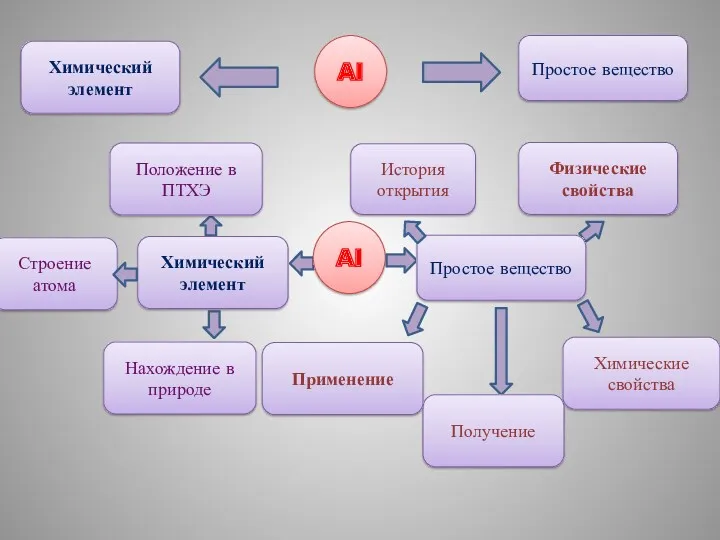
- 7. Химический элемент Al Простое вещество Al Химический элемент Положение в ПТХЭ Строение атома Нахождение в природе
- 8. Алюминий - химический элемент положение в периодической системе и строение атома 1. Химический знак (металл или
- 9. Al (металл) Ar= 27 13 III Нечётный III А (главная) Алюминий - химический элемент положение в
- 10. Алюминий - строение атома Al 27 +13 0 2 8 3 P = 13 e =
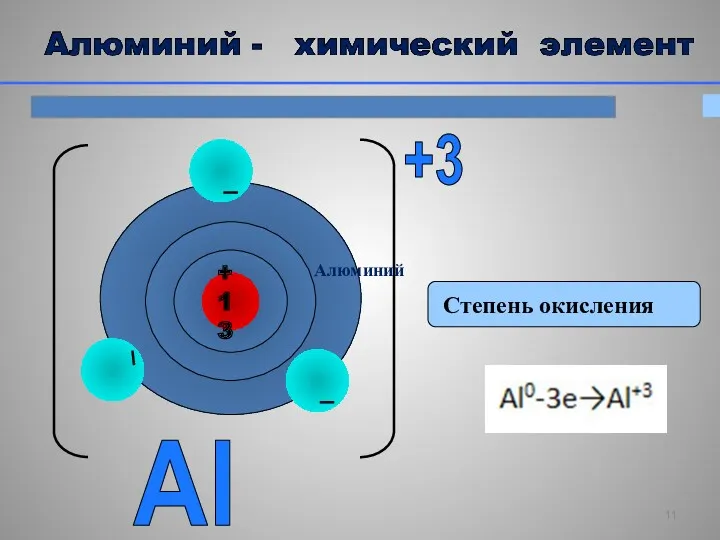
- 11. Степень окисления Al +3 Алюминий
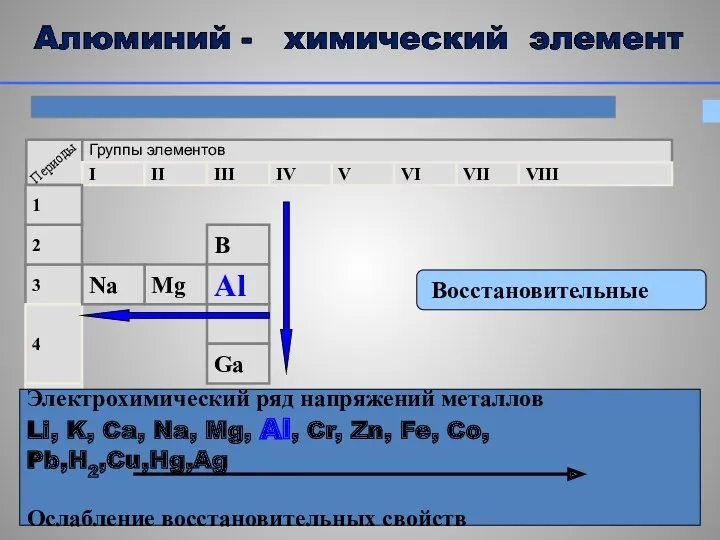
- 12. Восстановительные Электрохимический ряд напряжений металлов Li, K, Ca, Na, Mg, Al, Cr, Zn, Fe, Co, Pb,H2,Cu,Hg,Ag
- 13. Металлические Mg>Al 3 13 ē нет 3 +13
- 14. Строительство Алюминий и его сплавы применяются в промышленном и гражданском строительстве при изготовления каркасов зданий, ферм,
- 15. АЛЮМИНИЙ В РАКЕТНОМ ТОПЛИВЕ. При сгорании алюминия в кислороде и фторе выделяется много тепла. Поэтому его
- 16. Алюминиевая посуда и под воздействием кипящего молока и вареных овощей в микроскопических дозах отщепляется от емкости
- 17. По некоторым исследованиям поступление алюминия в организм человека было сочтено фактором в развитии болезни Альцгеймера
- 18. Рассмотрите электрохимический ряд металлов. Li K Ba Ca Na Mg Al Mn Cr Zn Fe Co
- 19. Алюминий – самый распространенный в природе элемент, по содержанию в земной коре (8%) находится на третьем
- 20. Бокситы – Al2O3 • H2O Нефелины – KNa3[AlSiO4]4 Глиноземы - Al2O3 Be3Al2Si6O18 Берилл Гранат Ca3Al2(SiO4)3
- 21. AL2O3 Глинозём Корунд сапфир рубин Боксит
- 22. Применение сапфиров и рубинов знаменитые сапфиры английской королевской семьи
- 23. «алюминий есть самый распространенный в природе; достаточно указать на то, что он входит в состав глины,
- 24. физические свойства Возьмите алюминиевую проволоку, рассмотрите ее, попробуйте изменить ее форму. На основании наблюдения и вашего
- 25. Алюминий как простое вещество химические свойства Если поверхность алюминия потереть солью ртути, то происходит реакция: 2Al
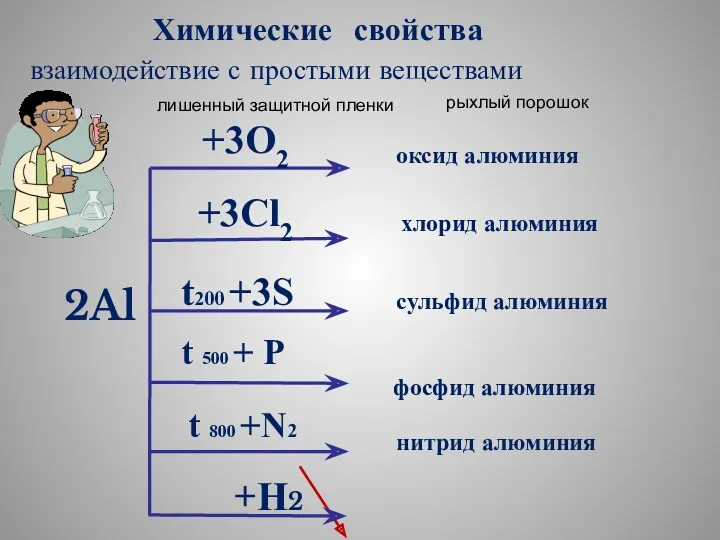
- 26. 2Al +3O2 оксид алюминия +3Cl2 хлорид алюминия t200 +3S сульфид алюминия фосфид алюминия +Н2 нитрид алюминия
- 27. взаимодействие с водой Если в отсутствии воздуха удалить с поверхности алюминия оксидную пленку, то он активно
- 28. Химические свойства взаимодействие со сложными веществами 2Al + 6H2SO4 = Al2(SO4)3 + 3SO2 + 6H2O 2.
- 29. взаимодействие со щелочами 2Al + 2NaOH + 6H2O=2Na[Al(OH)4] + 3H2 1. 2NaOH + Al2O3 + 3H2O=2Na[Al(OH)4]
- 30. 8Al + 3Fe3O4 = 9Fe + 4Al2O3 8 Al0 - 3ē → Al+3 – окисление, восстановитель
- 31. Датский физик Ганс Эрстед (1777-1851) Впервые алюминий был получен им в 1825 году действием амальгамы калия
- 32. Будучи студентом Оберлинского колледжа, он узнал, что можно разбогатеть и получить благодарность человечества, если изобрести способ
- 33. Поль Эру (1863-1914) – французский инженер - химик В 1889 году открыл алюминиевый завод во Фроне
- 34. Современное получение алюминия Современные метод получения был разработан независимо друг от друга: американцем Чарльзом Холлом и
- 35. Получение алюминия в промышленности Алюминий получают электрохимическим методом из бокситов. 2Al2O3 ток> 4Al + 3O2
- 36. Алюминий
- 37. Авиастроение Применение Al и его сплавов во всех видах транспорта, а в особенности воздушного привело к
- 38. Кораблестроение Al и его сплавы применяют при отделке и изготовлении корпусов и дымовых труб судов, спасательных
- 39. Пищевая промышленность Алюминиевая фольга – упаковочный материал для пищевых продуктов. Алюминиевая тара используется для консервирования и
- 40. Машиностроение Моторы, блоки, головки цилиндров, картеры, коробки передач, насосы и многие другие детали также изготавливают из
- 41. Электротехника Алюминий и его сплавы используют в электротехнической промышленности для изготовления кабелей, шинопроводов, конденсаторов, выпрямителей переменного
- 42. Военная промышленность Алюминий, а также его сплавы является стратегическим металлом и широко используется в военной промышленности
- 43. Соединения алюминия. Оксид Очень твердый порошок белого цвета. Образуется: а) при окислении или горении алюминия: 4Al
- 44. Химические свойства оксида алюминия Взаимодействует: а) с кислотами: Al2O3 + 3H2SO4 = Al2(SO4)3 + 3H2O Al2O3
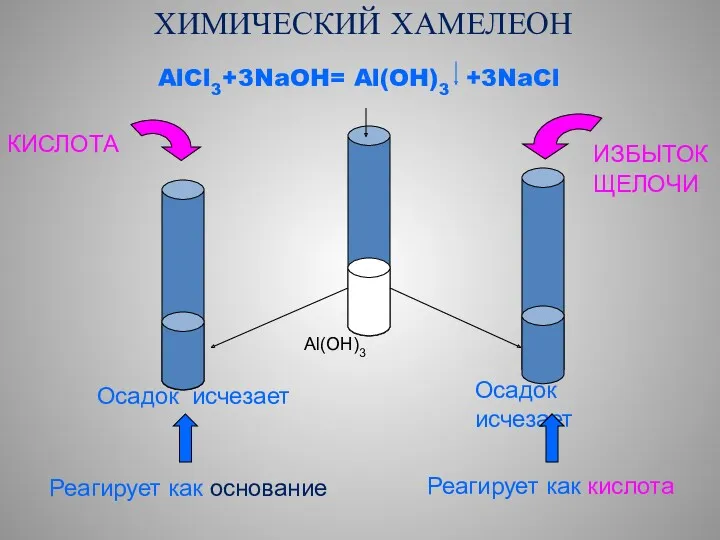
- 45. ХИМИЧЕСКИЙ ХАМЕЛЕОН AlCl3+3NaOH= Al(OH)3 +3NaCl Al(OH)3 КИСЛОТА ИЗБЫТОК ЩЕЛОЧИ Осадок исчезает Реагирует как основание Осадок исчезает
- 46. Амфотерный гидроксид Как основание: Al(OH)3 + 3HCl → AlCl3 + 3H2O Как кислота Al(OH)3 + NaOH
- 47. Гель из гидроксида алюминия входит в состав лекарст для лечения болезней желудка. Гидроксид алюминия используется для
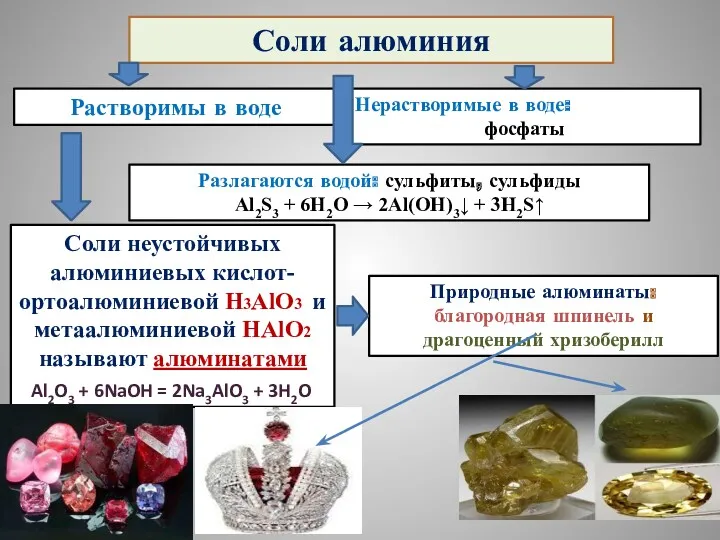
- 48. Соли алюминия Растворимы в воде Нерастворимые в воде: фосфаты Разлагаются водой: сульфиты, сульфиды Al2S3 + 6H2O
- 50. Алюминий Al «Он яркой звездой загорится, Белый и легкий металл, В 13-й клетке таблицы Почетное место
- 51. Э Т О И Н Т Е Р Е С Н О: Алюминий найдет свое место
- 52. 1 М Н Р Е Т О Ф К Р О И Л И Т Е
- 53. Какие из соединений вступят в реакцию с алюминием: Cl2 K2O CuSO4 H2O S BaSO4 HCL Cr
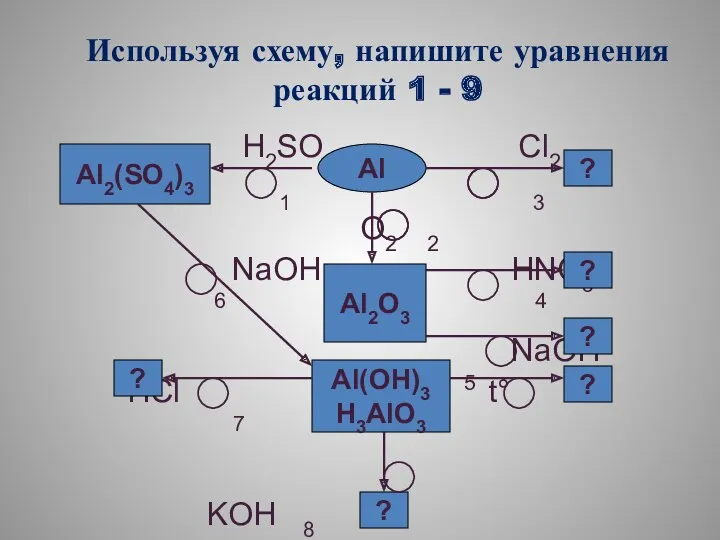
- 54. Используя схему, напишите уравнения реакций 1 - 9 H2SO4 Cl2 1 3 O2 2 NaOH HNO3
- 56. Скачать презентацию















![Бокситы – Al2O3 • H2O Нефелины – KNa3[AlSiO4]4 Глиноземы - Al2O3 Be3Al2Si6O18 Берилл Гранат Ca3Al2(SiO4)3](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/286262/slide-19.jpg)







![взаимодействие со щелочами 2Al + 2NaOH + 6H2O=2Na[Al(OH)4] + 3H2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/286262/slide-28.jpg)





















 Химические формулы
Химические формулы От алхимии к химии
От алхимии к химии Фенол и его свойства. (10 класс)
Фенол и его свойства. (10 класс) Introduction to Biochemistry
Introduction to Biochemistry Көмірсулар Қайталау сабағы
Көмірсулар Қайталау сабағы Свойства и биологическая роль карбонильных соединений
Свойства и биологическая роль карбонильных соединений 20231011_8_klass_binarnye_soedineniya
20231011_8_klass_binarnye_soedineniya Маңызды мұнай өнімдері
Маңызды мұнай өнімдері Предмет органической химии. 9 класс
Предмет органической химии. 9 класс Алкены – непредельные углеводороды. Получение, химические свойства и применение
Алкены – непредельные углеводороды. Получение, химические свойства и применение Методика изучения и описание вулканогенных обломочных пород
Методика изучения и описание вулканогенных обломочных пород Коллигативные свойства растворов неэлектролитов
Коллигативные свойства растворов неэлектролитов Высокомолекулярные соединения. Общие понятия
Высокомолекулярные соединения. Общие понятия Жуғыш заттардың адам өміріндегі маңызы. Химиялық өнімдердің адам өміріндері маңызы
Жуғыш заттардың адам өміріндегі маңызы. Химиялық өнімдердің адам өміріндері маңызы Дефекты в твердых телах
Дефекты в твердых телах Степень окисления. Определение степени окисления в соединениях
Степень окисления. Определение степени окисления в соединениях Амфотерность
Амфотерность Жиры (триглицериды)
Жиры (триглицериды) Состав, строение и свойства стекла и хрусталя
Состав, строение и свойства стекла и хрусталя Тема 11 -Дисперсные системы
Тема 11 -Дисперсные системы Кристаллическое строение и кристаллизация металлов
Кристаллическое строение и кристаллизация металлов Агрегатные состояния вещества с точки зрения атомно-молекулярных представлений
Агрегатные состояния вещества с точки зрения атомно-молекулярных представлений Медь и её соединения
Медь и её соединения Оксиды
Оксиды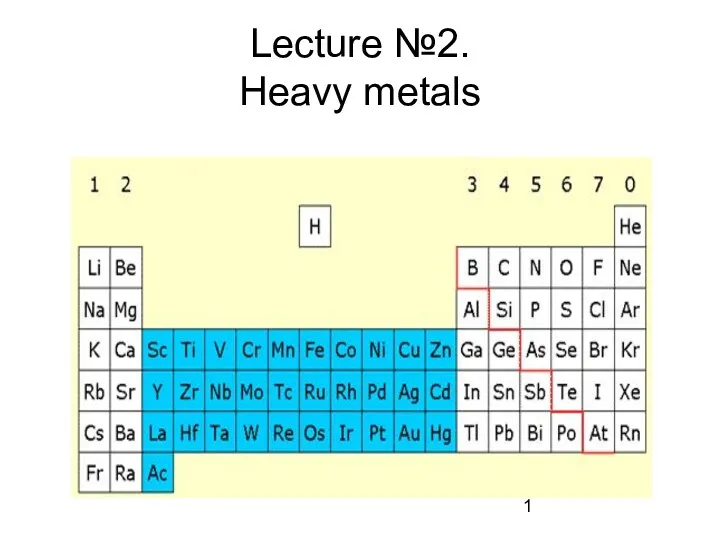 Heavy metals
Heavy metals Хром
Хром Биологическая химия (введение)
Биологическая химия (введение) Арены. Бензол
Арены. Бензол